Cho 2,7 gam Al vào V ml dung dịch HCL 3M .Phản ứng xảy ra hoàn toàn
a. Viết phương trình hóa học
b. Tính V
Năm 2,7 gam Al vào 200 gam dung dịch CH3COOH 10% đến khi phản ứng xảy ra hoàn toàn thu được dung dịch A và khí B a, Viết phương trình phản ứng hóa học đã xảy ra b, tính thể tích khí B thu được ở dktc và khối lượng axit CH3COOH đã tham gia phản ứng c, tính nồng độ phần trăm của các chất có trong dung dịch A sau phản ứng
\(a)2Al + 6CH_3COOH \to 2(CH_3COO)_3Al + 3H_2\\ b)n_{Al} = \dfrac{2,7}{27} = 0,1(mol) ; n_{CH_3COOH} = \dfrac{200.10\%}{60} = \dfrac{1}{3}(mol)\\ n_{CH_3COOH} = \dfrac{1}{3}> 3n_{Al} = 0,3 \to CH_3COOH\ dư\\ n_{H_2} = \dfrac{3}{2}n_{Al} = 0,15(mol) \Rightarrow V_{H_2} = 0,15.22,4 = 3,36(lít)\\ n_{CH_3COOH\ pư} = 3n_{Al} =0,3(mol) \Rightarrow m_{CH_3COOH\ pư} = 0,3.60 = 18(gam)\\ c) m_{dd} = 2,7 + 200 - 0,15.2 = 202,4(gam)\\ n_{(CH_3COO)_3Al} = n_{Al} = 0,1(mol)\\ m_{CH_3COOH\ dư} = 200.10\% - 18 = 2(gam)\\ C\%_{(CH_3COO)_3Al} = \dfrac{0,1.204}{202,4}.100\% = `10,08\%\\ \)
\(C\%_{CH_3COOH} = \dfrac{2}{202,4}.100\% = 0,988\%\)
Hoà tan hoàn toàn 7,2 gam magiê vào 300ml dụng dịch HCL thu được V lít H2 ở điều kiện tiêu chuẩn A / viết phương trình phản ứng hóa học xảy ra B/ tính V h2 sinh ra ở điều kiện tiêu chuẩn C/ tính nồng độ mol dung dịch HCL đã dùng
`a)PTHH:`
`Mg + 2HCl -> MgCl_2 + H_2`
`0,3` `0,6` `0,3` `0,3` `(mol)`
`b) n_[Mg] = [ 7,2 ] / 24 = 0,3 (mol)`
`=> V_[H_2] = 0,2 . 22,4 =6,72 (l)`
`c) C_[M_[HCl]] = [ 0,6 ] / [ 0,3 ] = 2 (M)`
Cho m gam một mẩu kim loại Ba tan hết vào 100 ml dung dịch A gồm HCl 0,08M và Al2(SO4)3 0,5M. Sau các phản ứng thu được dung dịch X, kết tủa Y và khí Z. Khối lượng dung dịch X giảm so sới dung dịch A là 14,19 gam. Thêm tiếp V ml dung dịch HCl 1M vào dung dịch X thấy xuất hiện 0,78gam kết tủa. Biết các phản ứng xảy ra hoàn toàn.
Viết phương trình phản ứng xảy ra và tính giá trị của m, V.
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
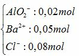 + V ml HCl 1M→ Al(OH)3: 0,01 (mol)
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
nHCl = 0,1. 0,8 = 0,08 (mol) ; nAl2(SO4)3 = 0,1.0,5 = 0,05 (mol) => nAl3+ = 0,1 (mol); nSO42- = 0,15 (mol)
Gọi số mol Ba là x (mol)
Ba + 2HCl → BaCl2 + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
3BaCl2 + Al2(SO4)3 → 3BaSO4 ↓+ 2AlCl3
3Ba(OH)2 + Al2(SO4)3 → BaSO4↓ + 2Al(OH)3↓
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 + 4H2O
Vì dd X + HCl sinh ra 0,78 gam kết tủa Al(OH)3 : 0,1 (mol) nên trong dung dịch X chắc chắn có chứa Ba(AlO2)2 => lượng OH- sinh ra đã hòa tan 1 phần lượng kết tủa Al(OH)3
Ba + 2H+ → Ba2+ + H2↑
0,04 ← 0,08 (mol)
Ba + 2H2O → Ba2+ + 2OH- + H2↑
(x – 0,04 ) → (2x – 0,08) (mol)
Ba2+ + SO42- → BaSO4
3OH- + Al3+ → Al(OH)3↓
OH- + Al(OH)3 → AlO2- + 2H2O
Vì Al(OH)3 bị hòa tan 1 phần
=> nOH - > 3nAl3+
=> 2x – 0,08 > 3. 0,1
=> x > 0,19
=> nBa2+ > 0,19 (mol) => SO42- bị kết tủa hết => nBaSO4 = nSO42- = 0,15 (mol)
Mặt khác: nOH- = 4nAl3+ - nAl(OH)3 còn lại => nAl(OH)3 còn lại = 0,48 – 2x (mol)
=> nAl(OH)3 còn lại = 0,32 – 2x (mol)
mdd giảm = mBaSO4 + mAl(OH)3 còn lại + mH2 - mBa
=> 0,15.233 + (0,48 – 2x).78 + 2x - 137x = 14,19
=> 291x = 58,2
=> x = 0,2 (mol)
=> mBa = 0,2. 137 = 27,4 (g)
Vậy dung dịch X chứa:
+ V ml HCl 1M→ Al(OH)3: 0,01 (mol)
TH1: AlO2- dư, H+ hết
AlO2- + H+ + H2O → Al(OH)3↓
=> nH+ = nAl(OH)3 = 0,01 (mol) => VHCl = n: CM = 0,01 (lít) = 10 (ml)
TH2: AlO2- , H+ đều phản ứng hết, kết tủa sinh ra bị hòa tan 1 phần
AlO2- + H+ + H2O → Al(OH)3↓
0,02 → 0,02 → 0,02 (mol)
H+ + Al(OH)3 → Al3+ + 2H2O
0,01← (0,02 – 0,01) (mol)
=> nH+ = 0,02 + 0,01 = 0,03 (mol) => VHCl = n : CM = 0,03 (lít) = 30 (ml)
Hòa tan hoàn toàn m gam Al2O3 cần tối thiểu 400 ml dung dịch HCl 1,5m
a,Viết phương trình hóa học của phản ứng xảy ra
b,Tính m và nồng độ mol của chất tan trong dung dịch sau phản ứng
a)
$Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O$
b)
n HCl = 0,4.1,5 = 0,6(mol)
n Al2O3 = 1/6 n HCl = 0,1(mol) => m = 0,1.102 = 10,2(gam)
n AlCl3 = 1/3 n HCl = 0,2(mol) => CM AlCl3 = 0,2/0,4 = 0,5M
nHCl = 0.4*1.5 = 0.6 (mol)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
nAlCl3 = 0.6*2/6 = 0.2 (mol)
mAlCl3 = 0.2*133.5 = 26.7 (g)
CM AlCl3 = 0.2/0.4 = 0.5 (M)
cho 5 ,4 gam al tác dụng với dung dịch hcl phản ứng xảy ra hoàn toàn . Dẫn toàn bộ lượng khí thu được qua CuO nung nóng .
a.viết phương trình hóa học của phản ứng xảy ra .tính khối lượng muối thu được saub phản ứng
b. tính khối lượng Cu qua phản ứng
a) nAl=0,2(mol)
PTHH: 2 Al + 6 HCl -> 2 AlCl3 + 3 H2
H2 + CuO -to-> Cu + H2O
nAlCl3= nAl= 0,2(mol)
=> mAlCl3= 133,5. 0,2= 26,7(g)
b) nCu= nH2= 3/2 . 0,2=0,3(mol)
=> mCu= 0,3.64=19,2(g)
(Qua phản ứng nghe kì á, chắc tạo thành chứ ha)
<3
Hòa tan m gam nhôm vào lượng vừa đủ 200 ml dung dịch HCl 1,5M thu được muối và V lít khí H2 (0⁰C, 1atm)
a) viết phương trình hóa học của phản ứng xảy ra
b) tính giá trị V và m
\(a,2Al+6HCl\rightarrow2AlCl_3+3H_2\\ n_{HCl}=0,2.1,5=0,6\left(mol\right)\\ n_{H_2}=\dfrac{3}{6}.0,6=0,3\left(mol\right);n_{Al}=\dfrac{2}{6}.0,6=0,2\left(mol\right)\\ b,V=V_{H_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\\ m=m_{Al}=0,2.27=5,4\left(g\right)\)
a)PTHH: AgNO3 + HCl → AgCl↓ + HNO3
nHCl = 0,2.0,5 = 0,1 mol
=> nAgCl = 0,1 mol = nAgNO3 = 0,1 mol = nHCl phản ứng
<=> mAgCl = 0,1.143,5 = 14,35 gam
mAgNO3 = 0,1.170 = 17 gam
=> mdd AgNO3 = \(\dfrac{17}{6,8\%}\)= 250 gam
b) X + 2HCl --> XCl2 + H2
1,2 gam X tác dụng vừa đủ với 0,1 mol HCl
=> Số mol của 1,2 gam X = 0,05 mol
<=> Mx = \(\dfrac{1,2}{0,05}\)= 24 (g/mol) => X là magie ( Mg )
Hỗn hợp X gồm ba kim loại Al, Fe, Cu. Cho m gam hỗn hợp X vào dung dịch CuSO4 (dư) sau khi phản ứng xảy ra hoàn toàn thu được 35,2 gam kim loại. Nếu cũng hòa tan m gam hỗn hợp X vào 500 ml dung dịch HCl 2M đến khi phản ứng xảy ra hoàn toàn thu được 8,96 lít khí H2 (đktc), dung dịch Y và a gam chất rắn.Viết phương trình phản ứng xảy ra và tìm giá trị của a.
Cho 8,4 gam MgCO3 vào 500 ml dung dịch HCl a M. Sau phản ứng xảy ra hoàn toàn thu được dung dịch X và V lít khí CO2(đktc)
a. Tính V và a HCL đã dùng?
b. Tính khối lượng muối sau phản ứng
\(a,n_{MgCO_3}=\dfrac{8,4}{84}=0,1\left(mol\right)\)
PTHH: \(MgCO_3+2HCl\rightarrow MgCl_2+CO_2\uparrow+H_2O\)
0,1------->0,2-------->0,1-------->0,1
\(\rightarrow\left\{{}\begin{matrix}V=0,1.22,4=2,24\left(l\right)\\a=\dfrac{0,2}{0,5}=0,4M\end{matrix}\right.\\ b,m_{muối}=0,1.95=9,5\left(g\right)\)