hòa tan 4,8g một kim loại hóa trị II bằng dung dịch HCL sau phản ứng ta thu được 4,48 lít khí hidro ở đktc. Kim loại hóa trị II đó là gì ?

Những câu hỏi liên quan
Hòa tan hoàn toàn 23,8 gam hỗn hợp một muối cacbonat của các kim loại hóa trị I và muối cacbonat của kim loại hóa trị II trong dung dịch HCl. Sau phản ứng thu được 4,48 lít khí (đktc). Đem cô cạn dung dịch thu được thì khối lượng muối khan là: A. 13 g B. 15 g C. 26 g D. 30 g
Đọc tiếp
Hòa tan hoàn toàn 23,8 gam hỗn hợp một muối cacbonat của các kim loại hóa trị I và muối cacbonat của kim loại hóa trị II trong dung dịch HCl. Sau phản ứng thu được 4,48 lít khí (đktc). Đem cô cạn dung dịch thu được thì khối lượng muối khan là:
A. 13 g
B. 15 g
C. 26 g
D. 30 g
Đáp án C
Gọi công thức của hai muối trong hỗn hợp ban đầu là A2CO3 và BCO3.
Có các phản ứng:
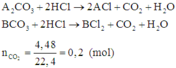
Quan sát phản ứng thấy khi cho hỗn hợp phản ứng với dung dịch HCl thì mỗi gốc C O 3 2 - trong muối được thay thế bởi hai gốc Cl-.
Có 1 mol C O 3 2 - bị thay thế bởi 2 mol Cl- thì khối lượng của muối tăng: (2.35,5 -60) = 11(gam)
Do đó khối lượng muối khan thu được khi cô cạn dung dịch là:
mmuối clorua = mmuối cacbonat + 0,2.11 = 23,8 + 0,2.11= 26 (gam)
Đúng 0
Bình luận (1)
Câu 1. Cho 2g hỗn hợp 2 kim loại Fe là kim loại hóa trị II vào dung dịch HCl dư thì thu được 1,12l khí H2(ĐKTC). Mặt khác nếu hòa tan 4,8g kim loại hóa trị II đó thì cần chưa tới 500ml dung dịch HCl 1M. Xác định kim loại hóa trị II.
Giúp MK với!!!
Cho 2g hỗn hợp gồm Fe và một kim loại Z hóa trị II vào dung dịch HCl dư thì thu được 1,12 lít khí (đktc). Xác định kim loại Z biết rằng 500ml dung dịch HCl hòa tan dư 4,8g kim loại đó
Sửa đề : Xác định kim loại Z biết rằng 500ml dung dịch HCl 1M hòa tan dư 4,8g kim loại đó
nH2=0,05 mol
PTHH:
Fe+2HCl→FeCl2+H2↑
Z + 2HCl →ZCl2+H2↑
Đặt công thức chung của hỗn hợp là N
N + 2HCl → NCl2 + H2
0,05______________0,05
⇒MN=\(\dfrac{2}{0,05}\)=40
Vì MFe =56>40
⇒MZ <40 (1)
Ta có : nHCl<0,5.1=0,5 mol
Z + 2HCl →ZCl2+H2↑
=> nZ < 0,25
=> MZ >\(\dfrac{4,8}{0,25}=19,2\)(2)
Từ (1), (2), ta có 19,2<MZ <40
Mà Z hóa trị II
⇒Z là Magie
Đúng 1
Bình luận (1)
Hòa tan hoàn toàn 0,5 gam Fe và một kim loại hóa trị II trong dung dịch HCl thu được 1,12 lít khí H2 đktc. Kim loại hóa trị II đó là kim loại nào sau đây.
A. Mg.
B. Ca.
C. Zn.
D. Be.
Đáp án D.
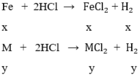
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là 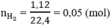
theo bài ra ta có hệ phương trình
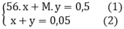
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
⇔ 2,8 – 56y + My = 0,5
2,3 = 56y – My
→ y = 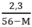
Ta có 0 < y < 0,05
y > 0 ↔ 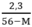 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56
y < 0,05 ↔ 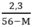 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10
Trong các kim loại hóa trị II chỉ có Be thỏa mãn do đó M là Be
Đúng 0
Bình luận (0)
Cho 4,8 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 4,48 lít H2 (đktc). Kim loại đó là ?
A. Ba
B. Ca
C. Mg
D. Sr
Đáp án C
Gọi kim loại là R.
![]() = 0,2 (mol)
= 0,2 (mol)
R + 2HCl → RCl2 + H2
0,2 ← 0,2 (mol)
![]() = 24(Mg)
= 24(Mg)
Đúng 0
Bình luận (0)
Cho 22,4 gam một kim loại hóa trị II tác dụng hết với dung dịch HCl, sau phản ứng thu được 8,96 lít khí hidro (đktc). Tìm tên kim loại
Hoà tan 16,8g kim loại vào dung dịch HCl dư, sau phản ứng thu được 6,72 lít khí H 2 (đktc). Kim loại đem hoà tan là (Biết trong muối thu được sau phản ứng kim loại có hóa trị II)
A. Mg
B. Zn
C. Pb
D. Fe
Hòa tan hoàn toàn 6 gam một kim loại M hóa trị II vào dung dịch HCl, sau phản ứng thu được 3,36 lit khí H 2 (đktc). Kim loại M là:
A. Zn (65)
B. Mg (24)
C. Fe (56)
D. Ca (40)
Chọn D
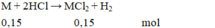
M M = 6 : 0 , 15 = 40 .
Vậy kim loại M là Ca.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 4,8 gam một kim loại R có hóa trị II vào 100 ml dung dịch HCl 5M. Sau phản ứng thu được 4,48 lít khí (đktc) và dung dịch A. Xác định R và tính nồng độ mol/lít các chất có trong dung dịch A.
PTHH: R + 2HCl ---> RCl2 + H2 (1)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{HCl}=\dfrac{100}{1000}.5=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,2}{1}< \dfrac{0,5}{2}\)
Vậy HCl dư.
Theo PT(1): \(n_R=n_{H_2}=0,2\left(mol\right)\)
=> \(M_R=\dfrac{4,8}{0,2}=24\left(g\right)\)
Vậy R là magie (Mg)
PT: Mg + 2HCl ---> MgCl2 + H2 (2)
Ta có: \(m_{dd_{MgCl_2}}=4,8+\dfrac{100}{1000}-0,2.2=4,5\left(lít\right)\)
Theo PT(2): \(n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,2}{4,5}=\dfrac{2}{45}M\)
Đúng 0
Bình luận (0)















