A và B là hai hợp chất đều có tỉ khối đối với H2 là 14. Đốt cháy A thu được sản phẩm chỉ có CO2. Đốt cháy 1,4 gam B thu được sản phẩm gồm 4,4 game CO2 và 1,8 gam H2O. Xác định công thức phân tử của A,B. Hãy cho biết A,B là hợp chất hữu cơ hay vô cơ.

Những câu hỏi liên quan
A và B là hai hợp chất đều có tỉ khối đối với
H
2
là 14. Đốt cháy A thu được sản phẩm chỉ có
CO
2
. Đốt cháy 1,4 gam B thu được sản phẩm gồm 4,4 gam
CO
2
và 1,8 gam
H
2
O. Xác định công thức phân tử của A, B. Hãy cho biết...
Đọc tiếp
A và B là hai hợp chất đều có tỉ khối đối với H 2 là 14. Đốt cháy A thu được sản phẩm chỉ có CO 2 . Đốt cháy 1,4 gam B thu được sản phẩm gồm 4,4 gam CO 2 và 1,8 gam H 2 O. Xác định công thức phân tử của A, B. Hãy cho biết A, B là hợp chất hữu cơ hay vô cơ.
Ta có M A = M B = 14 x 2 = 28 (gam).
A là hợp chất khi đốt chỉ tạo ra CO 2 . Vậy A phải chứa cacbon và oxi. Mặt khác, M A = 28 gam → công thức của A là CO.
B khi cháy sinh ra CO 2 và H 2 O, vậy trong B có cacbon và hiđro.
Ta có m C = 4,4/44 x 12 = 1,2g
m H = 1,8/18 x 2 = 0,2g
Vậy m B = m C + m H = 1,2 + 0,2 = 1,4 (gam).
=> Trong B chỉ có 2 nguyên tố là C và H.
Gọi công thức phân tử của B là C x H y , ta có :
4 C x H y + (4x +y) O 2 → 4x CO 2 + 2y H 2 O
n C x H y = 1,4/28 = 0,05mol
=> x = 2 ; y = 4. Công thức của B là C 2 H 4
Đúng 0
Bình luận (0)
Hợp chất hữu cơ A có tỷ khối đối với hiđro là 14. Đốt cháy 1,4 gam A thu được sản phẩm gồm 4,4 gam CO2 và 1,8 gam H,O. Xác định công thức phân tử của A?
cho mk xin gấp đ/an vs ạk
\(M_A=2.14=28\left(\dfrac{g}{mol}\right)\\ n_A=\dfrac{1,4}{28}=0,05\left(mol\right)\\ n_C=n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\\ n_H=2.n_{H_2O}=2.0,1=0,2\left(mol\right)\\ n_C:n_A=0,1:0,05=2;n_H:n_A=0,2:0,05=4\\ \Rightarrow CTPT.A:C_2H_4\)
Đúng 0
Bình luận (0)
Đốt cháy 4,5 gam chất hữu cơ A thu được sản phẩm gồm 6,6 gam CO2 và 2,7 gam H2O.
a. Hỏi A gồm có những nguyên tố nào?
b. Xác định công thức phân tử của A, biết khối lượng mol của hợp chất là 60g.
a.
Đốt cháy A thu được CO2 và H2O. Vậy A chứa nguyên tố C, H và có thể có O.
Ta có: \(n_C=\frac{6,6}{44}=0,15\left(mol\right),m_C=0,15.12=1,8\left(g\right)\)
\(n_{H_2O}=\frac{2,7}{18}=0,15\left(mol\right),m_H=0,15.2=0,3\left(g\right)\)
Khối lượng của Oxi : \(m_O=m_A-\left(m_H+m_C\right)=4,5-\left(1,8+0,3\right)=2,4g\)
Vậy A gồm có H, C và O.
Đúng 1
Bình luận (1)
b.
Đặt công thức cần tìm có dạng CxHyOz
Ta có: \(m_A=60g\text{/}mol\)
\(x=\frac{60.1,8}{4,5.12}=2;y=\frac{60.0,3}{4,5.1}=4;z=\frac{60.2,4}{4,5.16}=2\)
Vậy công thức cần tìm CxHyOz là C2H4O2
Đúng 1
Bình luận (2)
a.
Đốt cháy A thu được CO2 và H2O. Vậy A chứa nguyên tố C, H và có thể có O.
Ta có: nC=6,644=0,15(mol),mC=0,15.12=1,8(g)nC=6,644=0,15(mol),mC=0,15.12=1,8(g)
nH2O=2,718=0,15(mol),mH=0,15.2=0,3(g)nH2O=2,718=0,15(mol),mH=0,15.2=0,3(g)
Khối lượng của Oxi : mO=mA−(mH+mC)=4,5−(1,8+0,3)=2,4gmO=mA−(mH+mC)=4,5−(1,8+0,3)=2,4g
Vậy A gồm có H, C và O.
b.
Đặt công thức cần tìm có dạng CxHyOz
Ta có: mA=60g/molmA=60g/mol
x=60.1,84,5.12=2;y=60.0,34,5.1=4;z=60.2,44,5.16=2x=60.1,84,5.12=2;y=60.0,34,5.1=4;z=60.2,44,5.16=2
Vậy công thức cần tìm CxHyOz là C2H4O2
Đúng 1
Bình luận (0)
Hỗn hợp M gồm hai chất hữu cơ A và B (phân tử A có nhiều hơn phân tử B một nguyên tử cacbon). Đốt cháy hoàn toàn 12,96 gam hỗn hợp M bằng lượng khí oxi dư thu được sản phẩm cháy gồm H2O và 36,96 gam CO2. Biết tỉ khối hơi của hỗn hợp M so với H2 là 13,5.a) Tìm công thức phân tử và tính thành phần phần trăm theo khối lượng mỗi chất có trong hỗn hợp M.b) Khi dẫn toàn bộ sản phẩm cháy vào 552,9 gam dung dịch Ba(OH)2 20,72% thu được m gam chất kết tủa và dung dịch Z. Tìm giá trị của m và tính nồng độ...
Đọc tiếp
Hỗn hợp M gồm hai chất hữu cơ A và B (phân tử A có nhiều hơn phân tử B một nguyên tử cacbon). Đốt cháy hoàn toàn 12,96 gam hỗn hợp M bằng lượng khí oxi dư thu được sản phẩm cháy gồm H2O và 36,96 gam CO2. Biết tỉ khối hơi của hỗn hợp M so với H2 là 13,5.
a) Tìm công thức phân tử và tính thành phần phần trăm theo khối lượng mỗi chất có trong hỗn hợp M.
b) Khi dẫn toàn bộ sản phẩm cháy vào 552,9 gam dung dịch Ba(OH)2 20,72% thu được m gam chất kết tủa và dung dịch Z. Tìm giá trị của m và tính nồng độ C% của chất tan có trong dung dịch Z
Đốt cháy hoàn toàn 23 gam hợp chất hữu cơ A thu được sản phẩm gồm 44 gam CO2 và 27 gam H2O.
a) Hỏi trong A có những nguyên tố nào?
b) Xác định công thức phân tử của A, biết tỉ khối của A so với hidro bằng 23.
Đốt cháy A thu được CO2 và H2O.
Vậy A chứa cacbon, hidro và có thể có oxi.
mC = 44/44 x 12 = 12 (gam)
mH = 27/18 x 2 = 3 (gam)
Theo đề bài, ta có mO = mA – mC – mH => mO = 23 – 12 – 3 = 8 (gam) Trong A có 3 nguyên tố C,H,O và có công thức CxHyOz
Theo đề bài ta có: MA/2 = 23, vậy mA = 46
Cứ 23 gam A có 12 gam cacbon 46 gam A có 12x gam cacbon
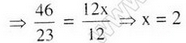
Tương tự ta có y = 6, z = 1
Vậy công thức của A là C2H6O
Đúng 5
Bình luận (0)
Đốt cháy hoàn toàn 1,8 gam hợp chất hữu cơ (A) thu được 1,792 lít CO2
(đktc) và 1,8 gam H2O. Tỉ khối của A so với H2 là 45. Xác định công thức phân tử
và công thức đơn giản nhất của A. (Cho biết C = 12, H = 1; O =16, N= 14)
$n_C = n_{CO_2} = \dfrac{1,792}{22,4} = 0,08(mol)$
$n_H = 2n_{H_2O} = 2.\dfrac{1,8}{18} = 0,2(mol)$
$n_O = \dfrac{1,8 - 0,08.12 - 0,2.1}{16} = 0,04(mol)$
Ta có :
$n_C : n_H : n_O = 0,08 : 0,2 : 0,04 = 2 : 5 : 1$
Vậy CTĐGN là $C_2H_5O$
CTPT : $(C_2H_5O)_n$
$M_A = (12.2 + 5 + 16)n = 45.2 \Rightarrow n = 2$
Vậy CTPT là $C_4H_{10}O_2$
Đúng 2
Bình luận (0)
\(n_{CO_2}=\dfrac{1.792}{22.4}=0.08\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(n_O=\dfrac{1.8-0.08\cdot12-0.1\cdot2}{16}=0.04\left(mol\right)\)
\(n_C:n_H:n_O=0.08:0.2:0.04=2:5:1\)
Công thức đơn giản nhất : C2H5O
\(M_A=2\cdot45=90\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow45n=90\)
\(\Rightarrow n=2\)
\(CT:C_4H_{10}O_2\)
Đúng 1
Bình luận (0)
53. Đốt cháy hoàn toàn một hợp chất hữu cơ A có dạng CxHyO thu đc sản phẩm cháy chỉ gồm CO2 và H2O với tỉ lệ khối lượng tương ứng là 44:27 . Công thức phân tử của A?
Xem chi tiết
Ta có CTPT: Cx Hy O
Suy ra: n CO2 = x (mol) Suy ra: m CO2 = 44x ( g)
Suy ra: n H2O = 0,5y (mol) Suy ra: m H2O = 9y ( g)
Ta lại có:44x/9y = 44/27
Suy ra: x/y = 1/3
Suy ra Công thức hóa học phân tử A là C2H6O.
Đúng 0
Bình luận (4)
Đốt cháy hoàn toàn 30 gam một hợp chất hữu cơ A thu được sản phẩm gồm 22,4 lít khí CO2 điều kiện tiêu chuẩn và 18 g H2O
a) xác định công thức phân tử của a biết tỉ khối hơi của a so với Oxi là1,1875l
b) Viết công thức phân tử của a biết ai vừa tác dụng được với NaOH
- Sửa đề xíu 1,875 chứ không phải 1,1875
MA=1,875.32=60\(\rightarrow\)\(n_A=\dfrac{30}{60}=0,5mol\)
\(n_{CO_2}=\dfrac{22,4}{22,4}=1mol\)
\(n_{H_2O}=\dfrac{18}{18}=1mol\)
- Đặt công thức CxHyOz
CxHyOz+\(\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)\)\(\rightarrow\)xCO2+\(\dfrac{y}{2}\)H2O
x=\(\dfrac{n_{CO_2}}{n_A}=\dfrac{1}{0,5}=2\)
\(\dfrac{y}{2}=\dfrac{n_{H_2O}}{n_A}=\dfrac{1}{0,5}=2\rightarrow y=4\)
MA=12.2+4+16z=60\(\rightarrow\)16z=32\(\rightarrow\)z=2
CTPT: C2H4O2
A tác dụng NaOH nên A có thể là este hoặc axit:
Este: HCOOCH3
Axit: CH3COOH
Đúng 0
Bình luận (0)
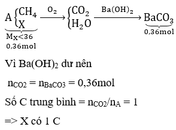
Hỗn hợp A gồm metan và một hợp chất hữu cơ X. Tỉ khối hơi của X so với hiđro nhỏ hơn 18. Đốt cháy hoàn toàn V lít A thu được sản phẩm chỉ gồm CO2 và H2O. Cho sản phẩm cháy hấp thụ hết vào dung dịch Ba(OH)2 lấy dư thấy tạo thành 70,92 gam kết tủa. Xác định các công thức phân tử có thể có của X. Biết rằng: V lít A đúng bằng thể tích của 11,52 gam khí O2 được đo trong cùng điều kiện nhiệt độ và áp suất.
Đọc tiếp
Hỗn hợp A gồm metan và một hợp chất hữu cơ X. Tỉ khối hơi của X so với hiđro nhỏ hơn 18. Đốt cháy hoàn toàn V lít A thu được sản phẩm chỉ gồm CO2 và H2O. Cho sản phẩm cháy hấp thụ hết vào dung dịch Ba(OH)2 lấy dư thấy tạo thành 70,92 gam kết tủa. Xác định các công thức phân tử có thể có của X. Biết rằng: V lít A đúng bằng thể tích của 11,52 gam khí O2 được đo trong cùng điều kiện nhiệt độ và áp suất.