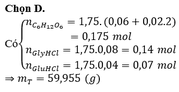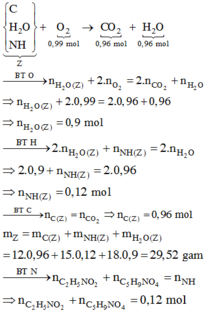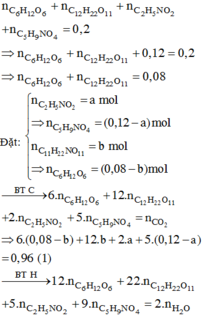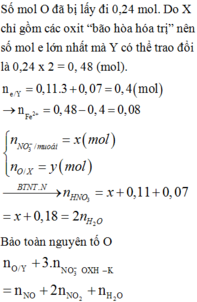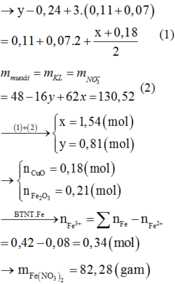13 Trong một bình kín dung tích 15 lít, chứa đầy dung dịch Ca(OH)2 0,01M. Sục vào bình một số mol CO2 có giá trị biến thiên 0,12mol £ nCO2 £ 0,26 mol muối thì khối lượng m gam chất rắn thu được sẽ có giá trị nhỏ nhất và lớn nhất là?

Những câu hỏi liên quan
Một bình kín chứa 46,54 gam hỗn hợp X gồm Mg, Cu(NO3)2. Thêm vào bình một lượng C rồi nung nóng bình (không có không khí) một thời gian thì thấy không còn C dư, thu được hỗn hợp rắn Y và 5,152 lít (đktc) hỗn hợp khí Z gồm NO2 (0,19 mol), CO2, O2. Hòa tan hoàn toàn Y trong dung dịch chứa m gam HC1 sau phản ứng chỉ thu được dung dịch T chứa (m + 30,184) gam các muối và a mol NO (sản phẩm khử duy nhất). Phần trăm khối lượng của Cu(NO3)2 trong X gần nhất với giá trị nào sau đây? A. 35% B. 77% C. 6...
Đọc tiếp
Một bình kín chứa 46,54 gam hỗn hợp X gồm Mg, Cu(NO3)2. Thêm vào bình một lượng C rồi nung nóng bình (không có không khí) một thời gian thì thấy không còn C dư, thu được hỗn hợp rắn Y và 5,152 lít (đktc) hỗn hợp khí Z gồm NO2 (0,19 mol), CO2, O2. Hòa tan hoàn toàn Y trong dung dịch chứa m gam HC1 sau phản ứng chỉ thu được dung dịch T chứa (m + 30,184) gam các muối và a mol NO (sản phẩm khử duy nhất). Phần trăm khối lượng của Cu(NO3)2 trong X gần nhất với giá trị nào sau đây?
A. 35%
B. 77%
C. 69%.
D. 94%.
Trong bình kín (không có không khí) chứa 65,76 gam hỗn hợp A gồm Al, Al2O3, Fe3O4 và FeCO3. Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn. Khí thoát ra khỏi bình được dẫn qua dung dịch Ca(OH)2 dư thu được 24,0 gam kết tủa. Hỗn hợp rắn B còn lại trong bình được chia làm 2 phần bằng nhau + Phần 1 cho vào dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2. Sục khí CO2 đến dư vào dung dịch sau phản ứng thu được 21,84 gam kết tủa. + Phần 2 tác dụng hết với dung dịch chứa H2SO4 và 0,23 mol H...
Đọc tiếp
Trong bình kín (không có không khí) chứa 65,76 gam hỗn hợp A gồm Al, Al2O3, Fe3O4 và FeCO3. Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn. Khí thoát ra khỏi bình được dẫn qua dung dịch Ca(OH)2 dư thu được 24,0 gam kết tủa. Hỗn hợp rắn B còn lại trong bình được chia làm 2 phần bằng nhau
+ Phần 1 cho vào dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2. Sục khí CO2 đến dư vào dung dịch sau phản ứng thu được 21,84 gam kết tủa.
+ Phần 2 tác dụng hết với dung dịch chứa H2SO4 và 0,23 mol HNO3 thu được dung dịch Z chỉ chứa các muối sunfat của kim loại có khối lượng 93,36 gam và hỗn hợp khí gồm a mol NO và b mol N2O. Tỉ lệ a:b là
A. 3,75.
B. 3,25
C. 3,50.
D. 3,45.
Chọn đáp án A
nCO2 = 0,24 mol. Bảo toàn khối lượng: mB = 65,76 - 0,24 × 44 = 55,2(g).
► Xét 1 phần ⇒ mB = 27,6(g). Có H2 ⇒ Al dư ⇒ B gồm Al dư, Al2O3 và Fe.
⇒ nAl = 0,06 ÷ 1,5 = 0,04 mol || nAl(OH)3 = 0,28 mol ⇒ nAl2O3 = 0,12 mol.
→ m b nFe = 0,255 mol ⇒ nSO42– = (93,36 - 0,28 × 27 - 0,255 × 56) ÷ 96 = 0,745 mol.
⇒ nH2SO4 = 0,745 mol ⇒ ∑nH+ = 0,745 × 2 + 0,23 = 1,72 mol.
● ∑nH+ = 4nNO + 10nN2O + 2nO ⇒ 4a + 10b = 1. Bảo toàn nguyên tố Nitơ:
a + 2b = 0,23 mol ||⇒ giải hệ có: a = 0,15 mol; b = 0,04 mol.
⇒ a : b = 3,75 ⇒ chọn A.
Đúng 0
Bình luận (0)
Trong bình kín (không có không khí) chứa 65,76 gam hỗn hợp gồm Al, Al2O3, Fe3O4 và FeCO3. Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn. Khí thoát ra khỏi bình được dẫn qua dung dịch Ca(OH)2 dư thu được 24,0 gam kết tủa. Rắn còn lại trong bình được chia làm 2 phần bằng nhau. - Phần 1 cho vào dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2. Sục khí CO2 đến dư vào dung dịch sau phản ứng thu được 21,84 gam kết tủa. - Phần 2 tác dụng hết với dung dịch chứa H2SO4 và 0,23 mol HNO3 thu...
Đọc tiếp
Trong bình kín (không có không khí) chứa 65,76 gam hỗn hợp gồm Al, Al2O3, Fe3O4 và FeCO3. Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn. Khí thoát ra khỏi bình được dẫn qua dung dịch Ca(OH)2 dư thu được 24,0 gam kết tủa. Rắn còn lại trong bình được chia làm 2 phần bằng nhau.
- Phần 1 cho vào dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2. Sục khí CO2 đến dư vào dung dịch sau phản ứng thu được 21,84 gam kết tủa.
- Phần 2 tác dụng hết với dung dịch chứa H2SO4 và 0,23 mol HNO3 thu được dung dịch Z chỉ chứa các muối sunfat của kim loại có khối lượng 93,36 gam và hỗn họp khí gồm a mol NO và b mol N2O.
Tỷ lệ a : b là:
A. 3,75
B. 3,25
C. 3,50
D. 3.45
Đáp án A
· Có n FeCO 3 = n CO 2 = n CaCO 3 = 24 100 = 0 , 24 mol
· Phần 1: n Al = 2 3 n H 2 = 2 3 . 0 , 06 = 0 , 04 mol
Þ Al dư, hỗn hợp rắn sau phản ứng gồm Fe, Al2O3.
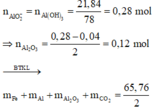 ⇒
m
Fe
=
32
,
86
-
44
.
0
,
24
2
-
102
.
0
,
12
-
27
.
0
,
04
=
14
,
28
g
⇒
n
Fe
=
0
,
255
mol
⇒
m
Fe
=
32
,
86
-
44
.
0
,
24
2
-
102
.
0
,
12
-
27
.
0
,
04
=
14
,
28
g
⇒
n
Fe
=
0
,
255
mol
· Phần 2: Đặt số mol muối Fe2(SO4)3 và FeSO4 lần lượt là x, y.
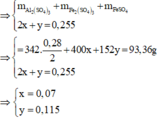
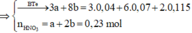
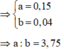
Đúng 0
Bình luận (0)
Trong bình kín (không có không khí) chứa 65,76 gam hỗn hợp A gồm Al, Al2O3, Fe3O4 và FeCO3. Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn. Khí thoát ra khỏi bình được dẫn qua dung dịch Ca(OH)2 dư thu được 24,0 gam kết tủa. Hỗn hợp rắn B còn lại trong bình được chia làm 2 phần bằng nhau + Phần 1 cho vào dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2. Sục khí CO2 đến dư vào dung dịch sau phản ứng thu được 21,84 gam kết tủa. + Phần 2 tác dụng hết với dung dịch chứa H2SO4 và 0,23 mol H...
Đọc tiếp
Trong bình kín (không có không khí) chứa 65,76 gam hỗn hợp A gồm Al, Al2O3, Fe3O4 và FeCO3. Nung bình ở nhiệt độ cao đến khi phản ứng xảy ra hoàn toàn. Khí thoát ra khỏi bình được dẫn qua dung dịch Ca(OH)2 dư thu được 24,0 gam kết tủa. Hỗn hợp rắn B còn lại trong bình được chia làm 2 phần bằng nhau
+ Phần 1 cho vào dung dịch NaOH dư thấy thoát ra 0,06 mol khí H2. Sục khí CO2 đến dư vào dung dịch sau phản ứng thu được 21,84 gam kết tủa.
+ Phần 2 tác dụng hết với dung dịch chứa H2SO4 và 0,23 mol HNO3 thu được dung dịch Z chỉ chứa các muối sunfat của kim loại có khối lượng 93,36 gam và hỗn hợp khí gồm a mol NO và b mol N2O. Tỉ lệ a:b là
A. 3,75.
B. 3,25
C. 3,50.
D. 3,45.
Chọn đáp án A
nCO2 = 0,24 mol. Bảo toàn khối lượng: mB = 65,76 - 0,24 × 44 = 55,2(g).
► Xét 1 phần ⇒ mB = 27,6(g). Có H2 ⇒ Al dư ⇒ B gồm Al dư, Al2O3 và Fe.
⇒ nAl = 0,06 ÷ 1,5 = 0,04 mol || nAl(OH)3 = 0,28 mol ⇒ nAl2O3 = 0,12 mol.
→ m B nFe = 0,255 mol ⇒ nSO42– = (93,36 - 0,28 × 27 - 0,255 × 56) ÷ 96 = 0,745 mol.
⇒ nH2SO4 = 0,745 mol ⇒ ∑nH+ = 0,745 × 2 + 0,23 = 1,72 mol.
● ∑nH+ = 4nNO + 10nN2O + 2nO ⇒ 4a + 10b = 1. Bảo toàn nguyên tố Nitơ:
a + 2b = 0,23 mol ||⇒ giải hệ có: a = 0,15 mol; b = 0,04 mol.
⇒ a : b = 3,75 ⇒ chọn A.
Đúng 0
Bình luận (0)
Sục V lít
CO
2
(đktc) vào dung dịch chứa a mol
Ba
(
OH
)
2
thì thu được 19,7 gam kết tủa (TN1). Mặt khác, sục V lít
CO
2
(đktc) vào dung dịch chứa a mol
Ba
(
OH
)
2
và a mol NaOH thì thu được 39,4 gam kết t...
Đọc tiếp
Sục V lít CO 2 (đktc) vào dung dịch chứa a mol Ba ( OH ) 2 thì thu được 19,7 gam kết tủa (TN1). Mặt khác, sục V lít CO 2 (đktc) vào dung dịch chứa a mol Ba ( OH ) 2 và a mol NaOH thì thu được 39,4 gam kết tủa (TN2). Giá trị của V và a tương ứng là:
A. 6,72 và 0,1
B. 5,6 và 0,2
C. 8,96 và 0,3
D. 6,72 và 0,2
Đáp án D
Lượng CO 2 tham gia phản ứng và lượng Ba ( OH ) 2 ở hai thí nghiệm đều bằng nhau, nhưng ở TN1 thu được lượng kết tủa ít hơn ở TN2. Suy ra ở TN1 kết tủa đã bị hòa tan một phần. Dựa vào tính chất của đồ thị ở TN1 suy ra :
n CO 2 = 2 n Ba ( OH ) 2 - n BaCO 3 = ( 2 a - 0 , 1 ) mol
Đồ thị biểu diễn sự biến thiên lượng kết tủa theo lượng CO 2 ở TN1 và TN2 :
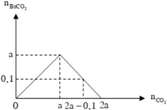
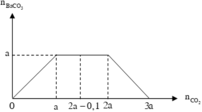
Dựa vào 2 đồ thị, ta thấy a < 2a - 0,1 < 2a nên ở TN2 kết tủa đạt cực đại. Suy ra :
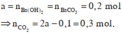
Vậy V = 6,72 lít và a = 0,2 mol
Đúng 0
Bình luận (0)
Hỗn hợp X gồm glucozơ và saccarozơ. Hỗn hợp Y gồm glyxin và axit glutamic. Đốt cháy hoàn toàn 0,2 mol hỗn hợp Z chứa X, Y cần dùng 0,99 mol O2, sản phẩm cháy gồm CO2, H2O và N2 (trong đó số mol CO2 bằng số mol H2O). Dẫn toàn bộ sản phẩm cháy qua bình chứa dung dịch Ca(OH)2 dư, thu được dung dịch có khối lượng giảm 36,48 gam. Nếu cho 51,66 gam Z trên vào dung dịch HCl loãng dư (đun nóng) thu được dung dịch T có chứa m gam các hợp chất hữu cơ. Giá trị của m là A. 53,655 B. 59,325 C. 60,125 D. 5...
Đọc tiếp
Hỗn hợp X gồm glucozơ và saccarozơ. Hỗn hợp Y gồm glyxin và axit glutamic. Đốt cháy hoàn toàn 0,2 mol hỗn hợp Z chứa X, Y cần dùng 0,99 mol O2, sản phẩm cháy gồm CO2, H2O và N2 (trong đó số mol CO2 bằng số mol H2O). Dẫn toàn bộ sản phẩm cháy qua bình chứa dung dịch Ca(OH)2 dư, thu được dung dịch có khối lượng giảm 36,48 gam. Nếu cho 51,66 gam Z trên vào dung dịch HCl loãng dư (đun nóng) thu được dung dịch T có chứa m gam các hợp chất hữu cơ. Giá trị của m là
A. 53,655
B. 59,325
C. 60,125
D. 59,955
Hỗn hợp X gồm glucozơ và saccarozơ. Hỗn hợp Y gồm glyxin và axit glutamic. Đốt cháy hoàn toàn 0,2 mol hỗn hợp Z chứa X, Y cần dùng 0,99 mol O2, sản phẩm cháy gồm CO2. H2O và N2, trong đó số mol CO2 bằng số mol của H2O. Dẫn toàn bộ sản phẩm cháy qua bình chứa dung dịch Ca(OH)2 dư, thu được dung dịch có khối lượng giảm 36,48 gam. Nếu cho 51,66 gam Z trên vào dung dịch HCl loãng dư (đun nóng) thu được dung dịch T có chứa m gam các hợp chất hữu cơ. Giá trị của m là: A.53,655. B. 59,325. C. 60,125....
Đọc tiếp
Hỗn hợp X gồm glucozơ và saccarozơ. Hỗn hợp Y gồm glyxin và axit glutamic. Đốt cháy hoàn toàn 0,2 mol hỗn hợp Z chứa X, Y cần dùng 0,99 mol O2, sản phẩm cháy gồm CO2. H2O và N2, trong đó số mol CO2 bằng số mol của H2O. Dẫn toàn bộ sản phẩm cháy qua bình chứa dung dịch Ca(OH)2 dư, thu được dung dịch có khối lượng giảm 36,48 gam. Nếu cho 51,66 gam Z trên vào dung dịch HCl loãng dư (đun nóng) thu được dung dịch T có chứa m gam các hợp chất hữu cơ. Giá trị của m là:
A.53,655.
B. 59,325.
C. 60,125.
D. 59,955.
Sục x mol
C
O
2
, với 0,12 mol ≤ x ≤ 0,26 mol , vào bình chứa 15 lit dd
C
a
O
H
2
0,01 M thu được m gam kết tủa thì giá trị của m: A. 12 g ≤ m ≤ 15 g B. 4 g ≤ m ≤ 12 g C. 0,12 g ≤ m ≤ 0,24 g D. 4 g ≤ m ≤ 15 g
Đọc tiếp
Sục x mol C O 2 , với 0,12 mol ≤ x ≤ 0,26 mol , vào bình chứa 15 lit dd C a O H 2 0,01 M thu được m gam kết tủa thì giá trị của m:
A. 12 g ≤ m ≤ 15 g
B. 4 g ≤ m ≤ 12 g
C. 0,12 g ≤ m ≤ 0,24 g
D. 4 g ≤ m ≤ 15 g
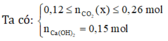
Nếu n C O 2 = x= 0,15 mol thì:
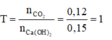
Chỉ tạo ra 1 muối C a C O 3 và khối lượng kết tủa thu được là tối đa.
C a O H 2 + C O 2 → C a C O 3 + H 2 O
0,15 0,15 mol
Nếu n C O 2 max = x = 0,26 mol thì:
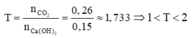
⇒ Tạo ra 2 muối C a C O 3 và C a H C O 3 2 và khi đó khối lượng kết tủa thu được là tối thiểu.
C O 2 + C a O H 2 → C a C O 3 + H 2 O 1
x…..x…..x......mol
2 C O 2 + C A O H 2 → C a H C O 3 2 2
2y…..y…..mol
Ta được hệ phương trình:
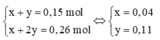
⇒ n C a C O 3 = x = 0,04 mol
⇒ m↓ = m C a C O 3 = 0,04.100 = 4 gam
Vậy 4 ≤ m↓ ≤ 15
⇒ Chọn D.
Đúng 0
Bình luận (0)
Dẫn luồng khí CO qua 48 gam hỗn hợp X gồm CuO, Fe2O3 nung nóng một thòi gian thu được chất rắn Y và hỗn hợp khí Z. Hấp thụ Z vào bình đựng Ca(OH)2 dư thu được 24 gam kết tủa. Hòa tan hoàn toàn Y trong dung dịch HNO3 thu được dung dịch T chỉ chứa 130,52 gam muối nitrat của kim loại và hỗn hợp khí chứa 0,11 mol NO và 0,07 mol NO2. Khối lượng muôi Fe(NO3)3 trong T gần nhất với giá trị nào sau đây? A. 19,4 B. 50,8 C. 101,6 D. 82,3
Đọc tiếp
Dẫn luồng khí CO qua 48 gam hỗn hợp X gồm CuO, Fe2O3 nung nóng một thòi gian thu được chất rắn Y và hỗn hợp khí Z. Hấp thụ Z vào bình đựng Ca(OH)2 dư thu được 24 gam kết tủa. Hòa tan hoàn toàn Y trong dung dịch HNO3 thu được dung dịch T chỉ chứa 130,52 gam muối nitrat của kim loại và hỗn hợp khí chứa 0,11 mol NO và 0,07 mol NO2. Khối lượng muôi Fe(NO3)3 trong T gần nhất với giá trị nào sau đây?
A. 19,4
B. 50,8
C. 101,6
D. 82,3