Câu 7: Đốt cháy hết 4,48 (l) hỗn hợp khí gồm metan và etilen thu được 5,6 (l) khí
cacbonic. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
a. Viết các phương trình hóa học của phản ứng.
b.Tính % thể tích mỗi khí trong hỗn hợp
Đốt cháy 4,48 l hỗn hợp khí metan và etilen cần phải dùng 11,2 l khí oxi.
a. Viết các phương trình hóa học của phản ứng.
b. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp.
(Biết rằng thể tích khí đo ở đktc)
a) PTHH: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
b) Đặt \(n_{CH_4}=x\left(mol\right);n_{C_2H_4}=y\left(mol\right)\). Khi đó \(22,4x+22,4y=4,48\) \(\Leftrightarrow x+y=0,2\)
Từ PTHH \(\Rightarrow n_{O_2\left(1\right)}=2x\left(mol\right)\)\(;n_{O_2\left(2\right)}=3y\left(mol\right)\). Khi đó \(2x.22,4+3y.22,4=11,2\) \(\Leftrightarrow2x+3y=0,5\)
Vậy ta có \(\left\{{}\begin{matrix}x+y=0,2\\2x+3y=0,5\end{matrix}\right.\Leftrightarrow x=y=0,1\left(mol\right)\)
\(\Rightarrow\%V_{CH_4}=\%V_{C_2H_4}=50\%\)
Đốt cháy hoàn toàn 5,6 lít khí metan (CH4) trong khí oxi, sau phản ứng thu được khí sunfurơ (SO2) và nước. Biết các khí đo ở điều kiện tiêu chuẩn.
a. Viết PTHH xảy ra.
b. Tính thể tích khí oxi cần dùng.
c. Tính thể tích khí sunfurơ thu được.
đang gấp cho mình xin dáp án
Đốt cháy hoàn toàn 3,6 g hỗn hợp metan và etilen thu được 5,6 l khí CO2 điều kiện tiêu chuẩn
A viết phương trình hóa học
b Tính khối lượng của từng chất trong hỗn hợp ban đầu
c Tính thể tích không khí điều kiện tiêu chuẩn cần đốt một lượng hiđrocacbon trên biết O2 chiếm 20% thể tích không khí
\(n_{CO_2}=\dfrac{5,6}{22,4}=0,25mol\)
\(\left\{{}\begin{matrix}CH_4:x\left(mol\right)\\C_2H_4:y\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}16x+28y=3,6\\BTC:x+2y=n_{CO_2}=0,25\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,05mol\\y=0,1mol\end{matrix}\right.\)
a)\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
b)\(m_{CH_4}=0,05\cdot16=0,8g\)
\(m_{C_2H_4}=0,1\cdot28=2,8g\)
c)\(\Sigma n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=2\cdot0,05+3\cdot0,1=0,4mol\)
\(\Rightarrow V_{O_2}=0,4\cdot22,4=8,96l\)
\(\Rightarrow V_{kk}=5V_{O_2}=5\cdot8,96=44,8l\)
Đốt cháy 4,48 lít benzen hỗn hợp khí gồm etan etilen, cần dùng 14,56 lít o2. Các khí đo ở điều kiện tiêu chuẩn a. viết phương trình xảy ra b. tính phần trăm thể tích mỗi khí trong hỗn hợp trên
Đốt cháy hoàn toàn 3,36,lít hỗ hợp khí A gồm metan và etan thu được 4,48 lít khí cacbonic. Các thể khí được đo ở điều kiện tiêu chuẩn. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp A.
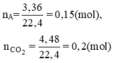
Gọi số mol của metan và etan lần lượt là x và y (mol)
Phương trình phản ứng:
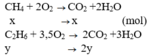
Vậy thành phần phần trăm về thể tích các khí trong hỗn hợp A là:
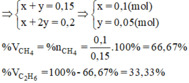
Để đốt cháy 5,6 lít khí etilen cần phải dùng:
a) Bao nhiêu lít oxi?
b) Bao nhiêu lít không khí chứa 1/5 thể tích oxi? Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Hỗn hợp A gồm CH4 và C2H4. Đốt cháy hoàn toàn 3,36 lít hỗn hợp A (đktc) thì thu được 8,8g khí cacbonic. Hãy tính thành phần % thể tích của mỗi khí trong hỗn hợp.
Câu 1:
\(a,PTHH:C_2H_4+5O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(n_{C_2H_4}=\dfrac{V_{\left(đktc\right)}}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(Theo.PTHH:n_{O_2}=5.n_{C_2H_4}=5.0,25=1,25\left(mol\right)\\ V_{O_2\left(đktc\right)}=n.22,4=1,25.22,4=28\left(l\right)\)
\(b,\Rightarrow V_{kk\left(đktc\right)}=5.V_{O_2\left(đktc\right)}=5.28=140\left(l\right)\)
B1:
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
Vì số mol tỉ lệ thuận với thể tích, đồng thời nhìn PTHH, ta sẽ được:
\(a,V_{O_2\left(đktc\right)}=3.V_{C_2H_4\left(đktc\right)}=3.5,6=16,8\left(l\right)\)
\(b,V_{kk}=5.V_{O_2\left(đktc\right)}=16,8.5=84\left(l\right)\)
B2:
Đặt số mol metan, etylen lần lượt là a,b (mol) (a,b>0)
\(n_{hh}=n_{CH_4}+n_{C_2H_4}=a+b=\dfrac{3,36}{22,4}=0,15\left(1\right)\)
PTHH: CH4 +2 O2 -to-> CO2 +2 H2O
C2H4 +3 O2 -to-> 2CO2 + 2H2O
\(n_{CO_2\left(tổng\right)}=a+2b=\dfrac{8,8}{44}=0,2\left(mol\right)\left(2\right)\)
(1), (2) =>a=0,1; b=0,05
Số mol tỉ lệ tương ứng với thể tích. Nên:
\(\%V_{CH_4}=\%n_{CH_4}=\dfrac{0,1}{0,15}.100\approx66,667\%\\ \Rightarrow\%V_{C_2H_4}\approx33,333\%\)
đốt cháy hoàn toàn 4,48 lít hỗn hợp khí metan và etylen cần dùng 15,68 lít khí o2 ( các khí đo ở đktc) a, viết phương trình phản ứng b, tính thể tích mỗi khí có trong hỗn hợp c, thể tích khí co2 thu được d, tính thành phần % của mỗi khí trong hỗn hợp ban đầu
a, \(CH_4+2O_2\underrightarrow{^{t^o}}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{^{t^o}}2CO_2+2H_2O\)
b, Gọi: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_4}=y\left(mol\right)\end{matrix}\right.\) \(\Rightarrow x+y=\dfrac{4,48}{22,4}=0,2\left(mol\right)\left(1\right)\)
Theo PT: \(n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=2x+3y=\dfrac{15,68}{22,4}=0,7\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=-0,1\\y=0,3\end{matrix}\right.\)
Đến đây thì ra số mol âm, bạn xem lại đề nhé.
Đốt cháy hoàn toàn 4,48 lít hỗn hợp 2 khí metan và etilen cần dùng 11,2 lít khí oxi.Phần trăm theo thể tích các khí trong hỗn hợp ban đầu lần lượt là(các thể tích khí đo ở cùng điều kiện nhiệt độ và áp suất)
Đốt cháy 5,6 l khí metan (CH4) cần V lít khí oxi a) viết phương trình phản ứng hoá học b) tính thể tích khí oxi(điều kiện tiêu chuẩn) và khối lượng nước sinh ra sau khi ngưng tụ
a)
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
b) Theo PTHH : $V_{O_2} = 2V_{CH_4} = 11,2(lít)$
$n_{CH_4} = \dfrac{5,6}{22,4} = 0,25(mol)$
Theo PTHH : $n_{H_2O} = 2n_{CH_4} = 0,5(mol)$
$m_{H_2O} = 0,5.18 = 9(gam)$
\(a,CH_4+2O_2\rightarrow CO_2+2H_2O\)
\(1:2:1:2\left(mol\right)\)
\(0,25:0,5:0,25:0,5\left(mol\right)\)
\(n_{CH_4}=\dfrac{V}{22,4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(b,V_{O_2}=n.22,4=0,5.22,4=11,2\left(l\right)\)
\(m_{H_2O}=n.M=0,5.18=9\left(g\right)\)