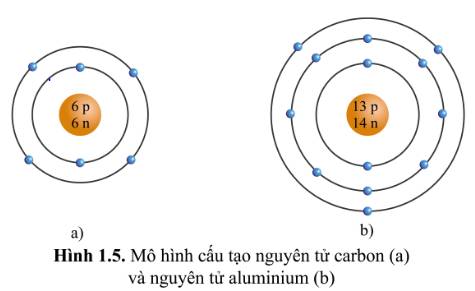
Quan sát hình ảnh mô tả cấu tạo nguyên tử carbon và nhôm (hình 1.5), hãy cho biết mỗi nguyên tử đó có bao nhiêu lớp electron và số electron trên mỗi lớp electron đó.
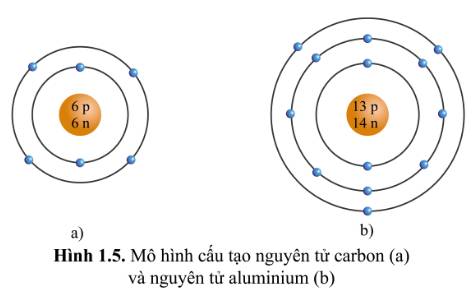
Quan sát hình 1.5, hãy cho biết:
a) Số proton, neutron, electron trong mỗi nguyên tử carbon và nhôm
b) Khối lượng nguyên tử của carbon và nhôm
`a,` Carbon:
`p = 6 , e = 6 , n = 6`
`Alu``mi``nium:`
`p = 13 , n = 14 , e = 13`
`b,`Khối lượng nguyên tử của Carbon: `p+n = 6+6 = 12 <am``u>`
Khối lượng nguyên tử của Nhôm: `p+n = 13+14 = 27 <am``u>`
Quan sát Hình 2.5, hãy cho biết nguyên tử nitrogen và potassium có bao nhiêu
a) điện tích hạt nhân nguyên tử?
b) lớp electron?
c) electron trên mỗi lớp?
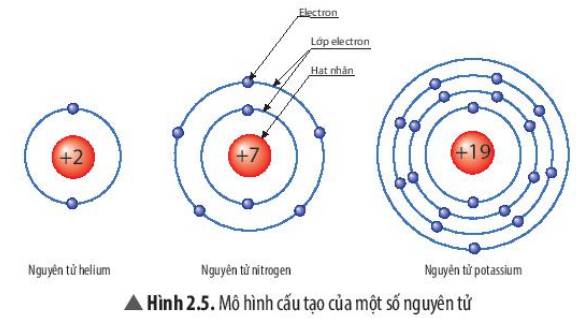
Nguyên tử nitrogen có:
-7 điện tích hạt nhân.
-2 lớp electron.
-Lớp 1 có 2 electron, lớp 2 có 5 electron.
Nguyên tử potassium có:
-19 điện tích hạt nhân.
-4 lớp electron.
-Lớp 1 có 2 electron, lớp 2 có 8 electron, lớp 3 có 8 electron, lớp 4 có 1 electron.
Quan sát hình 1.4, hãy cho biết nguyên tử natri có bao nhiêu lớp electron. Mỗi lớp có bao nhiêu electron?

nguyên tử natri có 3 lớp electron
+lớp thứ nhất có 2 electron
+lớp thứ hai có 8 electron
+lớp thứ ba có 1 electron
Cấu hình electron của: - Nguyên tử X: 1s22s22p63s23p64s1 - Nguyên tử Y: 1s22s22p63s23p4 a. Mỗi nguyên tử X và Y chứa bao nhiêu electron? b. Hãy cho biết số hiệu nguyên tử của X và Y. c. Lớp electron nào trong nguyên tử X và Y có mức năng lượng cao nhất? d. Mỗi nguyên tử X và Y có bao nhiêu lớp electron, bao nhiêu phân lớp electron? e. X và Y là nguyên tố kim loại, phi kim hay khí hiếm?
Hãy viết cấu hình electron của nguyên tử S (Z=16). Cho biết:
a, Nguyên tử lưu huỳnh có bao nhiêu lớp electron, mỗi lớp có bao nhiêu electron?
b, Phân lớp electron nào có mức năng lượng cao nhất?
Cấu hình electron của nguyên tử S (Z=16) : \(1s^22s^22p^63s^23p^4\)
a) Nguyên tử lưu huỳnh có 3 lớp electron
+ Lớp thứ nhất : 2e
+ Lớp thứ hai : 8e
+ Lớp thứ 3 : 6e
b) Phân lớp cuối cùng chứa mức năng lượng cao nhất : 3p
Quan sát Hình 6.2, em hãy mô tả sự tạo thành ion sodium, ion magnesium. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
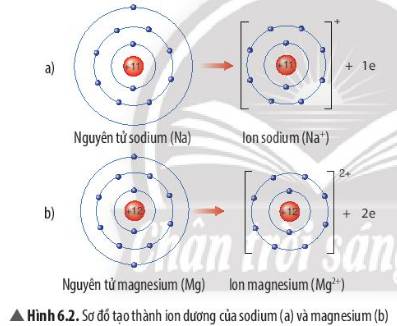
- Sự tạo thành ion sodium: Nguyên tử sodium (Na) cho đi 1 electron lớp ngoài cùng để tạo thành ion dương Na+
- Sự tạo thành ion magnesium: Nguyên tử magnesium (Mg) cho đi 2 electron lớp ngoài cùng để tạo thành ion dương Mg2+
=> Sau khi nhường electron, ion sodium và ion magnesium đều có 2 lớp electron và có 8 electron ở lớp ngoài cùng
=> Sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm Neon (Ne)
Quan sát Hình 6.3, em hãy mô tả sự tạo thành ion chloride, ion oxide. Nhận xét về số electron lớp ngoài cùng của các ion này và cho biết sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm nào?
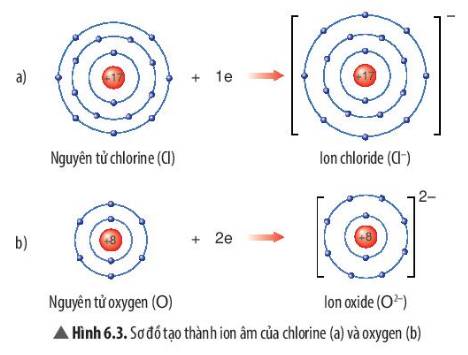
- Sự tạo thành ion chloride: Nguyên tử chlorine (Cl) nhận thêm 1 electron ở lớp ngoài cùng để tạo thành ion âm Cl-
- Sự tạo thành ion oxide: Nguyên tử oxygen (O) nhận thêm 2 electron ở lớp ngoài cùng để tạo thành ion âm O2-
- Sau khi nhận electron, ion chloride có 3 lớp electron và có 8 electron ở lớp ngoài cùng
=> Giống sự phân bố electron của nguyên tử khí hiếm Neon (Ne)
- Sau khi nhận electron, ion oxide có 2 lớp electron và có 8 electron ở lớp ngoài cùng
=> Giống sự phân bố electron của nguyên tử Argon (Ar)
Dựa vào các Hình 6.5, 6.6 và 6.7, em hãy cho biết số electron lớp ngoài cùng của mỗi nguyên tử trong phân tử hydrogen và oxygen là bao nhiêu? Khi đó, lớp electron ngoài cùng của nguyên tử hydrogen và nguyên tử oxygen sẽ giống với khí hiếm nào?
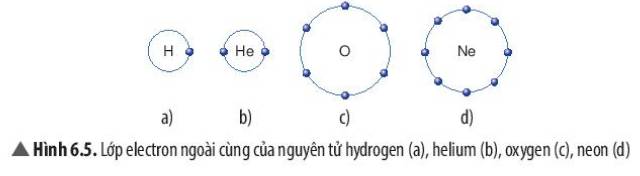

- Xét phân tử hydrogen: mỗi nguyên tử hydrogen có 2 electron lớp ngoài cùng
=> Giống cấu hình electron của nguyên tử khí hiếm Helium
- Xét phân tử Oxygen: mỗi nguyên tử Oxygen có 8 electron ở lớp ngoài cùng
=> Giống cấu hình electron của nguyên tử khí hiếm Neon
Quan sát hình 5.10, cho biết trong phân tử nước, mỗi nguyên tử H và O có bao nhiêu electron ở lớp ngoài cùng
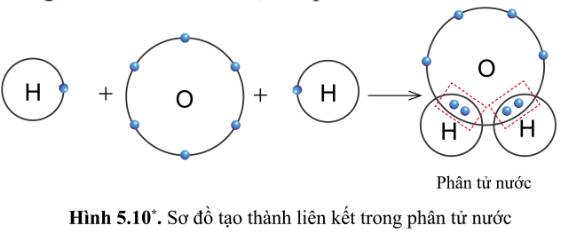
- Trong phân tử nước:
+ Nguyên tử H có 2 quả cầu màu xanh => Có 2 electron ở lớp ngoài cùng
+ Nguyên tử O có 8 quả cầu màu xanh => Có 8 electron ở lớp ngoài cùng