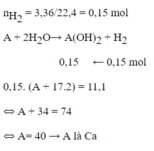Cho kim loại A hóa trị 2 tấc dụng với nước ở nhiệt độ thường . Biết rằng sau phản ứng thu được 3,36 lít thoát ra ở dktc và khối lượng của bazo có trong dung dịch là 11,1 gam . Tìm A

Những câu hỏi liên quan
Cho kim loại A, hóa trị II tác dụng với nước ở nhiệt độ thường. Biết rằng sau phản ứng thu được 3,36 l khí thoát ra ở đktc và khối lượng của bazơ có trong dung dịch thu được là 11,1 gam. Tìm A
A. Ba
B. Ca
C. Na
D. Cu
Cho kim loại A, hóa trị II tác dụng với nước ở nhiệt độ thường. Biết rằng sau phản ứng thu được 3,36 l khí thoát ra ở đktc và khối lượng của bazơ thu được là 11,1 gam. Tìm A
A. Ba
B. Ca
C. Na
D. Cu
giúp mk với
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(A+2H_2O\rightarrow A\left(OH\right)_2+H_2\)
\(................0.15.....0.15\)
\(M_{A\left(OH\right)_2}=\dfrac{11.1}{0.15}=74\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow A=40\)
\(\Rightarrow B\)
Đúng 2
Bình luận (0)
$A + 2H_2O \to A(OH)_2 + H_2$
n A(OH)2 = n H2 = 3,36/22,4 = 0,15(mol)
M A(OH)2 = A + 34 = 11,1/0,15 = 74
=> A = 40(Ca)
Vậy A là Canxi
Đáp án B
Đúng 1
Bình luận (0)
Cho kim loại A, hóa trị II tác dụng với nước ở nhiệt độ thường. Biết rằng sau phản ứng thu được 4,48 l khí thoát ra ở đktc và khối lượng của bazo thu được là 34,2 gam. Tìm kim loại A
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\); \(n_{A\left(OH\right)_2}=\dfrac{34,2}{M_A+34}\left(mol\right)\)
\(A+2H_2O\rightarrow A\left(OH\right)_2+H_2\)
\(\dfrac{34,2}{M_A+34}\) --> \(\dfrac{34,2}{M_A+34}\) ( mol )
\(\rightarrow n_{H_2}=\dfrac{34,2}{M_A+34}=0,2\left(mol\right)\)
\(\Leftrightarrow34,2=0,2M_A+6,8\)
\(\Leftrightarrow0,2M_A=27,4\)
\(\Leftrightarrow M_A=137\) ( g/mol )
--> A là Bari ( Ba )
Đúng 4
Bình luận (0)
\(A+H_2O\rightarrow A\left(OH\right)_2+H_2\\ n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ TheoPT:n_{H_2}=n_{A\left(OH\right)_2}=0,2\left(mol\right)\\ \Rightarrow M_{A\left(OH\right)_2}=A+17.2=\dfrac{34,2}{0,2}=171\\ \Rightarrow A=137\left(Ba\right)\)
Đúng 2
Bình luận (0)
Cho kim loại A, hóa trị II tác dụng với nước ở nhiệt độ thường. Biết rằng sau phản ứng thu được 4,48 l khí thoát ra ở đktc và khối lượng của bazơ có trong dung dịch thu được là 34,2 gam. Tìm A
`A + 2H_2 O -> A(OH)_2 + H_2`
`n_[H_2] = [ 4,48 ] / [22,4 ] = 0,2 (mol)`
`n_[A(OH)_2] = [ 34,2 ] / [ M_A + 34 ] (mol)`
Mà `n_[H_2] = n_[A(OH)_2]`
`=> [34,2] / [M_A + 34] = 0,2`
`<=>M_A = 137 ( g // mol)`
`-> A` là `Ba`
Đúng 2
Bình luận (0)
Cho 20 gam kim loại R có hóa trị II tác dụng hoàn toàn với nước ở nhiệt độ thường , sau phản ứng thu được dung dịch base và thấy có 11,2 lít khí hydrogen thoát ra ngoài .
a. Viết PTHH của phản ứng
b. Xác định kim loại R. Biết thể tích các khí đo ở đktc
\(a.R+2H_2O\rightarrow R\left(OH\right)_2+H_2\\
b.n_{H_2}=\dfrac{11,2}{22,4}=0,5mol\\
n_R=n_{H_2}=0,5mol\\
M_R=\dfrac{20}{0,5}=40g/mol\)
Vậy kim loại R là Ca
Đúng 2
Bình luận (0)
a)cho 9,75 gam kim loại x hóa trị 2 tác dụng với dung dịch HCl dư thu được dung dịch A có 3,36 lít khí thoát ra
b) nếu dùng 200 ml dung dịch HCl 2n cho phản ứng trên tính khối lượng muối và nồng độ các chất tan trong dung dịch A
\(a,PTHH:X+2HCl\to XCl_2+H_2\\ \Rightarrow n_{X}=n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ \Rightarrow M_X=\dfrac{9,75}{0,15}=65(g/mol)(Zn)\\ b,n_{HCl}=2.0,2=0,4(mol)\)
Vì \(\dfrac{n_{H_2}}{1}<\dfrac{n_{HCl}}{2}\) nên \(HCl\) dư
\(\Rightarrow n_{ZnCl_2}=n_{H_2}=0,15(mol)\\ \Rightarrow m_{ZnCl_2}=136.0,15=20,4(g)\\ C_{M_{ZnCl_2}}=\dfrac{0,15}{0,2}=0,75M\)
Đúng 2
Bình luận (1)
Cho 4,6 gam kim loại R có hóa trị I tác dụng hoàn toàn với nước ở nhiệt độ thường , sau phản ứng thu được 8 gam base và thấy có khí hydrogen thoát ra ngoài .
a. Viết PTHH của phản ứng
b. Xác định kim loại R
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, th...
Đọc tiếp
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
A. Al.
B. Na
C. Ca.
D. K.
Hỗn hợp rắn X gồm M, MO và MCl2 (M là kim loại có hóa trị II không đổi). Cho 18,7 gam X tác dụng với dung dịch HCl (vừa đủ), thu được dung dịch A và 6,72 lít khí (đktc). Cho dung dịch NaOH dư vào dung dịch A, sau phản ứng thu được kết tủa B. Nung B ở nhiệt độ cao đến khối lượng không đổi thu được 18,0 gam chất rắn. Mặt khác, khi cho 18,7 gam hỗn hợp X vào 500 ml dung dịch CuCl2 1,0M, sau phản ứng, tách bỏ chất rắn rồi cô cạn dung dịch, thu được 65,0 gam muối khan. Biết các phản ứng hóa học xảy r...
Đọc tiếp
Hỗn hợp rắn X gồm M, MO và MCl2 (M là kim loại có hóa trị II không đổi). Cho 18,7 gam X tác dụng với dung dịch HCl (vừa đủ), thu được dung dịch A và 6,72 lít khí (đktc). Cho dung dịch NaOH dư vào dung dịch A, sau phản ứng thu được kết tủa B. Nung B ở nhiệt độ cao đến khối lượng không đổi thu được 18,0 gam chất rắn. Mặt khác, khi cho 18,7 gam hỗn hợp X vào 500 ml dung dịch CuCl2 1,0M, sau phản ứng, tách bỏ chất rắn rồi cô cạn dung dịch, thu được 65,0 gam muối khan. Biết các phản ứng hóa học xảy ra hoàn toàn.
Xác định kim loại M và tính thành phần phần trăm theo khối lượng của các chất có trong hỗn hợp X.