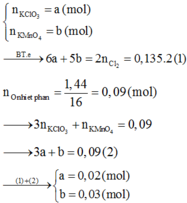Khỏi nung nóng hỗn hợp A gồm KMnO4 và KClO3 đến khi phản ứng hết thì khối lượng giảm 1/4 so với ban đầu. Xác định phần trăm theo khối lượng KClO3 trong hỗn hợp A

Những câu hỏi liên quan
nung nóng 49, 975 gam hỗn hợp y gồm KMnO4 và KClO3 đến khi khối lượng không đổi thì thấy khối lượng chất rắn giảm giảm 10,4 gam so với khối lượng hỗn hợp Y . Tính phần trăm khối lượng mỗi chất trong hỗn hợp Y
Gọi số mol KMnO4, KClO3 là a, b
=> 158a + 122,5b = 49,975
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
_______a----------------------------------->a
2KClO3 --to--> 2KCl + 3O2
_b---------------------->1,5b
mO2 = mgiảm = 10,4
=> \(n_{O_2}=\dfrac{10,4}{32}=0,325\left(mol\right)\)
=> 0,5a + 1,5b = 0,325
=> a = 0,2; b = 0,15
=> \(\left\{{}\begin{matrix}\%KMnO_4=\dfrac{0,2.158}{49,975}.100\%=63,23\%\\\%KClO_3=\dfrac{0,15.122,5}{49,975}.100\%=36,77\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Bài 1: Nung nóng 49,975 gam hỗn hợp Y gồm KMnO4 và KClO3 đến khi khối lượng không đổi thì thấy khối lượng chất rắn giảm 10,4 gam so với khối lượng hỗn hợp Y. Tính phần trăm khối lượng mỗi chất trong hỗn hợp Y.
giúp mình với
Gọi số mol KMnO4, KClO3 là a, b
=> 158a + 122,5b = 49,975
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
2KClO3 --to--> 2KCl + 3O2
mO2 = mgiảm = 10,4
=> \(n_{O_2}=\dfrac{10,4}{32}=0,325\left(mol\right)\)
=> 0,5a + 1,5b = 0,325
=> a = 0,2; b = 0,15
=> \(\left\{{}\begin{matrix}\%KMnO_4=\dfrac{0,2.158}{49,975}.100\%=63,23\%\\\%KClO_3=\dfrac{0,15.122,5}{49,975}.100\%=36,77\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
nung nóng 49, 975 gam hỗn hợp y gồm KMNO4 và KClO3 đến khi khối lượng không đổi thì thấy khối lượng chất rắn giảm giảm 4,0 gam . Tính phần trăm khối lượng mỗi chất trong hỗn hợp X
Gọi $n_{KMnO_4} = a(mol) ; n_{KClO_3} = b(mol) \Rightarrow 158a + 122,5b = 49,975(1)$
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
$2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2$
$m_{O_2} = m_{giảm} = 4(gam)$
$\Rightarrow n_{O_2} = 0,5a + 1,5b = \dfrac{4}{32} = 0,125(2)$
Từ (1)(2) suy ra a = 0,339 ; b = -0,029 < 0
(Sai đề)
Đúng 1
Bình luận (0)
Hỗn hợp X gồm a mol KClO3 và b mol Cu. Nung nóng hỗn hợp X đến khi các phản ứng xảy ra hoàn toàn thì thấy khối lượng hỗn hợp chất rắn Y thu được bằng khối lượng hỗn hợp X. Xác định mối liên hệ của a và b.
Do khối lượng chất rắn trong X và Y bằng nhau
=> Lượng O2 sinh ra khi phân hủy KClO3 phản ứng hết với Cu
PTHH: 2KClO3 --to--> 2KCl + 3O2
a--------------->1,5a
2Cu + O2 --to--> 2CuO
3a<--1,5a
=> b \(\ge\) 3a
Đúng 7
Bình luận (0)
1/Nung hỗn hợp gồm KMnO4 và KClO3 ở nhiệt độ cao đến khối lương không đổi thu được hỗn hợp chất rắn mới có khối lượng bằng 75% khối lượng hỗn hợp ban đầu tính tỉ lệ khối lượng KMnO4 và KClO3 cần lấy và thành phần % theo khối lượng mỗi muối trong hỗn hợp ban đầu
giả sử có 100g KMnO4, KClO3
⇒m chất rắn =75g
2KMnO4\(\underrightarrow{^{to}}\)K2MnO4+MnO2+O2
x___________x/2_____ x /2__ x/2 (mol)
2KClO3→2KCl+3O2
y _________y___3y/2
\(\left\{{}\begin{matrix}\text{158x+122.5y=100}\\\text{142x+74.5y=75 }\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}\text{x=0.3}\\\text{y=0.4 }\end{matrix}\right.\)
⇒mKMnO4⇒%
⇒mKClO3⇒%
Nung một hỗn hợp A gồm kalipemanganat và kaliclorat (có xúc tác) , đến khi phản ứng xong thấy khối lượng giảm mất 1/4 so với ban đầu . Xác định phần trăm theo khối lượng của kaliclorat trong hỗn hợp A?
Nung 43,3 gam hỗn hợp gồm KMnO4 và KClO3. Sau một thời gian thu được khí X và chất rắn Y. Nguyên tố Mn chiếm 24,103% khối lượng chất rắn Y. Tính khối lượng của KMnO4 và KClO3 trong hỗn hợp ban đầu. Biết hiệu suất các phản ứng đều đạt 90%.
Gọi n KMnO4 = a
n KClO3 = b ( mol )
--> 158a + 122,5 b = 43,3
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
0,9b 1,35b
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,9a 0,45a
\(\%Mn=\dfrac{55a}{43,3-32\left(0,45a+1,35b\right)}=24,103\%\)
\(\rightarrow a=0,15\)
\(b=0,16\)
\(m_{KMnO_4}=0,15.158=23,7\left(g\right)\)
\(m_{KClO_3}=0,16.122,5=19,6\left(g\right)\)
Đúng 3
Bình luận (0)
Thêm 3,0 gam MnO2 vào 200gam hỗn hợp X gồm KCl và KClO3, trộn kĩ hỗn hợp thu được và đun nóng đến phản ứng xảy ra hoàn toàn (khối lượng hỗn hợp không đổi) thu được chất rắn Y cân nặng 145,4gam. Xác định thành phần phần trăm theo khối lượng của các muối trong hỗn hợp X
mgiảm = mO2 (sinh ra) = 200 + 3 - 145,4 = 57,6 (g)
\(\rightarrow n_{O_2}=\dfrac{57,6}{32}=1,8\left(mol\right)\)
PTHH: 2KClO3 --to, MnO2--> 2KCl + 3O2
1,2 1,8
\(\rightarrow m_{KClO_3}=1,2.122,5=147\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{147}{200}=73,5\%\\\%m_{KCl}=100\%-73,5\%=26,5\%\end{matrix}\right.\)
Đúng 6
Bình luận (0)
Khối lượng oxi thoát ra: 197 + 3 – 152 = 48(g)
Số mol O2=4832=1,5(mol)O2=4832=1,5(mol)
Phương trình hóa học của phản ứng :
2KClO3MnO2,to⟶2KCl+3O22KClO3⟶MnO2,to2KCl+3O2
2 mol 3 mol
1,5×23=1mol1,5×23=1mol ←← 1,5 mol
Khối lượng KClO3KClO3 trong hỗn hợp : 1 x 122,5 =122,5 (g)Khối lượng KCl trong hỗn hợp ban đầu: 197 – 122,5 = 74,5(g)→%mKClO3=62,18%;%mKCl=37,82%→%mKClO3=62,18%;%mKCl=37,82%
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 đến khối lượng không đổi thu được (m – 1,44) gam chất rắn. Mặt khác cho m gam hỗn hợp X tác dụng với một lượng dư dung dịch HCl đặc, đun nóng đến khi phản ứng xảy ra hoàn toàn thu được 3,024 lít Cl2 (đktc). Tỷ lệ mol giữa KClO3 và KMnO4 có trong hỗn hợp X là A. 3:2 B. 2:3 C. 1:2 D. 2:1
Đọc tiếp
Nung m gam hỗn hợp X gồm KClO3 và KMnO4 đến khối lượng không đổi thu được (m – 1,44) gam chất rắn. Mặt khác cho m gam hỗn hợp X tác dụng với một lượng dư dung dịch HCl đặc, đun nóng đến khi phản ứng xảy ra hoàn toàn thu được 3,024 lít Cl2 (đktc). Tỷ lệ mol giữa KClO3 và KMnO4 có trong hỗn hợp X là
A. 3:2
B. 2:3
C. 1:2
D. 2:1