Đốt cháy 4,48 lít hỗn hợp gồm etan,butan. Cho toàn bộ sản phẩm cháy vào bình nước vôi trong dư thu được 56g chất kết tủa .
a)% theo thể tích, theo khối lượng mỗi chất trong hỗn hợp đầu
b)thể tích không khí cần dùng
Hỗn hợp A gồm CH4 và C2H4. Đốt cháy hoàn toàn 5,6 lít hỗn hợp A (đktc) rồi cho toàn bộ sản phẩm cháy vào bình nước vôi trong dư thu được 40 gam kết tủa. Tính % khối lượng mỗi chất trong A ?
Hỗn hợp A gồm phenol , ancol etylic phản ứng với Kali thì thu đc 2,464 lít khí . Nếu đốt cháy cùng lượng A trên, cho toàn bộ sản phẩm cháy vào bình chứa nước vôi trong dư thu đc 84g chất kết tủa
a) % theo khối lượng mỗi chất trong hỗn hợp A
b)Nếu cho \(\dfrac{3}{4}\)lượng A trên vào bình chứa dung dịch brom(vừa đủ), tính khối lượng kết tủa thu đc
a, BTNT H, có: \(n_{C_6H_5OH}+n_{C_2H_5OH}=2n_{H_2}=2.\dfrac{2,464}{22,4}=0,22\left(mol\right)\left(1\right)\)
BTNT C, có: \(6n_{C_6H_5OH}+2n_{C_2H_5OH}=n_{CO_2}=n_{CaCO_3}=\dfrac{84}{100}=0,84\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{C_6H_5OH}=0,1\left(mol\right)\\n_{C_2H_5OH}=0,12\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{C_6H_5OH}=\dfrac{0,1.94}{0,1.94+0,12.46}.100\%\approx63\%\\\%m_{C_2H_5OH}\approx37\%\end{matrix}\right.\)
b, 3/4 lượng A có nC6H5OH = 3/4.0,1 = 0,075 (mol)
PT: \(C_6H_5OH+3Br_2\rightarrow C_6H_2Br_3OH_{\downarrow}+3HBr\)
Theo PT: \(n_{C_6H_2Br_3OH}=n_{C_6H_5OH}=0,075\left(mol\right)\)
\(\Rightarrow m_{\downarrow}=0,075.331=24,825\left(g\right)\)
Đốt cháy hoàn toàn 8,96 lít (đktc) hỗn hợp C2H4, C2H6, C3H6, C4H8 rồi cho toàn bộ sản phẩm cháy vào dung dịch nước vôi trong dư, thu được 110 gam kết tủa và khối lượng dung dịch giảm 40 gam. Phần trăm thể tích của C2H6 trong hỗn hợp là
A. 37,5%
B. 75%
C. 25%
D. 50%
Đốt cháy hoàn toàn 1,68 lít (ở đktc) hỗn hợp gồm methane và acetylene rồi hấp thụ toàn bộ sản phẩm vào dung dịch nước vôi trong dư, thấy thu được 10 gam kết tủa. Tính thể tích của mỗi khí có trong hỗn hợp ban đầu
Ta có: \(n_{CH_4}+n_{C_2H_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\left(1\right)\)
PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=n_{CH_4}+2n_{C_2H_2}=\dfrac{10}{100}=0,1\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CH_4}=0,05\left(mol\right)\\n_{C_2H_2}=0,025\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}V_{CH_4}=0,05.22,4=1,12\left(l\right)\\V_{C_2H_2}=0,025.22,4=0,56\left(l\right)\end{matrix}\right.\)
Đốt cháy hoàn toàn một hỗn hợp gồm C 2 H 2 và C 2 H 4 có thể tích 6,72 lít (đktc) rồi cho toàn bộ sản phẩm thu được hấp thụ hết vào dung dịch Ca OH 2 dư. Sau khi phản ứng kết thúc, thấy khối lượng bình đựng Ca OH 2 tăng thêm 33,6 gam đồng thời có m gam kết tủa. Xác định thành phần % thể tích của mỗi chất trong hỗn hợp và tính m.
Gọi số mol C 2 H 2 và C 2 H 4 trong hỗn hợp là x, y.
Ta có x + y = 6,72/22,4 = 0,3 mol
2 C 2 H 2 + 5 O 2 → 4C O 2 + 2 H 2 O
C 2 H 4 + 3 O 2 → 2C O 2 + 2 H 2 O
Theo phương trình hoá học của phản ứng cháy, ta có :
n CO 2 = 2x + 2y => m CO 2 = 44(2x + 2y)
n H 2 O = x + 2y → m H 2 O = 18 (x + 2y)
Theo đề bài, khối lượng bình Ca OH 2 tăng lên chính là khối lượng của C O 2 và H 2 O . Vậy :
m CO 2 + m H 2 O = 44(2x + y) + 18 (x + 2y) = 33,6g
Ta có các phương trình : x + y = 0,3
106x + 124y = 33,6
Giải ra ta được : x = 0,2 ; y = 0,1.
% V C 2 H 2 = 0,2x22,4/6,72 x 100% = 66,67%
% V C 2 H 4 = 33,33%
n CO 2 = 2(x+y) = 0,6 mol = n CaCO 3
m CaCO 3 = 0,6 x 100 = 60g
Hỗn hợp X gồm C 3 H 4 , C 3 H 6 , C 3 H 8 có tỉ khối so với H 2 là 21. Đốt cháy hoàn toàn 1,12 lít hỗn hợp X (đktc), rồi hấp thụ toàn bộ sản phẩm cháy vào bình đựng nước vôi trong dư, lọc bỏ kết tủa, khối lượng dung dịch thu được so với khối lượng nước vôi trong ban đầu
A. giảm 5,7 gam
B. giảm 15 gam.
C. tăng 9,3 gam
D. giảm 11,4 gam
Chọn A
Đề cho hỗn hợp X gồm 3 chất, nhưng chỉ có 2 giả thiết liên quan đến các chất đó nên quy đổi hỗn hợp X thành hỗn hợp gồm C 3 H 6 , C 3 H 8
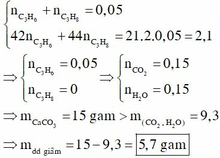
Một hỗn hợp X gồm etan, propen và butađien. Tỷ khối của hỗn hợp X đối với H 2 là 20. Đốt cháy hoàn toàn 0,15 mol hỗn hợp X sau đó cho toàn bộ sản phẩm cháy vào dung dịch vôi trong dư. Tính khối lượng kết tủa thu được?
A. 45,0 gam
B. 37,5 gam
C. 40,5 gam
D. 42,5 gam
Một hỗn hợp X gồm etan, propen và butađien. Tỷ khối của hỗn hợp X đối với H2 là 20. Đốt cháy hoàn toàn 0,15 mol hỗn hợp X sau đó cho toàn bộ sản phẩm cháy vào dung dịch vôi trong dư. Tính khối lượng kết tủa thu được?
A. 45,0 gam
B. 37,5 gam
C. 40,5 gam
D. 42,5 gam
X gồm C2H6 ; C3H6 ; C4H6.
⇒ Gọi công thức chung của X là CnH6
MX = 20.2 = 40
⇒ 12n + 6 = 40 ⇒ n =17/6
⇒ nCO2 = nC/X = 0,15 . 17/6 =0,425
⇒ mCaCO3 = 0,425 . 100 = 42,5g
Đáp án D.
Bài 4: Đốt cháy hỗn hợp X gồm Metan và Etilen có thể tích 8,96 lít (đktc) rồi cho sản phẩm thu được hấp thụ hết vào dung dịch nước vôi trong dư. Thấy khối lượng bình tăng 45,2 gam đồng thời có m gam kết tủa. Tính % thể tích hỗn hợp X và m ?
\(\left\{{}\begin{matrix}CH_4:x\left(mol\right)\\C_2H_4:y\left(mol\right)\end{matrix}\right.\)⇒ x + y = \(\dfrac{8,96}{22,4} = 0,4\)(1)
\(m_{CO_2} + m_{H_2O} = m_{bình\ tăng} = 45,2(gam)\)
Bảo toàn nguyên tố với C:\(n_{CO_2} = x + 2y(mol)\)
Bảo toàn nguyên tố với H:\(n_{H_2O} = 2x + 2y (mol)\)
Suy ra :(x + 2y).44 + (2x+2y).18 = 45,2(2)
Từ (1)(2) suy ra: x = 0,1 ; y = 0,3
Vậy :
\(\%V_{CH_4} = \dfrac{0,1}{0,4}.100\% = 25\%\\ \%V_{C_2H_4} = 100\% - 25\% = 75\%\\ CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CaCO_3} = n_{CO_2} = 0,1 + 0,3.2 = 0,7(mol)\\ \Rightarrow m = 0,7.100 = 70(gam)\)