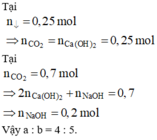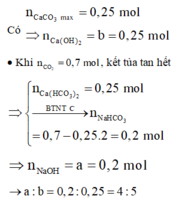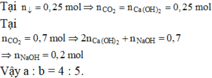Những câu hỏi liên quan
Hãy viết phương trình hóa học của CO2 với dung dịch NaOH, dung dịch Ca(OH)2 trong trường hợp:
a. Tỉ lệ số mol n : n = 1 : 1
b. Tỉ lệ số mol n : n = 1 : 2
\(CO_2+NaOH\rightarrow NaHCO_3\\ CO_2+Ca\left(OH\right)_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
Đúng 0
Bình luận (0)
Sục khí CO2 vào dung dịch NaOH. Hãy viết phương trình phản ứng và nêu ra tỉ lệ số mol tạo thành
a. muối axit
b. Muối trung hòa
c. muối axit vầ muối trung hòa
d. Nếu cho khí CO2 vào dung dịch nước vôi trong với tỉ lệ :
+ n(co2) : n (Ca(OH)2) =1:1 tạo thành muối gì ?
+ n(co2) : n (Ca(OH)2) = 2:1 tạo thành muối gì?
a, \(NaOH+CO_2\rightarrow NaHCO_3\)
Tỉ lệ mol nNaOH: nCO2= 1:1
b, \(2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\)
Tỉ lệ mol nNaOH: nCO2= 2:1
c, Khi tỉ lệ mol \(T=\frac{n_{NaOH}}{n_{CO2}}\) có 1 < T < 2 thì tạo 2 muối
d, Khi sục CO2 vào Ca(OH)2:
- Tỉ lệ mol nCO2: nCa(OH)2= 1:1 tạo muối CaCO3
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
- Tỉ lệ mol nCO2: nCa(OH)2= 2:1 tạo muối Ca(HCO3)2
\(Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\)
Lập các phương trình hóa học ở dạng phân tử và dạng ion rút gọn của phản ứng giữa các chất sau đây trong dung dịch: (1) K3PO4 và Ba(NO3)2 (2) Na3PO4 và CaCl2 (3) Ca(H2PO4)2 và Ca(OH)2 với tỉ lệ mol 1:1 (4) (NH4)3PO4 + Ba(OH)2
Đọc tiếp
Lập các phương trình hóa học ở dạng phân tử và dạng ion rút gọn của phản ứng giữa các chất sau đây trong dung dịch:
(1) K3PO4 và Ba(NO3)2
(2) Na3PO4 và CaCl2
(3) Ca(H2PO4)2 và Ca(OH)2 với tỉ lệ mol 1:1
(4) (NH4)3PO4 + Ba(OH)2
(1) 2K3PO4 + 3Ba(NO3)2 → Ba3(PO4)2 ↓ + 6KNO3
Ba2+ + 2PO43- → Ba3(PO4)2 ↓
(2) 2Na3PO4 + 3CaCl2 → Ca3(PO4)2 ↓ + 6NaCl
Ca2+ + 2PO43- → Ca3(PO4)2 ↓
(3) Ca(H2PO4)2 + Ca(OH)2 → 2CaHPO4 + 2H2O
H2PO4- + OH- → HPO42- + H2O
(4) 2(NH4)3PO4 + 3Ba(OH)2 → Ba3(PO4)2 ↓ + 6NH3 ↑ + 6H2O
6NH4+ + 2PO43- + 3Ba2+ + 6OH- → Ba3(PO4)2 ↓ + 6NH3 ↑ + 6H2O
Đúng 0
Bình luận (0)
Sụ từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2 Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau: Tỉ lệ a:b tương ứng là A. 4 : 3. B. 2 : 3. C. 4 : 5. D. 5 : 4
Đọc tiếp
Sụ từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2 Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau:
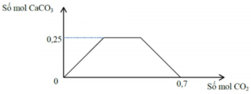
Tỉ lệ a:b tương ứng là
A. 4 : 3.
B. 2 : 3.
C. 4 : 5.
D. 5 : 4
Sục từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2. Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau: Tỉ lệ a : b tương ứng là A. 4 : 5. B. 2 : 3. C. 5 : 4. D. 4 : 3.
Đọc tiếp
Sục từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2. Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau: Tỉ lệ a : b tương ứng là
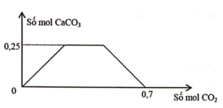
A. 4 : 5.
B. 2 : 3.
C. 5 : 4.
D. 4 : 3.
Sục từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2 Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau Tỉ lệ a:b tương ứng là A. 4 : 3. B. 2 : 3. C. 4 : 5. D. 5 : 4.
Đọc tiếp
Sục từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2 Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau
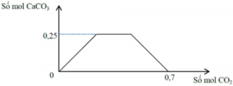
Tỉ lệ a:b tương ứng là
A. 4 : 3.
B. 2 : 3.
C. 4 : 5.
D. 5 : 4.
Sục từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2. Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau: Tỉ lệ a : b tương ứng là A. 4 : 5 B. 2 : 3 C. 5 : 4 D. 4 : 3
Đọc tiếp
Sục từ từ khí CO2 đến dư vào dung dịch gồm a mol NaOH và b mol Ca(OH)2. Sự phụ thuộc của số mol kết tủa CaCO3 vào số mol CO2 được biểu diễn theo đồ thị sau:
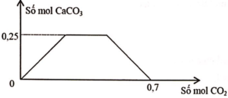
Tỉ lệ a : b tương ứng là
A. 4 : 5
B. 2 : 3
C. 5 : 4
D. 4 : 3
Chọn đáp án A.
Có n C a C O 3 m a x = 0 , 25 m o l
⇒ n C a O H 2 = b = 0 , 25 m o l
· Khi n C O 2 = 0 , 7 m o l , kết tủa tan hết
⇒ n C a H C O 3 2 = 0 , 25 m o l → B T N T C n N a H C O 3 = 0 , 2 m o l
⇒ n N a O H = a = 0 , 2 m o l
![]()
Đúng 0
Bình luận (0)
1. Hòa tan m gam Na và 250 ml dung dịch NaOH 10% D=1,2g/mol thu được dung dịch NaOH 14,94%. Tính m?
2. Trong một dung dịch muối magie dihidrophotphat tỉ lệ số mol nguyên tử O: số mol nguyên tử H là 1,25. Tính C% của dung dịch muối nói trên.
1) m dd naOH (bđ) = \(250.1,2=300\left(g\right)\)
\(m_{NaOH\left(bđ\right)}=\frac{300.10}{200}=30\left(g\right)\)
\(n_{Na}=\frac{m}{23}\left(mol\right)\)
PTHH: \(2Na+2H_2O\rightarrow2NaOH+H_2\uparrow\)
_______ \(\frac{m}{23}\) -------------------> \(\frac{m}{23}\)-------> \(\frac{m}{46}\)(mol)
\(=>m_{NaOH}=\frac{m}{23}.40=\frac{40m}{23}\left(g\right)\)
=> \(m_{dd}\) sau pư = \(m+300-2.\frac{m}{46}\) = \(\frac{22m}{23}+300\left(g\right)\)
=> \(C\%=\frac{\frac{40m}{23}}{\frac{22m}{23}+300}.100\%=14,94\%\)
=> m = 28,1 (g)
Đúng 0
Bình luận (0)
Cho các khẳng định sau: (1) Hỗn hợp Ag và Fe3O4 (tỉ lệ mol 1:1) có thể tan trong dung dịch HCl dư. (2) Nhỏ dung dịch H2SO4 loãng vào dung dịch K2CrO4 thì màu vàng của dung dịch chuyển dần sang màu cam. (3) Cr(OH)3 và Cr2O3 đều là các chất lưỡng tính, tan hoàn toàn trong dung dịch NaOH loãng. (4) Fe và Cr tác dụng với HCl trong dung dịch với cùng tỉ lệ mol. (5) Không tồn tại dung dịch chứa đồng thời AgNO3 và Fe(NO3)2. (6) Tính chất hóa học đặc trưng của hợp chất sắt (III) là tính khử. Số phát biể...
Đọc tiếp
Cho các khẳng định sau:
(1) Hỗn hợp Ag và Fe3O4 (tỉ lệ mol 1:1) có thể tan trong dung dịch HCl dư.
(2) Nhỏ dung dịch H2SO4 loãng vào dung dịch K2CrO4 thì màu vàng của dung dịch chuyển dần sang màu cam.
(3) Cr(OH)3 và Cr2O3 đều là các chất lưỡng tính, tan hoàn toàn trong dung dịch NaOH loãng.
(4) Fe và Cr tác dụng với HCl trong dung dịch với cùng tỉ lệ mol.
(5) Không tồn tại dung dịch chứa đồng thời AgNO3 và Fe(NO3)2.
(6) Tính chất hóa học đặc trưng của hợp chất sắt (III) là tính khử.
Số phát biểu đúng là
A. 3.
B. 5
C. 2.
D. 4