Dẫn 11,2 lít khí hiđrô (ở điều kiện tiêu chuẩn) từ từ qua 60 g đồng (II) oxit nung nóng.
a/ Chất nào còn dư sau phản ứng?
b/ Tính khối lượng chất dư sau phản ứng?
Đốt cháy 11,2 gam sắt trong 12,8 gam oxi sau phản ứng thu được sản phẩm là oxit sắt từ Fe3O4 Sau phản ứng chất nào còn dư và dư bao nhiêu mol? Tính khối lượng sản phẩm thu được Tính V không khí cần dùng ở điều kiện tiêu chuẩn? Biết O2 chiếm 1/5 thể tích không khí
PTHH: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
Ta có: \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\n_{O_2}=\dfrac{12,8}{32}=0,4\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{3}< \dfrac{0,4}{2}\) \(\Rightarrow\) Oxi còn dư, Fe p/ứ hết
\(\Rightarrow n_{O_2\left(dư\right)}=0,4-\dfrac{2}{15}=\dfrac{4}{15}\left(mol\right)\)
+) Theo PTHH: \(\left\{{}\begin{matrix}n_{O_2}=\dfrac{2}{15}\left(mol\right)\\n_{Fe_3O_4}=\dfrac{1}{15}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{kk}=\dfrac{2}{15}\cdot22,4\cdot5\approx14,93\left(l\right)\\m_{Fe_3O_4}=\dfrac{1}{15}\cdot232\approx15,47\left(g\right)\end{matrix}\right.\)
Cho 6,72(lít) khí H2 phản ứng với 8,96(lít) khí O2(các thể tích khí đo ở điều kiện tiêu chuẩn)
a) Sau phản ứng chất nào hết, chất nào dư, tính khối lượng chất dư?
b) Tính số phân tử H2O tạo ra sau phản ứng
c) Khối lượng O2 tham gia vào phản ứng trên được điều chế từ KMnO4 hãy tính khối lượng KMnO4 cần dùng
\(a,n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
bđ 0,3 0,4
pư 0,3 0,15
sau pư 0 0,25 0,3
=> H2 hết, O2 dư
\(m_{O_2\left(dư\right)}=0,25.32=8\left(g\right)\)
b) \(A_{H_2O}=0,3.6.10^{23}=1,8.10^{23}\left(phân.tử\right)\)
c) \(m_{O_2\left(pư\right)}=0,15.32=4,8\left(g\right)\)
PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,3<-------------------------------------0,15
\(\rightarrow m_{KMnO_4}=0,3.158=47,4\left(g\right)\)
Khử 8,68 gam thủy ngân (II) oxit bằng 0,56 lít khí hiđrô ở nhiệt độ
cao.
a/ Chất nào còn dư sau phản ứng và dư bao nhiêu?
b/ Tính khối lượng kim loại thu được sau phản ứng?
HgO+H2-to>Hg+H2O
0,025-0,025--0,025
n HgO=\(\dfrac{8,68}{217}\)=0,04 mol
n H2=\(\dfrac{0,56}{22,4}\)=0,025 mol
=>HgO dư
=>m Hg=0,025.201=5,025g
nH2 = 0,56/22,4 = 0,025 (mol)
nHgO = 8,68/217 = 0,04 (mol)
PTHH: HgO + H2 -> (t°) Hg + H2O
LTL: 0,025 < 0,04 => H2 dư
nH2 (p/ư) = nHg = 0,025 (mol)
VH2 = (0,04 - 0,025) . 22,4 = 0,336 (l)
mHg = 0,025 . 201 = 5,025 (g)
Câu 4. Đốt cháy 6,2 gam photpho trong bình chứa 7,84 lít khí oxi ở điều kiện tiêu chuẩn
a/ Chất nào còn dư sau phản ứng và dư bao nhiêu gam?
b/ Tính khối lượng sản phẩm tạo thành sau phản ứng.
nP=\(\dfrac{62}{31}\)=0,2(mol)
nO2=\(\dfrac{7,84}{22,4}\)=0,35(mol)
PTHH:4P+5O2to→2P2O5
tpứ: 0,2 0,35
pứ: 0,2 0,25 0,1
spứ: 0 0,1 0,1
a)chất còn dư là oxi
mO2dư=0,1.32=3,2(g)
b)mP2O5=n.M=0,1.142=14,2(g)
\(a.n_P=0,2\left(mol\right);n_{O_2}=0,35\left(mol\right)\\ 4P+5O_2-^{t^o}\rightarrow2P_2O_5\\ LTL:\dfrac{0,2}{4}< \dfrac{0,35}{5}\\ \Rightarrow SauphảnứngO_2dư\\ n_{O_2\left(pứ\right)}=\dfrac{5}{4}n_P=0,25\left(mol\right)\\ \Rightarrow m_{P\left(dư\right)}=\left(0,35-0,25\right).32=3,2\left(g\right)\\ b.n_{P_2O_5}=\dfrac{1}{2}n_P=0,1\left(mol\right)\\ \Rightarrow m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
a) n\(_P\) = \(\dfrac{6,2}{31}\) = 0,2(mol); n\(_{O_2}\) = \(\dfrac{7,84}{22,4}\) = 0,35(mol).
Theo phương trình hóa học:
\(4P+5O_2\) \(\underrightarrow{t^o}\) \(2P_2O_5\)
4 5 2 (mol)
0,2 \(\rightarrow\)0,25 \(\rightarrow\) 0,1(mol)
Tỉ lệ số mol: \(\dfrac{0,2}{4}< \dfrac{0,35}{5}\) \(\Rightarrow\) \(O_2\) phản ứng dư, P phản ứng hết.
\(n_{O_2}\)dư = 0,35 - \(\dfrac{0,2.5}{4}\) = 0,1(mol) \(\Rightarrow\) \(m_{O_2}\)dư = 0,1.32 = 3,2g
b) \(n_{P_2O_5}\) = 0,1.142 = 14,2g
Theo gt ta có: $n_{CO}=0,1(mol)$
Bảo toàn nguyên tố C và theo tỉ khối ta có:
$n_{CO}=0,025(mol);n_{CO_2}=0,075(mol)$
Ta lại có: $n_{O/oxit}=n_{CO_2}=0,075(mol)$
Gọi CTTQ của oxit sắt đó là $Fe_xO_y$
Ta có: $M_{Fe_xO_y}=\frac{160y}{3}$
Do đó công thức của oxit sắt là $Fe_3O_4$
cho 2,5 gam nhôm vào bình chứa 0,5 mol dung dịch axit sunfuric loãng
a,Viết phương trình phản ứng
b,chất nào còn dư sau phản ứng Tính khối lượng chất dư
c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
\(n_{Al}=\dfrac{2,5}{27}=\dfrac{25}{270}=\dfrac{5}{54}\left(mol\right)\\ n_{H_2SO_4}=0,5\left(mol\right)\\ a,2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ b,Vì:\dfrac{\dfrac{5}{54}}{2}< \dfrac{0,5}{4}\Rightarrow H_2SO_4dư\\ b,n_{H_2SO_4\left(dư\right)}=0,5-\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{13}{36}\left(mol\right)\\ \Rightarrow m_{H_2SO_4}=\dfrac{13}{36}.98=\dfrac{637}{18}\left(g\right)\\ c,n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.\dfrac{5}{54}=\dfrac{5}{36}\left(mol\right)\\ \Rightarrow V_{H_2\left(đktc\right)}=\dfrac{5}{36}.22,4=\dfrac{28}{9}\left(l\right)\)
Tóm tắt:
mAl= 2,5(g)
\(n_{H_2SO_4}=0,5\left(mol\right)\)
---
a) PTHH?
b) Chất dư? m?
c) Thể tích khí sau phản ứng?
Anh ít tóm tắt lắm nên không biết tóm tắt như ri ổn không, vì em cần nên anh tóm tắt ra thử
cho 2,5 gam nhôm vào bình chứa 0,25 mol dung dịch axit sunfuric loãng a,Viết phương trình phản ứng b,chất nào còn dư sau phản ứng Tính khối lượng chất dư c,Tính thể tích khí thoát ra ở điều kiện tiêu chuẩn
a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{Al}=\dfrac{2.5}{27}< \dfrac{1}{4}\)
=>H2SO4 dư, Al đủ
\(m_{H_2SO_4}=0.25\cdot98=24.5\left(g\right)\)
c: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{2.5}{54}=\dfrac{5}{108}\left(mol\right)\)
\(\Leftrightarrow n_{H_2}=\dfrac{5}{36}\left(mol\right)\)
\(V_{H_2}=\dfrac{5}{36}\cdot22.4=\dfrac{28}{9}\left(lít\right)\)
Mình thấy bạn Thịnh tính lượng dư sai
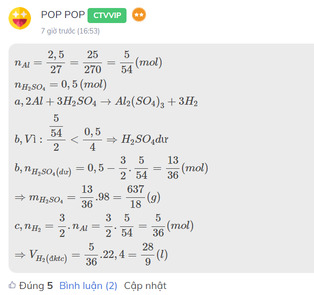
Đây là bài mình từng làm, bạn tham khảo nhé!
a) nKMnO4=0,01(mol)
PTHH: 2 KMnO4 -to-> K2MnO4 + MnO2 + O2
0,01______________0,005_____0,005___0,005(mol)
V(O2,đktc)=0,005.22,4=0,112(l)
b) PTHH: 2 Cu + O2 -to-> 2 CuO
nCu=0,1(mol); nO2=0,005(mol)
Ta có: 0,1/2 > 0,005/1
=> Cu dư, O2 hết, tính theo nO2.
nCu(p.ứ)=2.0,005=0,01(mol)
=> nCu(dư)=0,1-0,01=0,09(mol)
=>mCu(dư)=0,09.64=5,76(g)
cho 11,2 g sắt tác dụng với axit clohidric (HCl) thu duco759 sắt (II) clorua (FeCl2)
a) viết PTHH?
B) tính thể tích khí H2 sinh ra ở điều kiện tiêu chuẩn ?
c) nếu cho toàn bộ lượng khí hidro sinh ra trên phản ứng với 32g khí oxi để thu được nước thì chất khí nào còn dư sau phản ứng và dư bao nhiêu gam?