
Những câu hỏi liên quan
Cho các nhận định sau: 1) Cấu hình electron của ion X2+ là:
1
s
2
2
s
2
2
p
6
3
s
2
3
p
6
3
d
6
. Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố X thuộc chu kì 4 nhóm VIIIB. 2) Các ion và nguyên tử Ne, Na+, F-có điểm chung là có cùng số electron ....
Đọc tiếp
Cho các nhận định sau:
1) Cấu hình electron của ion X2+ là: 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6 3 d 6 .
Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố X thuộc chu kì 4 nhóm VIIIB.
2) Các ion và nguyên tử Ne, Na+, F-có điểm chung là có cùng số electron .
3) Khi đốt cháy ancol no thì ta có n H2O > n CO2
4) Dãy gồm các nguyên tố được sắp xếp theo chiều giảm dần bán kính nguyên tử từ trái sang phải K, Mg, Si, N
5) Tính bazơ của dãy hidroxit: NaOH, Mg(OH)2, Al(OH)3 giảm dần
Số nhận định đúng là
A. 3
B. 5
C. 4
D. 2
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp (
Z
X
Z
Y
) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.Xác định các nguyên tố X và Y.
Đọc tiếp
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp ( Z X < Z Y ) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).
- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.
- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.
Xác định các nguyên tố X và Y.
X tạo bởi chất ion với clo có công thức là XC1, vậy X là kim loại có hoá trị I.
Y cùng số nhóm với X vậy cũng có hoá trị I, công thức clorua của nó là YC1.
Ta có:
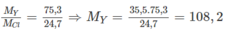
( M Y và M Cl lần lượt là NTK của nguyên tố Y và nguyên tố clo). Đó là Ag. Nguyên tố X cùng chu kì, cùng số thứ tự nhóm với Ag là kali (K))
Đúng 0
Bình luận (0)
Cho các phát biểu sau: (1) Các nguyên tố nhóm A trong bảng tuần hoàn là các nguyên tố nhóm s (2) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một chu kì được lặp đi lặp lại sau mỗi chu kì (3) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong một nhóm A biến đổi một cách không tuần hoàn (4) Số thứ tự của nhóm (IA,IIA,..) cho biết số electron ở lớp ngoài cùng nhưng không cho biết số electron hóa trị trong nguyên tử của các nguyên tố đó (5) Nhóm VIIIA là...
Đọc tiếp
Cho các phát biểu sau:
(1) Các nguyên tố nhóm A trong bảng tuần hoàn là các nguyên tố nhóm s
(2) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một chu kì được lặp đi lặp lại sau mỗi chu kì
(3) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong một nhóm A biến đổi một cách không tuần hoàn
(4) Số thứ tự của nhóm (IA,IIA,..) cho biết số electron ở lớp ngoài cùng nhưng không cho biết số electron hóa trị trong nguyên tử của các nguyên tố đó
(5) Nhóm VIIIA là nhóm khí hiếm
(6) Nguyên tử của tất cả các nguyên tố trong nhóm khí hiếm đều có 8 electron ở lớp ngoài cùng
Số phát biểu đúng là:
A. 5
B. 2
C. 3
D. 4
Cho các phát biểu sau: (1) Các nguyên tố nhóm A trong bảng tuần hoàn là các nguyên tố nhóm s (2) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một chu kì được lặp đi lặp lại sau mỗi chu kì (3) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong một nhóm A biến đổi một cách không tuần hoàn (4) Số thứ tự của nhóm (IA, IIA,..) cho biết số electron ở lớp ngoài cùng nhưng không cho biết số electron hóa trị trong nguyên tử của các nguyên tố đó (5) Nhóm VIIIA là...
Đọc tiếp
Cho các phát biểu sau:
(1) Các nguyên tố nhóm A trong bảng tuần hoàn là các nguyên tố nhóm s
(2) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một chu kì được lặp đi lặp lại sau mỗi chu kì
(3) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong một nhóm A biến đổi một cách không tuần hoàn
(4) Số thứ tự của nhóm (IA, IIA,..) cho biết số electron ở lớp ngoài cùng nhưng không cho biết số electron hóa trị trong nguyên tử của các nguyên tố đó
(5) Nhóm VIIIA là nhóm khí hiếm
(6) Nguyên tử của tất cả các nguyên tố trong nhóm khí hiếm đều có 8 electron ở lớp ngoài cùng
Số phát biểu đúng là
A.5.
B. 2.
C. 3.
D. 4.
Cho các phát biểu sau:(1) Các nguyên tố nhóm A trong bảng tuần hoàn là các nguyên tố nhóm s(2) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một chu kì được lặp đi lặp lại sau mỗi chu kì(3) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong một nhóm A biến đổi một cách không tuần hoàn(4) Số thứ tự của nhóm (IA,IIA,..) cho biết số electron ở lớp ngoài cùng nhưng không cho biết số electron hóa trị trong nguyên tử của các nguyên tố đó(5) Nhóm VIIIA là nhóm...
Đọc tiếp
Cho các phát biểu sau:
(1) Các nguyên tố nhóm A trong bảng tuần hoàn là các nguyên tố nhóm s
(2) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một chu kì được lặp đi lặp lại sau mỗi chu kì
(3) Cấu hình electron lớp ngoài cùng của nguyên tử các nguyên tố trong một nhóm A biến đổi một cách không tuần hoàn
(4) Số thứ tự của nhóm (IA,IIA,..) cho biết số electron ở lớp ngoài cùng nhưng không cho biết số electron hóa trị trong nguyên tử của các nguyên tố đó
(5) Nhóm VIIIA là nhóm khí hiếm
(6) Nguyên tử của tất cả các nguyên tố trong nhóm khí hiếm đều có 8 electron ở lớp ngoài cùng
Số phát biểu đúng là:
A. 5
B. 2
C. 3
D. 4
Một hợp chất A được tạo thành từ các ion X+ và Y 2- . Trong X+ có 5 hạt nhân của hai nguyên tố và có 10 electron. Trong ion Y2- có bốn hạt nhân thuộc hai nguyên tố trong cùng một chu kì và đứng cách một ô trong bảng hệ thống tuần hoàn. Tổng số electron trong Y 2- là 32. Xác định công thức hóa học của A A. (NH4)2CO3 B. (NH4)2SiO3 C. (NH4)2SO4 D. (NH4)2CrO4
Đọc tiếp
Một hợp chất A được tạo thành từ các ion X+ và Y 2- . Trong X+ có 5 hạt nhân của hai nguyên tố và có 10 electron. Trong ion Y2- có bốn hạt nhân thuộc hai nguyên tố trong cùng một chu kì và đứng cách một ô trong bảng hệ thống tuần hoàn. Tổng số electron trong Y 2- là 32. Xác định công thức hóa học của A
A. (NH4)2CO3
B. (NH4)2SiO3
C. (NH4)2SO4
D. (NH4)2CrO4
Nhận thấy hợp chất A có dạng X2Y.
Dễ nhận thấy X+ trong tất cả các đáp án là NH4+ hoặc lập luận như sau:
• Với ion X+ chứa 5 hạt nhân của 2 nguyên tố → X có dạng AaBb+ với a+ b = 5
Trong X+ có 10 electron → Ztb =
10
+
1
5
= 2,2 → trong X chắc chắn chứa H → X có dạng HaBb
Với a = 1, b= 4 → ZB =
11
-
1
4
= 2,5 loại
Với a = 2, b= 3 → ZB =
11
-
2
3
= 3 ( loại do B(Z= 3) không tạo được liên kết ion với H)
Với a = 3, b= 2 → ZB =
11
-
3
2
= 4 ( Loại do không tồn tại ion C2H3+)
Với a= 4, b= 1 → ZB =
11
-
4
1
= 7 (N) → X là NH4+ ( thỏa mãn)
•Trong ion Y2- có bốn hạt nhân → Y có dạng CcDd với c + d= 4 ( Loại C, D)
Trong ion Y2- có bốn hạt nhân thuộc hai nguyên tố trong cùng một chu kì và đứng cách một ô trong bảng hệ thống tuần hoàn. → ZD = ZC + 2
Với c=1, d= 3 → ZC + 3. (ZC +2) = 30 → ZC = 6 ( C) → ZD = 8(O). Vậy Y2- có công thức CO32-.
Với c= 2,d= 2 → 2ZC + 2. (ZC +2) = 30 → ZC = 6,5 ( loại)
Với c= 3, d= 1→ 3ZC + (ZC +2) = 30 → ZC = 7 (N), ZD = 9 (F) → loại do không tạo được ion N3F2-.
Công thức của A là (NH4)2CO3.
Đáp án A.
Đúng 0
Bình luận (0)
1 Một hợp chất A tạo thành từ các ion X+ và Y2-. Trong ion X+ có 5 hạt nhân của hai nguyên tố và có 10 eletron. Trong ion Y2- có 4 hạt nhân thuộc hai nguyên tố trong cùng một chu kỳ và đứng cách nhau một ô trong bảng tuần hoàn. Tổng số eletron trong Y2- là 32. Hãy xác định các nguyên tố trong hợp chất A và lập công thức hóa học của A.
Xác định X+
X+ có 10 electron nên tổng proton trong 5 hạt nhân là 11
Z = 2,2. Vậy có 1 nguyên tử là H
Gọi nguyên tử thứ hai trong X+ là R, công thức X+ có thể là;
RH4+ : ZR + 4 = 11 → ZR = 7 (N) ; X+: NH4+ (nhận)
R2H3+ : 2ZR + 3 = 11 ZR = 4 loại : R3H2+ : 3ZR + 2 = 11 ZR = 3 loại
Xác định Y2-
Y2- có 32 eletron nên tổng số hạt proton trong 4 nguyên tử là 30.
= 7,5 2 nguyên tử trong Y2- đều thuộc cùng chu kỳ 2.
Gọi 2 nguyên tử là A, B: ZB = ZA +2
Công thức Y2- có thể là
AB32- : ZA + 3ZB = 30
ZB= ZA +2 ZA= 6 (C); ZB = 8 (O)
A2B22- : 2ZA+ 2ZB = 30
ZB = ZA + 2 ZA= 6,5; ZB = 8,5 loại
A3B2- : 3ZA + ZB = 30
ZB = ZA + 2 ZA = 7; ZB = 9 loại
Hợp chất A có công thức (NH4)2CO3
Đúng 0
Bình luận (2)
Ta có trong X+ nhé
Có 2 nguyên tố là a và b
Vì có 5 hạt nhân tức là có 5 nguyên tử mà chỉ có 10 e -> Chắc chắn phải có Hidro ( chứ nếu sang tới B là có tới 3 e rồi!)
Biện luận về số nguyên tử hidro và số e của nguyên tố còn lại (ntcl)<--- lưu ý là ion X+ có 10 -> tổng 2 nguyên tố có đến 11 e
Số Hidro : 1------2------3-----4
Số ntcl : 4------3------2-----1
Số e của ntcl:2.5----3------4-----7
Ta thấy chỉ có giá trị 4-1-7 là phù hợp bởi vì 2,5 lẻ bị loại, 3,4 là các nguyên tố kim loại ko tạo ion với Hiđro
Tra bảng tuần hoàn ta có số hiệu 7 là nguyên tố Nitơ. -> X+ là NH4+
Tổng số e trong Y 2- là 32 <=> tổng số e của 4 nguyên tố tạo nên Y2- là 30
Gọi số e của nguyên tố thứ nhất là a thì̀ số e của nguyên tố thứ 2 là a+2
lại gọi thêm số nguyên tử của 2 nguyên tố lần lượt là x,y thì ta có
x+y=4
xa + y(a+2) = 30 <=> xa + ya =28 - 2y <=> (x+y)a= 28 - 2y <=> 4a = 28 - 2y
biện luận
y-----1---------2---------3
a----6.5-----6.25------6
tới đây dừng vì y<4 ta thấy có 1 nguyên tố có 1 nguyên tử mang số hiệu 6 (oxi) -> nguyên tố còn lại mang số hiệu 8 (cacbon) và có 3 nguyên tử -> Y2- là CO3(2-)
-> A chính là ..... (NH4)2CO3
Đúng 0
Bình luận (0)
Câu 7. Nguyên tử X nhận 1e trở thành ion X- có cấu hình e:1s22s22p63s23p6 .Vị trí nguyên tố X trong BTH là: A. Chu kì 3, nhóm VIIA. B. Chu kì 4, nhóm VIA C. Chu kì 3, nhóm IA D. Chu kì 4, nhóm IA.
Đọc tiếp
Câu 7. Nguyên tử X nhận 1e trở thành ion X- có cấu hình e:1s22s22p63s23p6 .Vị trí nguyên tố X trong BTH là:
A. Chu kì 3, nhóm VIIA. B. Chu kì 4, nhóm VIA
C. Chu kì 3, nhóm IA D. Chu kì 4, nhóm IA.
X- có cấu hình e là: 1s22s22p23s23p6
=> X có cấu hình: 1s22s22p63s23p64s1
có 4 lớp e => chu kì 4
1 e lớp ngoài cùng => nhóm IA
=> D
Đúng 2
Bình luận (0)
Một hợp chất ion có công thức XY. Hai nguyên tố X,Y thuộc 2 chu kì kế cận nhau trong bảng tuần hoàn. X thuộc nhóm IA hoặc IIA, còn Y thuộc VIA hoặc VIIA. Biết tổng số electron trong XY bằng 20. XY là hợp chất nào sau đây
A. NaCl
B. NaF
C. MgO
D. B và C đúng
Đáp án D
Hướng dẫn X thuộc nhóm IA,IIA nên có điện hóa trị +1,+2
Y thuộc cùng nhóm VIA,VIIA nên Y có điện hóa trị -2 và -1
Ngoài ra ZX + ZY = 20. Vì X, Y thuộc hai chu kì kế cận nên nghiệm thích hợp là
ZX = 11 thì ZY = 9 ; X là Na , Y là F và XY là NaF
ZX = 12 thì ZY = 8 ; X là Mg , Y là O và XY là MgO
Đúng 1
Bình luận (0)








