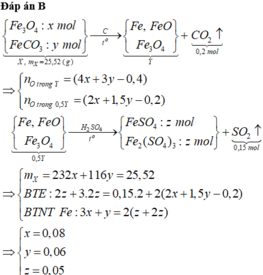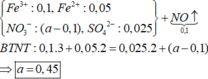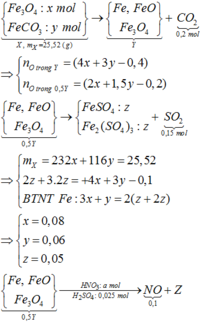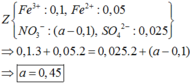GIÚP EM VỚI Ạ HUHU:((
chia m gam hỗn hợp X gồm Fe và FeO thành 2 phần bằng nhau
Phần 1: hòa tan hoàn toàn phần 1 trong h2so4 loãng dư thì thu đc 0,2 mol khí
Phần 2: hòa tan hết trong h2so4 đặc , dư thì thu được 0,35 mol khí So2 ( duy nhất )
a. tính giá trị m
b. tính số mol NaOH tối thiểu cần để hấp thụ hết lượng khí So2 trên

Những câu hỏi liên quan
Hỗn hợp X gồm Al , fe và Cu. chia a gam X thành 3 phần bằng nhau
- Phần 1 cho tác dụng vào lượng dư dung dịch HCl thì thu được 5,6 lit khí H2
- phần 2 hòa tan hoàn toàn bằng lượng dư dung dịch H2SO4 đặc đun nóng thì thu được 7,84 lít khí SO2 (sản phẩm khử duy nhất) ,dung dịch y và chất rắn Z. Cho y tác dụng với lượng dư dung dịch NaOH thu được kết tủa T. Lọc lấy T đem nung trong không khí đến khối lượng không đổi thì thu được 12 g rắn G
- phần 3 đốt cháy trong bình có chứa lượng dư khí Clo thu...
Đọc tiếp
Hỗn hợp X gồm Al , fe và Cu. chia a gam X thành 3 phần bằng nhau - Phần 1 cho tác dụng vào lượng dư dung dịch HCl thì thu được 5,6 lit khí H2 - phần 2 hòa tan hoàn toàn bằng lượng dư dung dịch H2SO4 đặc đun nóng thì thu được 7,84 lít khí SO2 (sản phẩm khử duy nhất) ,dung dịch y và chất rắn Z. Cho y tác dụng với lượng dư dung dịch NaOH thu được kết tủa T. Lọc lấy T đem nung trong không khí đến khối lượng không đổi thì thu được 12 g rắn G - phần 3 đốt cháy trong bình có chứa lượng dư khí Clo thu được b gam chất rắn E biết các phản ứng xảy ra hoàn toàn. Tính giá trị của a và b Làm hộ em với ạ!!!。゚( ゚^∀^゚)゚。
Có 78,40g hỗn hợp X gồm CuO và 1 kim loại sắt oxit được chia làm 2 phần bằng nhau Phần 1 khử hoàn toàn bằng khí CO dư ở nhiệt độ cao rồi hòa tan hết sản phẩm bằng dung dịch H2SO4 loãng dư thu được 12,80g chất không tan Phần 2 hòa tan trong dung dịch HCl thấy vừa hết 43,80 g HCl Biết các phản ứng xảy ra hoàn toàna) Viết phương trình phản ứng tính % khối lượng mỗi chất trong hỗn hợp ban đầub) Cho biết tên của sắt oxit
Đọc tiếp
Có 78,40g hỗn hợp X gồm CuO và 1 kim loại sắt oxit được chia làm 2 phần bằng nhau Phần 1 khử hoàn toàn bằng khí CO dư ở nhiệt độ cao rồi hòa tan hết sản phẩm bằng dung dịch H2SO4 loãng dư thu được 12,80g chất không tan Phần 2 hòa tan trong dung dịch HCl thấy vừa hết 43,80 g HCl Biết các phản ứng xảy ra hoàn toàn
a) Viết phương trình phản ứng tính % khối lượng mỗi chất trong hỗn hợp ban đầu
b) Cho biết tên của sắt oxit
\(\text{a) Khối lượng phần 1 = Khối lượng phần 2 = 78.4/2=39.2}\)
Đặt công thức của oxit sắt là \(Fe_xO_y\)
Phần 1: \(CuO+CO\underrightarrow{t^0}Cu+CO_2\)
\(Fe_xO_y+yCO\underrightarrow{t^0}xFe+yCO_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(\Rightarrow m_{Cu}=12.8\Rightarrow n_{Cu}=n_{CuO}=0.2\Rightarrow m_{CuO\left(\text{1 phần}\right)}=0.2\times80=16\left(g\right)\)
\(\Rightarrow\%^mCuO=\dfrac{16}{39.2}\times100\approx40.81\%\Rightarrow\%^mFe_xO_y=51.9\%\)
b)
\(\text{Đặt số mol của Fe_xO_y là a( mol)}\)
\(CuO+2HCl\rightarrow CuCl_2+H_2\)
0.2 0.4
\(Fe_xO_y+2yHCl\rightarrow FeCl_{\dfrac{2y}{x}}+yH_2O\)
a 2ay
\(\Sigma^nHCl=\dfrac{43.8}{36.5}=1.2\left(mol\right)\)
=> 2ay+0.4=1.2=>ay=0.4 (1)
\(m_{Fe_xO_y\left(\text{1 phần}\right)}=39.2-16=23.2\Rightarrow n_{Fe_xO_y}=a=\dfrac{23.2}{56x+16y}\left(mol\right)\)
=>(56x+16y)a=23.2=>56ax+16ay=23.2 (2)
Từ (1) (2) => 56ax+16*0.4=23.2=>56ax=16.8=> ax=0.3 (3)
\(\text{Từ (1) (3)}\Rightarrow\dfrac{ax}{ay}=\dfrac{0.3}{0.4}\Rightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
Công thức oxit sắt là \(Fe_3O_4\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 20 gam hỗn hợp X gồm Fe và FeO vào m gam dung dịch H2SO4 9,8% (loãng), (dư 10% so với lượng đã lấy) thì thu được 2,24 lít khí (đktc)a) Tính % theo khối lượng của FeO và giá trị mb) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng, dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính Vc) Lượng khí SO2 này có thể làm mất màu tối đa bao nhiêu ml dung dịch Br2 1M
Đọc tiếp
Hòa tan hoàn toàn 20 gam hỗn hợp X gồm Fe và FeO vào m gam dung dịch H2SO4 9,8% (loãng), (dư 10% so với lượng đã lấy) thì thu được 2,24 lít khí (đktc)
a) Tính % theo khối lượng của FeO và giá trị m
b) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng, dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính V
c) Lượng khí SO2 này có thể làm mất màu tối đa bao nhiêu ml dung dịch Br2 1M
Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp X gồm CO2, CO, H2, H2O. Dẫn X đi qua 25,52 gam hỗn hợp Fe3O4 và FeCO3 nung nóng thu được chất rắn Y gồm Fe, FeO, Fe3O4; hơi nước và 0,2 mol CO2. Chia Y thành 2 phần bằng nhau: – Phần 1: Hòa tan hết trong dung dịch chứa a mol HNO3 và 0,025 mol H2SO4, thu được 0,1 mol khí NO duy nhất. – Phần 2: Hòa tan hết trong dung dịch H2SO4 đặc nóng, thu được dung dịch chứa hai muối có số mol bằng nhau và 0,15 mol khí SO2 duy nhất. Giá trị của a là A. 0,40 mol...
Đọc tiếp
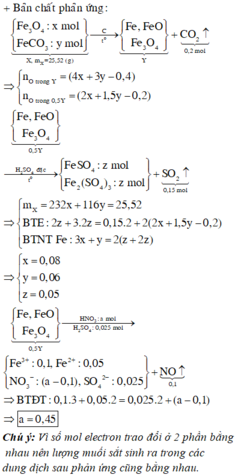
Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp X gồm CO2, CO, H2, H2O. Dẫn X đi qua 25,52 gam hỗn hợp Fe3O4 và FeCO3 nung nóng thu được chất rắn Y gồm Fe, FeO, Fe3O4; hơi nước và 0,2 mol CO2. Chia Y thành 2 phần bằng nhau:
– Phần 1: Hòa tan hết trong dung dịch chứa a mol HNO3 và 0,025 mol H2SO4, thu được 0,1 mol khí NO duy nhất.
– Phần 2: Hòa tan hết trong dung dịch H2SO4 đặc nóng, thu được dung dịch chứa hai muối có số mol bằng nhau và 0,15 mol khí SO2 duy nhất.
Giá trị của a là
A. 0,40 mol
B. 0,45 mol
C. 0,35 mol
D. 0,50 mol
Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp X gồm
C
O
2
, CO,
H
2
,
H
2
O
. Dẫn X đi qua 25,52 gam hỗn hợp
F
e
3
O
4
và
F
e
C
O
3
nung nóng thu được chất rắn Y gồm Fe, FeO,
F...
Đọc tiếp
Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp X gồm C O 2 , CO, H 2 , H 2 O . Dẫn X đi qua 25,52 gam hỗn hợp F e 3 O 4 và F e C O 3 nung nóng thu được chất rắn Y gồm Fe, FeO, F e 3 O 4 ; hơi nước và 0,2 mol C O 2 . Chia Y thành 2 phần bằng nhau:
- Phần 1: Hòa tan hết trong dung dịch chứa a mol H N O 3 và 0,025 mol H 2 S O 4 , thu được 0,1 mol khí NO duy nhất.
- Phần 2: Hòa tan hết trong dung dịch H 2 S O 4 đặc nóng, thu được dung dịch chứa hai muối có số mol bằng nhau và 0,15 mol khí S O 2 duy nhất.
Giá trị của a là
A. 0,50 mol.
B. 0,45 mol.
C. 0,35 mol.
D. 0,40 mol.
Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp X gồm CO2, CO, H2, H2O. Dẫn X đi qua 25,52 gam hỗn hợp Fe3O4 và FeCO3 nung nóng thu được chất rắn Y gồm Fe, FeO, Fe3O4; hơi nước và 0,2 mol CO2. Chia Y thành 2 phần bằng nhau: - Phần 1: Hòa tan hết trong dung dịch chứa a mol HNO3 và 0,025 mol H2SO4, thu được 0,1 mol khí NO duy nhất. - Phần 2: Hòa tan hết trong dung dịch H2SO4 đặc nóng, thu được dung dịch chứa hai muối có số mol bằng nhau và 0,15 mol khí SO2 duy nhất. Giá trị của a là A. 0,40 mo...
Đọc tiếp
Cho hơi nước đi qua than nóng đỏ thu được hỗn hợp X gồm CO2, CO, H2, H2O. Dẫn X đi qua 25,52 gam hỗn hợp Fe3O4 và FeCO3 nung nóng thu được chất rắn Y gồm Fe, FeO, Fe3O4; hơi nước và 0,2 mol CO2. Chia Y thành 2 phần bằng nhau:
- Phần 1: Hòa tan hết trong dung dịch chứa a mol HNO3 và 0,025 mol H2SO4, thu được 0,1 mol khí NO duy nhất.
- Phần 2: Hòa tan hết trong dung dịch H2SO4 đặc nóng, thu được dung dịch chứa hai muối có số mol bằng nhau và 0,15 mol khí SO2 duy nhất.
Giá trị của a là
A. 0,40 mol
B. 0,45 mol
C. 0,35 mol
D. 0,50 mol
Cho 15,6gam hỗn hợp A gồm Zn,Cu,Al thành 2 phần bằng nhau. Phần 1 hòa tan hết trong dd H2SO4 đặc nóng dư thì thu được 7,84l khí SO2 *dktc. Phần 2 tác dụng với oxi dư thu được m gam hỗn hợp oxit. Tìm m
\(m_{KL\left(mỗi.phần\right)}=\dfrac{1}{2}.15,6=7,8\left(g\right)\)
- Phần 1:
\(n_{SO_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
PTHH:
\(Zn+2H_2SO_{4\left(đ,nóng\right)}\rightarrow ZnSO_4+SO_2\uparrow+2H_2O\left(1\right)\\ Cu+2H_2SO_{4\left(đ,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\left(2\right)\\ 2Al+6H_2SO_{4\left(đ,nóng\right)}\rightarrow Al_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\left(3\right)\)
Theo PTHH (1,2, 3): \(n_{H_2O}=n_{H_2SO_4}=2n_{SO_2}=2.0,35=0,7\left(mol\right)\)
Áp dụng ĐLBTKL:
\(m_{KL}+m_{H_2SO_4}=m_{muối.sunfat}+m_{SO_2}+m_{H_2O}\)
=> mmuối sunfat = 7,8 + 0,7.98 - 0,35.64 - 0,7.18 = 41,4 (g)
\(\rightarrow m_{SO_4^{2-}}=41,4-7,8=33,6\left(g\right)\\ n_{SO_4^{2-}}=\dfrac{33,6}{96}=0,35\left(mol\right)\)
- Phần 2:
PTHH:
\(2Zn+O_2\underrightarrow{t^o}2ZnO\\ 2Cu+O_2\underrightarrow{t^o}2CuO\\ 4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(n_{O^{2-}}=n_{SO_4^{2-}}=0,35\left(mol\right)\\ \rightarrow m_{O^{2-}}=0,35.16=5,6\left(g\right)\\ \rightarrow m=5,6+7,8=13,4\left(g\right)\)
Đúng 3
Bình luận (2)
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư. 1. Tính số mol H2SO4 đã tham gia phản ứng 2. Tính khối lượng muối sunfat thu được. b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc). Xác định công thức của oxit kim loại đã dùng?
Đọc tiếp
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư. 1. Tính số mol H2SO4 đã tham gia phản ứng 2. Tính khối lượng muối sunfat thu được.
b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc). Xác định công thức của oxit kim loại đã dùng?
a, Ta có: $n_{O}=0,6(mol)$
Suy ra $n_{H^+/pu}=1,2(mol)\Rightarrow n_{H_2SO_4}=0,6(mol)$
Bảo toàn khối lượng ta có: $m_{muoi}=29,6+0,6.96=87,2(g)$
Đúng 1
Bình luận (0)
Theo gt ta có: $n_{H_2}=0,044(mol);n_{H_2/(2)}=0,033(mol)$
Gọi CTTQ của oxit là $M_xO_y$
Ta có: \(M_{M_xO_y}=58y\)
Mặt khác $m_{M}=2,552-0,044.16=1,848(g)\Rightarrow M_{M}=28n$
Vậy M là Fe
Do đó CT của oxit cần tìm là Fe3O4
Đúng 1
Bình luận (0)
Chia 14,8 gam hỗn hợp gồm Mg, Ni, Zn thành 2 phần bằng nhau. Phần 1 hòa tan hoàn toàn trong dung dịch H2SO4 đặc nóng dư, thu được 21,8 gam muối. Phần 2 cho tác dụng hết với dung dịch AgNO3 thấy khối lượng chất rắn tăng m gam. Giá trị của m là: A. 25 B. 17,6 C. 8,8 D. 1,4
Đọc tiếp
Chia 14,8 gam hỗn hợp gồm Mg, Ni, Zn thành 2 phần bằng nhau. Phần 1 hòa tan hoàn toàn trong dung dịch H2SO4 đặc nóng dư, thu được 21,8 gam muối. Phần 2 cho tác dụng hết với dung dịch AgNO3 thấy khối lượng chất rắn tăng m gam. Giá trị của m là:
A. 25
B. 17,6
C. 8,8
D. 1,4
Đáp án A
Khối lượng hỗn hợp kim loại ở mỗi phần là 7,4 gam.
Phần 1: Khối lượng muối thu được lớn hơn khối lượng kim loại ban đầu là do các cation kim loại kết hợp với các gốc S O 4 2 - tạo thành muối.
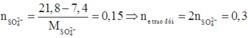
Số mol electron trao đổi ở hai phần bằng nhau.
Do đó ở phần 2: nAg = ne trao đổi = 0,3
=> mAg = 32,4 (gam)
Vậy m = 32,4 – 7,4 = 25 (gam)
Đúng 0
Bình luận (0)