Đốt cháy hoàn toàn một hợp chất hữu cơ A chỉ chứa 2 nguyên tố thu được 11 gam CO2 và 6,75 gam H,O. Hãy xác định công thức phân tử của A, biết PTK của A là 30?
cho mk xin gấp đáp án với ạ
Đốt cháy hoàn toàn 3,75 gam một chất hữu cơ A, thu được 11 gam CO2 và 6,75 gam H2O. Biết khối lượng mol của A là 30 gam. Xác định công thức phân tử của A.
a) A hợp chất hữu cơ A gồm những nguyên tố nào ?
b) xác định công thức phân tử của hợp chất hữu cơ A
c) Dẫn toàn bộ khí sinh đi qua bình đựng dung dịch NaOH dư. Tính khối lượng muối tạo thành.
a, có nCO2=11/44=0,25 mol
có nC=nCO2=0,25mol=>mC=12.0,25=3(g)
có nH2O=6,75/18=0,375mol
có nH=2nH2O=2.0,375=0,75mol=>mH=0,75(g)
=>mH+mC=0,75+3=3,75=mA
=> A gồm nguyên tố C và H
b, gọi CTPT A là CxHy
có x/y=nC/nH=0,25/0,75=1/3
=> công thức thực nghiệm (CH3)n<=>CnH3n
có MA=30 gam/mol<=>12n+3n=30<=>n=2
vậy CTPT của A là C2H6
c;PTHH: CO2+2NaOH->Na2CO3+H2O
=> nNa2CO3=nCO2=0,25mol=>mNa2CO3=0,25.106=26,5 gam
Đốt hoàn toàn 1 dung lượng hợp chất hữu cơ AC gồm 2 nguyên tố, thu được 8,8 gam khí CO2 và 5,4 gam h2O. Hãy xác định công thức phân tử của A biết PTK của A bằng 30
Đốt cháy hoàn toàn 3 gam chất hữu cơ A chứa các nguyên tố C, H, O thu được 6,6 gam khí CO 2 và 3,6 gam H 2 O . Hãy xác định công thức phân tử của A, biết khối lượng mol phân tử của A là 60 gam/mol.
Gọi công thức của A là C x H y O z
Đốt cháy 3 gam A được 6,6 gam CO 2 và 3,6 gam H 2 O
Vậy m C trong 3 gam A là 6,6/44 x 12 = 1,8g
m H trong 3 gam A là 3,6/18 x 2 = 0,4g
Vậy trong 3 gam A có 3 - 1,8 - 0,4 = 0,8 (gam) oxi.
Ta có quan hệ:
60 gam A → 12x gam C → y gam H → 16z gam O
3 gam A → 1,8 gam C → 0,4 gam H → 0,8 gam O
=> x = 60 x 1,8 /36 = 3 ; y = 60 x 0,4/3 = 8
z = 60 x 0,8/48 = 1
Công thức của A là C 3 H 8 O
hợp chất hữu cơ A có 2 nguyên tố. Khi đốt hoàn toàn 6 gam một hợp chất hữu cơ A thu được 17.6 gam co2 và 10.8 gam h2o .
trong a có chứa những nguyên tố nào?
biết phân tử khối của a nhở hơn 40. xác định công thức phân tử a?
a có làm mất màu dung dịch brom không ?
- Đốt cháy A thu CO2 và H2O, A có 2 nguyên tố.
→ A chứa C và H.
Gọi CTPT của A là CxHy.
Ta có:\(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\Rightarrow n_H=0,6.2=1,2\left(mol\right)\)
⇒ x:y = 0,4:1,2 = 1:3
→ A có CTPT dạng (CH3)n ( n nguyên dương)
Mà: MA < 40
\(\Rightarrow\left(12+1.3\right)n< 40\Rightarrow n< 2,67\)
⇒ n = 1 (loại vì không thỏa mãn hóa trị của C)
n = 2 (tm)
Vậy: CTPT của A là C2H6.
- A không làm mất màu dd Br2.
Thủy phân hoàn toàn 2,85 gam hợp chất hữu cơ A (chứa C, H, O) thu được m1 gam chất X và m2 gam chất Y chỉ chứa một loại nhóm chức. Đốt cháy hết m1 gam X tạo ra 0,09 mol CO2 và 0,09 mol H2O, còn khi đốt cháy hết m2 gam Y thu được 0,03 mol CO2 và 0,045 mol H2O. Tổng lượng oxi tiêu tốn cho cả hai phản ứng cháy trên đúng bằng lượng oxi tạo ra khi nhiệt phân hoàn toàn 42,66 gam KMnO4. Biết phân tử khối của X là 90(u); Y không hòa tan Cu(OH)2. Xác định công thức phân tử của các chất A, X, Y biết A có công thức phân tử trùng với công thức đơn giản nhất.
Hai chất hữu cơ A, B có cùng công thức phân tử. Đốt cháy hoàn toàn 7,4 gam hỗn hợp A, B thu được 17,6 gam CO 2 và 9 gam H 2 O . Xác định công thức phân tử của A, B. Biết trong phân tử A, B chứa một nguyên tử oxi.
Cho 7,4 gam hỗn hợp A, B tác dụng với Na dư sao cho phản ứng xảy ra hoàn toàn thấy tạo ra 0,672 lít khí H 2 ở đktc. Hãy xác định công thức cấu tạo của A, B.
Gọi công thức phân tử của A, B là C x H y O
Phương trình hoá học:
C x H y O + (x +y/4 -1/2) O 2 → x CO 2 + y/2 H 2 O
n CO 2 = 17,6/44 = 0,4 mol; n H 2 O = 9/18 = 0,5 mol (1)
m C = 0,4.12 = 4,8 gam; m H = 0,5.2 = 1g (2)
Từ (1), (2)
→ x : y : 1 = 4,8/12 : 1/1 : 1,6/16 = 0,4 : 1 : 0,1
Vậy m O = 7,4 - 4,8 - 1,0 = 1,6 (gam)
=> Công thức phân tử của A, B là C 4 H 10 O
Ta có M A , B = 74 (g/mol)
n A , B = 7,4/74 = 0,1 mol
Khi phản ứng với Na có khí bay ra → trong A, B có nhóm OH.
Phương trình hoá học :
C 4 H 9 OH + Na → C 4 H 9 ONa + 1/2 H 2
Vậy số mol có nhóm OH là 2 n H 2 = 2. 0,672/22,4 = 0,06 < n A , B
→ trong A, B có 1 chất không có nhóm OH → Cấu tạo tương ứng là
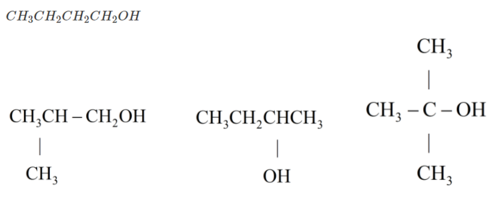
Chất không có nhóm OH :
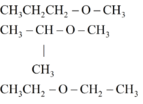
đốt cháy hoàn toàn 5,75 gam hợp chất hữu cơ X(chứa C , H , O)thu được 11,0 gam CO2 và 6,75 gam H20
a)Tính thành phần phần trăm của các nguyên tố trong X
b)Lập công thức đơn giản nhất của X
c)Tìm công thức phân tử của X.Biết tỉ khối hơi của X so với khí hiđro bằng 23
Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{11}{44}=0,25\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2.\dfrac{6,75}{18}=0,75\left(mol\right)\)
\(n_O=\dfrac{5,75-\left(0,25.12+0,75.1\right)}{16}=0,125\left(mol\right)\)
\(\%C=\dfrac{0,25.12}{5,75}.100=52,17\%\)
\(\%H=\dfrac{0,75.1}{5,75}.100=13,04\%\)
\(\%O=100-52,17-12,04=34,79\%\)
Đặt CTTQ X: CxHyOz
\(x:y:z=0,25:0,75:0,125=2:6:1\)
CTĐG X: \(\left(C_2H_6O\right)_n\)
\(M_X=23.2=46\) \((g/mol)\)
\(\Leftrightarrow46n=46\)
\(\Leftrightarrow n=1\)
`->` CTPT X: C2H6O
Khi đốt hoàn toàn 2,2 gam một hợp chất hữu cơ X thu được 6,6 gam CO2 và 3,6 gam H2O.Tỷ khối của X đối với hiđro là 22. Xác định công thức phân tử của hợp chất hữu cơ X?
xin đ/án gấp ạk
\(n_C=n_{CO_2}=\dfrac{6,6}{44}=0,15\left(mol\right);n_H=2.n_{H_2O}=2.0,2=0,4\left(mol\right)\\ m_C+m_H=0,15.12+0,4.1=2,2\left(g\right)=m_X\\ Đặt.CTPT.X:C_aH_b\left(a,b:nguyên,dương\right)\\ a:b=0,15:0,4=3:8\\ Vậy.CTPT.X:C_3H_8\)
Hợp chất hữu cơ A có tỷ khối đối với hiđro là 14. Đốt cháy 1,4 gam A thu được sản phẩm gồm 4,4 gam CO2 và 1,8 gam H,O. Xác định công thức phân tử của A?
cho mk xin gấp đ/an vs ạk
\(M_A=2.14=28\left(\dfrac{g}{mol}\right)\\ n_A=\dfrac{1,4}{28}=0,05\left(mol\right)\\ n_C=n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)\\ n_H=2.n_{H_2O}=2.0,1=0,2\left(mol\right)\\ n_C:n_A=0,1:0,05=2;n_H:n_A=0,2:0,05=4\\ \Rightarrow CTPT.A:C_2H_4\)