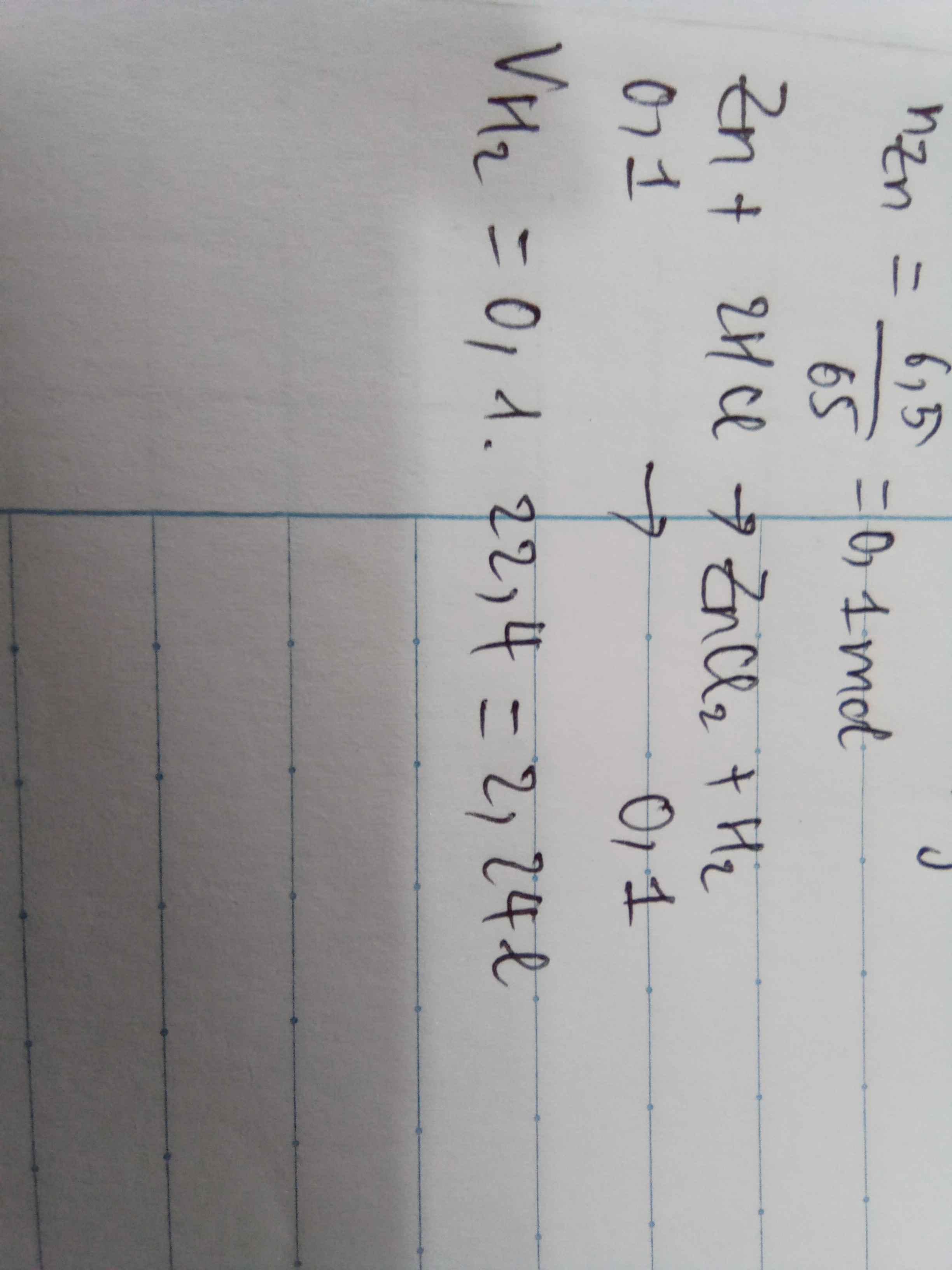Cho 6,5 g zn tác dụng với 200g dd hcl thu được v lít ở đktc A, viết pt B, tính V C, tính C% ddsaupư

Những câu hỏi liên quan
Cho 6,5g Zn tác dụng với 200g dd HCl 17,8%. Sau phản ứng thu được V lít khí Hidro a) Tính khối lượng HCl cần dùng b) tính V c) Tính C% các chất còn lại sau phản ứng
\(a.n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ n_{HCl}=\dfrac{17,8\%.200}{36,5}=\dfrac{356}{365}\left(mol\right)\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ Vì:\dfrac{0,1}{1}< \dfrac{\dfrac{356}{365}}{2}\\ \Rightarrow Znhết,HCldư\\ n_{HCl\left(dùng\right)}=0,1.2=0,2\left(mol\right)\\ m_{HCl\left(dùng\right)}=0,2.36,5=7,3\left(g\right)\\ b.n_{H_2}=n_{ZnCl_2}=n_{Zn}=0,1\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ c.n_{HCl\left(Dư\right)}=\dfrac{356}{365}-0,2=\dfrac{283}{365}\left(mol\right)\\ C\%_{ddZnCl_2}=\dfrac{0,1.136}{6,5+200}.100\approx6,586\%\)
\(C\%_{ddHCl\left(dư\right)}=\dfrac{\dfrac{283}{365}.36,5}{6,5+200}.100\approx13,705\%\)
Đúng 2
Bình luận (0)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính thể tích khí H2 (đktc)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
Đúng 2
Bình luận (0)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).a) Viết phương trình hóa học xảy ra.b) Tính thể tích khí H2 (đktc)
Cho m g Zn tác dụng vừa đủ với 250 ml dd HCl 7,3% tạo ra khí H2 và ZnCl2
a. Viết PTHH.
b. Tính m và V H2 (đktc)
c. Tính C% dd muối thu được sau phản ứng.
a) $Zn+ 2HCl \to ZnCl_2 + H_2$
b) $n_{HCl} = \dfrac{250.7,3\%}{36,5} = 0,5(mol)$
$n_{Zn} = n_{H_2} = \dfrac{1}{2}n_{HCl} = 0,25(mol)$
$m = 0,25.65 =16,25(gam) ; V_{H_2} = 0,25.22,4 = 5,6(lít)$
c)
$m_{dd\ sau\ pư} = 16,25 + 250 - 0,25.2 = 265,75(gam)$
$C\%_{ZnCl_2} = \dfrac{0,25.136}{265,75}.100\% = 12,8\%$
Đúng 2
Bình luận (0)
\(a/ 4Zn+2HCl \to ZnCl_2+H_2 \\ n_{HCl}=\frac{250.7,3\%}{36,5}=0,5(mol)\\ b/ \\ n_{Zn}=n_{H_2}=n_{ZnCl_2}=\frac{1}{2}.n_{HCl}=\frac{1}{2}.0,5=0,25(mol)\\ m_{Zn}=0,25.65=16,25(g)\\ V_{H_2}=0,25.22,4=5,6(l)\\ c/ \\ C\%_{ZnCl_2}=\frac{0,25.136}{16,25+250-0,25.2}.100=12,8\% \)
Đúng 0
Bình luận (0)
Cho m g Zn tác dụng vừa đủ với 250 ml dd HCl 7,3% tạo ra khí H2 và ZnCl2
a. Viết PTHH.
b. Tính m và V H2 (đktc)
c. Tính C% dd muối thu được sau phản ứng.
a)
Zn+2HCl→ZnCl2+H2
b)
nZn=nH2=12nHCl=0,25(mol)
m=0,25.65=16,25(gam);VH2=0,25.22,4=5,6(lít)
c)
mdd sau pư=16,25+250−0,25.2=265,75(gam)
Đúng 1
Bình luận (0)
Cho 6,5 gam Zn tác dụng hết với dung dịch axit HCl thu được muối ZnCl2 và thoát ra V lít khí H2 (đktc).
a) Viết phương trình hóa học xảy ra.
b) Tính thể tích khí H2 (đktc)
Đánh máy giúm nha
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ----> ZnCl2 + H2
Mol: 0,1 0,1
b, \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
cho khối lượng của Zn là 6,5 g phản ứng hết với dung dịch HCl tạo ra khí H2 và zncl2 Tính khối lượng của zncl2 sinh ra b tính thể tích khí sinh ra ở điều kiện chuẩn
Đúng 0
Bình luận (0)
Cho 6,5 gam Zn tác dụng với dung dịch HCL. Sau phản ứng thu được m(g) muối và V (lít) khí. Tính m và V
Zn+2Hcl->Zncl2+H2
0,1------------0,1----0,1 mol
n Zn=6,5\65=0,1 mol
=>m, ZnCl2=0,1.136=13,6g
=>VH2=0,1.22,4=2,24l
Đúng 1
Bình luận (0)
Cho 6,5 gam Zn tác dụng với dung dịch HCl dưa. Viết PTHH xảy ra.b. Tính thể tích khí hidro thu được ở đktc ?c. Tính khối lượng HCl cần dùng
Đọc tiếp
Cho 6,5 gam Zn tác dụng với dung dịch HCl dư
a. Viết PTHH xảy ra.
b. Tính thể tích khí hidro thu được ở đktc ?
c. Tính khối lượng HCl cần dùng
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,1\left(mol\right)\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c, \(n_{HCl}=2n_{Zn}=0,2\left(mol\right)\Rightarrow m_{HCl}=0,2.36,5=7,3\left(g\right)\)
Đúng 2
Bình luận (0)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(1mol\) \(2mol\) \(1mol\)
\(0,1mol\) \(0,2mol\) \(0,1mol\)
\(n_{Zn}=\dfrac{m}{M}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(m_{HCl}=n.M=0,2.36,5=7,3\left(g\right)\)
\(V_{H_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
Đúng 0
Bình luận (0)
Gặp trường hợp
Cho một lượng Zn dư tác dụng với 100 mol dd hcl phản ứng Thu được 3.36 lít h2 (đktc)
a. Viết phản ứng
B. tính mzn tham gia
c . Tính CM hcl đã dùng
Xem chi tiết
a) Zn + 2HCl → ZnCl2 + H2
b) nH2 = 3,36:22,4 = 0,15 mol => mZn = 0,15.65 = 9,75 gam
c) nHCl = 2nH2 = 0,3 mol
=>CHCl = \(\dfrac{0,3}{0,1}\)= 3M
Đúng 1
Bình luận (0)
cho 6,5 g Zn tác dụng hết 200g dung dịch HCl
a. Viết PTHH
b. Tính khối lượng muối thu được(ZnCl2) và V khí Hidro thu được (ở đktc)
c. tính nồng độ phần trăm dung dịch axit và nêu cách pha chế 200g dung dịch tương ứng với C% trên
Giúp mình câu c với ạ!! Cảm ơn