cho 10 gam hỗn hợp X gồm Fe và FeO tác dụng với axit clohidic tạo ra muối và 2,24 (l) khí hidro (đktc)
a) viết PTHH
b) tính khối lượng từng chất trong hỗn hợp X
c) tính % khối lượng từng chất trong X?
Cho 16g hỗn hợp gồm Fe và Cu tác dụng với axit Clohidic, sau phản ứng thu được 4,48 lít khí H2 (đktc)
a) Viết PTHH
b)Tính khối lượng kim loại trong hỗn hợp
c) Tính khối lượng axit đã tham gia phản ứng..
\(n_{H2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
a) Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2
b) \(n_{Fe}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{Fe}=0,2.56=11,2\left(g\right)\)
\(m_{Cu}=16-11,2=4,8\left(g\right)\)
c) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
Chúc bạn học tốt
4. Cho 16,5g hỗn hợp X gồm Fe và ZnO tác dụng với dung dịch H2SO4 2M, thu được 3,36 lít khí (đktc)
a) Viết PTHH
b) Tính khối lượng từng chất trong hỗn hợp ban đầu
c) Tính thể tích dung dịch H2SO4 2M cần dùng
d) Cho lượng hỗn hợp X nói trên vào dung dịch CuSO4 dư thì sau phản ứng thu được bao nhiêu gam chất rắn.
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\\ a)ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,15 0,15 0,15 0,15
\(b)m_{Fe}=0,15.56=8,4g\\ m_{ZnO}=16,5-8,4=8,1g\\ c)n_{ZnO}=\dfrac{8,1}{81}=0,1mol\\ ZnO+H_2SO_4\rightarrow ZnSO_4+H_2O\)
0,1 0,1 0,1 0,1
\(V_{ddH_2SO_4}=\dfrac{0,15+0,1}{2}=0,125M\\ d)Fe+CuSO_4\rightarrow FeSO_4+Cu\)
0,15 0,15 0,15 0,15
\(m_{rắn}=m_{ZnO}+m_{Cu}=8,1+0,15.64=17,7g\)
Cho dung dịch HCl 0,5M tác dụng vừa đủ với 21,6 gam hỗn hợp A gồm Fe, FeO, FeCO 3 . Thấy thoát ra một hỗn hợp khí có tỉ khối đối với H 2 là 15 và tạo ra 31,75 gam muối clorua. Tính % khối lượng của mỗi chất trong hỗn hợp A.
Phương trình hóa học :
Fe + 2HCl → FeCl 2 + H 2
FeO + 2HCl → FeCl 2 + H 2 O
FeCO 3 + 2HCl → FeCl 2 + H 2 O + CO 2
Tính % khối lượng: Gọi số mol Fe, FeO, FeCO 3 trong hỗn hợp là x, y, z => x + y + z = 0,25
Theo phương trình hóa học : Số mol H 2 , CO 2 là x, z
![]()
Mặt khác : 56x + 72y + 116z = 21,6
Giải ra ta có:
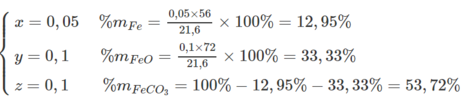
Cho 17 g hỗn hợp Na và Na2O tác dụng với lượng nước dư thì được 2,24 lit khí hidro (ở đktc)
a. Viết PTHH của các phản ứng xảy ra .
b. Tính khối lượng mỗi chất có trong hỗn hợp X
c. Tính khối lượng chất tan trong dung dịch sau phản ứng.
d. Nếu đem toàn bộ lượng H2 sinh ra ở trên khử 24 g bột CuO ở nhiệt độ cao thì sau phản ứng thu được bao nhiêu gam Cu.
Biết : Na = 23 ; O = 16; H = 1 ; Cu=64 .
nH2 = 2.24/22.4 = 0.1 (mol)
Na + H2O => NaOH + 1/2 H2
0.2....................0.2..........0.1
mNa = 0.2 * 23 = 4.6 (g)
mNa2O = 17 - 4.6 = 12.4 (g)
nNa2O = 12.4/62 = 0.2 (mol)
Na2O + H2O => 2NaOH
0.2........................0.4
nNaOH = 0.2 + 0.4 = 0.6 (mol)
mNaOH = 0.6 * 40 = 24 (g)
nCuO = 24/80 = 0.3 (mol)
CuO + H2 -t0-> Cu + H2O
1...........1
0.3.........0.1
LTL : 0.3/1 > 0.1/1
=> CuO dư
nCu = nH2 = 0.1 (mol)
mCu = 0.1 * 64 = 6.4 (g)
Bài 23: Cho 23,8 gam hỗn hợp X gồm Mg, Fe và Al tác dụng hoàn toàn với dung dịch HCl dư thì thu được 17,92 lit khí ở đktc. Mặt khác, cho 23,8 gam hỗn hợp X tác dụng vừa đủ với 20,16 lít khí Cl2 ở đktc. Tính khối lượng từng chất trong hỗn hợp X?
Gọi số mol Mg, Fe, Al là a, b, c
=> 24a + 56b + 27c = 23,8
PTHH: Mg + 2HCl --> MgCl2 + H2
a------------------------->a
Fe + 2HCl --> FeCl2 + H2
b------------------------->b
2Al + 6HCl --> 2AlCl3 + 3H2
c------------------------->1,5c
=> a + b + 1,5c = \(\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
PTHH: Mg + Cl2 --to--> MgCl2
a-->a
2Fe + 3Cl2 --to--> 2FeCl3
b--->1,5b
2Al + 3Cl2 --to--> 2AlCl3
c--->1,5c
=> \(a+1,5b+1,5c=\dfrac{20,16}{22,4}=0,9\left(mol\right)\)
=> a = 0,3; b = 0,2; c = 0,2
=> \(\left\{{}\begin{matrix}m_{Mg}=0,3.24=7,2\left(g\right)\\m_{Fe}=0,2.56=11,2\left(g\right)\\m_{Al}=0,2.27=5,4\left(g\right)\end{matrix}\right.\)
Cho 10,65 gam hỗn hợp X gồm Zn, Fe và Al tác dụng hoàn toàn với 200 gam dung dịch HCl a% vừa đủ thì thu được 5,04 lit khí ở đktc. Mặt khác, cho 10,65 gam hỗn hợp X tác dụng vừa đủ với 5,6 lít khí Cl2 ở đktc. Tính khối lượng từng chất trong hỗn hợp X?
a. Tính phần trăm khối lượng của từng KL trong hỗn hợp ban đầu.
b. Tính a=?
c. Tính C% các chất trong dung dịch thu được sau phản ứng.
Gọi \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\\n_{Al}=c\left(mol\right)\end{matrix}\right.\) => 65a + 56b + 27c = 10,65 (1)
PTHH: Zn + 2HCl --> ZnCl2 + H2
Fe + 2HCl --> FeCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
=> \(n_{H_2}=a+b+1,5c=\dfrac{5,04}{22,4}=0,225\left(mol\right)\) (2)
PTHH: Zn + Cl2 --to--> ZnCl2
2Fe + 3Cl2 --to--> 2FeCl3
2Al + 3Cl2 --to--> 2AlCl3
=> \(n_{Cl_2}=a+1,5b+1,5c=\dfrac{5,6}{22,4}=0,25\left(mol\right)\) (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,1\left(mol\right)\\b=0,05\left(mol\right)\\c=0,05\left(mol\right)\end{matrix}\right.\) => \(\left\{{}\begin{matrix}m_{Zn}=0,1.65=6,5\left(g\right)\\m_{Fe}=0,05.56=2,8\left(g\right)\\m_{Al}=0,05.27=1,35\left(g\right)\end{matrix}\right.\)
a) \(\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{6,5}{10,65}.100\%=61,033\%\\\%m_{Fe}=\dfrac{2,8}{10,65}.100\%=26,291\%\\\%m_{Al}=\dfrac{1,35}{10,65}.100\%=12,676\%\end{matrix}\right.\)
b) nHCl = 2a + 2b + 3c = 0,45 (mol)
=> mHCl = 0,45.36,5 = 16,425 (g)
=> \(a\%=C\%=\dfrac{16,425}{200}.100\%=8,2125\%\)
c) mdd sau pư = 10,65 + 200 - 0,225.2 = 210,2 (g)
=> \(\left\{{}\begin{matrix}C\%_{ZnCl_2}=\dfrac{0,1.136}{210,2}.100\%=6,47\%\\C\%_{FeCl_2}=\dfrac{0,05.127}{210,2}.100\%=3,02\%\\C\%_{AlCl_3}=\dfrac{0,05.133,5}{210,2}.100\%=3,176\%\end{matrix}\right.\)
cho 27,2 gam hỗn hợp A gồm rượu etylic và axit axetic tác dụng với natri dư thu được 5,6 lít khí H2 (đktc).tính khối lượng từng chất trong hỗn hợp A
n C2H5OH =a (mol) ; n CH3COOH = b(mol)
=> 46a + 60b = 27,2(1)
$2C_2H_5ONa + 2Na \to 2C_2H_5ONa + H_2$
$2CH_3COOH + 2Na \to 2CH_3COONa + H_2$
Theo PTHH :
n H2 = 0,5a + 0,5b = 5,6/22,4 = 0,25(2)
Từ (1)(2) suy ra a = 0,2 ; b = 0,3
Suy ra:
m C2H5OH = 0,2.46 = 9,2(gam)
m CH3COOH = 0,3.60 = 18(gam)
Cho 1,98 gam hỗn hợp X gồm Mg và Al vào 160 ml HCl 1,5M (dư) thu được 2,352 lít (đktc) khí H2 và dung dịch Y a. Tính % khối lượng từng chất trong hỗn hợp X b. Tính khối lượng muối có trong Y và nồng độ mol/l từng chất trong dung dịch Y cho rằng thể tích dung dịch
a) Gọi số mol Mg, Al là a, b (mol)
=> 24a + 27b = 1,98 (1)
PTHH: Mg + 2HCl --> MgCl2 + H2
a--->2a-------->a---->a
2Al + 6HCl --> 2AlCl3 + 3H2
b---->3b------->b----->1,5b
=> \(n_{H_2}=a+1,5b=\dfrac{2,352}{22,4}=0,105\left(mol\right)\) (2)
(1)(2) => a = 0,015 (mol); b = 0,06 (mol)
\(\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,015.24}{1,98}.100\%=18,18\%\\\%m_{Al}=\dfrac{0,06.27}{1,98}.100\%=81,82\%\end{matrix}\right.\)
b)
\(\left\{{}\begin{matrix}m_{MgCl_2}=0,015.95=1,425\left(g\right)\\m_{AlCl_3}=0,06.133,5=8,01\left(g\right)\end{matrix}\right.\)
\(\left\{{}\begin{matrix}C_{M\left(MgCl_2\right)}=\dfrac{0,015}{0,16}=0,09375M\\C_{M\left(AlCl_3\right)}=\dfrac{0,06}{0,16}=0,375M\\C_{M\left(HCl.dư\right)}=\dfrac{0,16.1,5-0,015.20,06.2}{0,16}=0,5625M\end{matrix}\right.\)
Bài 7: Cho 10,65 gam hỗn hợp X gồm Zn, Fe và Al tác dụng hoàn toàn với 200 gam dung dịch HCl a% vừa đủ thì thu được 10,08 lit khí ở đktc. Mặt khác, cho 10,65 gam hỗn hợp X tác dụng vừa đủ với 5,6 lít khí Cl2 ở đktc. Tính khối lượng từng chất trong hỗn hợp X?
a. Tính phần trăm khối lượng của từng KL trong hỗn hợp ban đầu.
b. Tính a=?
c. Tính C% các chất trong dung dịch thu được sau phản ứng.