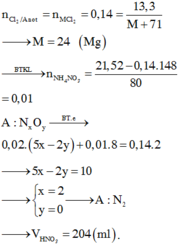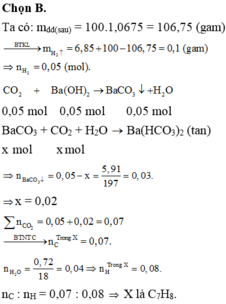Cho 1,365 gam một kim loại kiềm A tan hoàn toàn vào H2O thu được 1 dung dịch có khối lượng nước lớn hơn so với lượng nước đã dùng là 1,33 gam. Tìm A

Những câu hỏi liên quan
Hòa tan hoàn toàn 2,73 gam kim loại kiềm vào nước thu được một dung dịch có khối lượng lớn hơn so với lượng nước đã dùng là 2,66 gam. Đó là kim loại A. Na B. RB C. K D. Li
Đọc tiếp
Hòa tan hoàn toàn 2,73 gam kim loại kiềm vào nước thu được một dung dịch có khối lượng lớn hơn so với lượng nước đã dùng là 2,66 gam. Đó là kim loại
A. Na
B. RB
C. K
D. Li
Hòa tan hoàn toàn 2,73 gam kim loại kiềm vào nước thu được một dung dịch có khối lượng lớn hơn so với lượng nước đã dùng là 2,66 gam. Đó là kim loại A. Na. B. RB C. K. D. Li
Đọc tiếp
Hòa tan hoàn toàn 2,73 gam kim loại kiềm vào nước thu được một dung dịch có khối lượng lớn hơn so với lượng nước đã dùng là 2,66 gam. Đó là kim loại
A. Na.
B. RB
C. K.
D. Li
Điện phân nóng chảy hoàn toàn 13,3 gam muối clorua của một kim loại kiềm thổ, thu được 3,136 lít khí (đktc) thoát ra ở anot. Hòa tan hoàn toàn lượng kim loại sinh ra vào dung dịch HNO3 2M (dùng dư 20% so với lượng cần thiết), khuấy đều cho các phản ứng xảy ra hoàn toàn thu được 0,448 lít khí A (đktc) và dung dịch X chứa 21,52 gam muối. Thể tích dung dịch HNO3 đã dùng là : A. 170 B. 120 C. 144 D. 204
Đọc tiếp
Điện phân nóng chảy hoàn toàn 13,3 gam muối clorua của một kim loại kiềm thổ, thu được 3,136 lít khí (đktc) thoát ra ở anot. Hòa tan hoàn toàn lượng kim loại sinh ra vào dung dịch HNO3 2M (dùng dư 20% so với lượng cần thiết), khuấy đều cho các phản ứng xảy ra hoàn toàn thu được 0,448 lít khí A (đktc) và dung dịch X chứa 21,52 gam muối. Thể tích dung dịch HNO3 đã dùng là :
A. 170
B. 120
C. 144
D. 204
Cho 10 gam hỗn hợp hai kim loại kiềm tan hoàn toàn vào 100ml
H
2
O
(
D
H
2
O
1
g
/
ml
) thu được dung dịch A...
Đọc tiếp
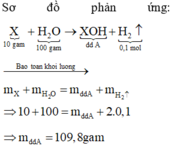
Cho 10 gam hỗn hợp hai kim loại kiềm tan hoàn toàn vào 100ml H 2 O ( D H 2 O = 1 g / ml ) thu được dung dịch A và 2,24 lít khí (đktc). Khối lượng dung dịch A là
A. 11,7 gam.
B. 109,8 gam.
C. 9,8 gam.
D. 110 gam.
Hòa tan hoàn toàn 25,8 gam kim loại kiềm A và oxit của nó vào nước dư thu được dung dịch B. Cô cạn dung dịch B thu được 33,6 g chất rắn khan. xác định kim loại kiềm A và khối lượng mỗi chất trong hỗn hợp
Gọi kim loại cần tìm là A
Công thức oxit là A2O
Đặt \(\left\{{}\begin{matrix}n_A=x\left(mol\right)\\n_{A_2O}=y\left(mol\right)\end{matrix}\right.\)
=> \(x.M_A+y\left(2.M_A+16\right)=25,8\)
=> \(x.M_A+2y.M_A+16y=25,8\) (1)
PTHH: 2A + 2H2O --> 2AOH + H2
A2O + H2O --> 2AOH
=> \(\left(x+2y\right)\left(M_A+17\right)=33,6\)
=> \(x.M_A+2y.M_A+17x+34y=33,6\) (2)
(2) - (1) = 17x + 18y = 7,8
=> \(x=\dfrac{7,8-18y}{17}\)
Do x > 0 => \(\dfrac{7,8-18y}{17}>0\Rightarrow0< y< \dfrac{13}{30}\) (3)
Thay vào (1) => 7,8.MA + 16y.MA + 272y = 25,8
=> \(M_A=\dfrac{571,2}{7,8+16y}-17\) (4)
(3)(4) => 21,77 < MA < 56,23
=> \(A\left[{}\begin{matrix}Natri\left(Na\right)\\Kali\left(K\right)\end{matrix}\right.\)
- Nếu A là Na:
=> 23x + 62y = 25,8
Và (x + 2y).40 = 33,6
=> x = 0,03; y = 0,405
\(\left\{{}\begin{matrix}m_{Na}=0,03.23=0,69\left(g\right)\\m_{Na_2O}=0,405.62=25,11\left(g\right)\end{matrix}\right.\)
- Nếu A là K
=> 39x + 94y = 25,8
Và (x + 2y).56 = 33,6
=> x = 0,3; y = 0,15
=> \(\left\{{}\begin{matrix}m_K=0,3.39=11,7\left(g\right)\\m_{K_2O}=0,15.94=14,1\left(g\right)\end{matrix}\right.\)
Đúng 6
Bình luận (1)
Hòa tan hoàn toàn a gam kim loại Ba vào nước thu được dung dịch A. Hấp thụ hoàn toàn 2,24 lít CO2 (đktc) vào dung dịch A thu được b gam kết tủa đồng thời thấy khối lượng dung dịch A giảm 7,42 gam so với ban đầu. Biết các phản ứng xảy ra hoàn toàn, giá trị của a và b lần lượt là A. 8,22 và 17,76 B. 10,96 và 15,76 C. 10,96 và 11,82 D. 8,22 và 11,82
Đọc tiếp
Hòa tan hoàn toàn a gam kim loại Ba vào nước thu được dung dịch A. Hấp thụ hoàn toàn 2,24 lít CO2 (đktc) vào dung dịch A thu được b gam kết tủa đồng thời thấy khối lượng dung dịch A giảm 7,42 gam so với ban đầu. Biết các phản ứng xảy ra hoàn toàn, giá trị của a và b lần lượt là
A. 8,22 và 17,76
B. 10,96 và 15,76
C. 10,96 và 11,82
D. 8,22 và 11,82
Hòa tan 6,85 gam một kim loại kiềm thổ M vào 100 gam nước thu được 100ml dung dịch A (d 1,0675 gam/ml). Đốt cháy 0,92 gam chất hữu cơ X thu được CO2 và 0,72 gam nước. Cho toàn bộ lượng CO2 thu được vào 100 ml dung dịch A trên, thu được 5,91 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, công thức phân tử của X là: A. C3H8O2 B. C7H8 C. C4H8O3 D. C6H6.
Đọc tiếp
Hòa tan 6,85 gam một kim loại kiềm thổ M vào 100 gam nước thu được 100ml dung dịch A (d = 1,0675 gam/ml). Đốt cháy 0,92 gam chất hữu cơ X thu được CO2 và 0,72 gam nước. Cho toàn bộ lượng CO2 thu được vào 100 ml dung dịch A trên, thu được 5,91 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, công thức phân tử của X là:
A. C3H8O2
B. C7H8
C. C4H8O3
D. C6H6.
Hòa tan 6,85 gam một kim loại kiềm thổ M vào 100 gam nước thu được 100 ml dung dịch A (d 1,0675 gam/ml). Đốt cháy 0,92 gam chất hữu cơ X thu được CO2 và 0,72 gam nước. Cho toàn bộ lượng CO2 thu được vào 100 ml dung dịch A trên, thu được 5,91 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, công thức phân tử của X là A. C3H8O2. B. C7H8. C. C4H8O3. D. C6H6
Đọc tiếp
Hòa tan 6,85 gam một kim loại kiềm thổ M vào 100 gam nước thu được 100 ml dung dịch A (d = 1,0675 gam/ml). Đốt cháy 0,92 gam chất hữu cơ X thu được CO2 và 0,72 gam nước. Cho toàn bộ lượng CO2 thu được vào 100 ml dung dịch A trên, thu được 5,91 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, công thức phân tử của X là
A. C3H8O2.
B. C7H8.
C. C4H8O3.
D. C6H6
Cho 5,05 gam hỗn hợp gồm kali và một kim loại kiềm khác tác dụng hết với nước. Để trung hoà hoàn toàn dung dịch thu được cần dùng hết 250 ml dung dịch
H
2
SO
4
0,3M. Biết rằng tỉ lệ về số mol của kim loại kiềm chưa biết và kali trong hỗn hợp lớn hơn
1
4
. Phần trăm khối lượng kali trong hỗn hợp là A, 22,6%. B. 38,6%. C. 77,2%. D. 96,5%.
Đọc tiếp
Cho 5,05 gam hỗn hợp gồm kali và một kim loại kiềm khác tác dụng hết với nước. Để trung hoà hoàn toàn dung dịch thu được cần dùng hết 250 ml dung dịch H 2 SO 4 0,3M. Biết rằng tỉ lệ về số mol của kim loại kiềm chưa biết và kali trong hỗn hợp lớn hơn 1 4 . Phần trăm khối lượng kali trong hỗn hợp là
A, 22,6%.
B. 38,6%.
C. 77,2%.
D. 96,5%.