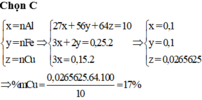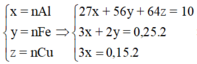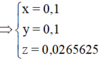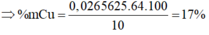Hỗn hợp X gồm Ba, Al, Fe . Chia hỗn hợp thành 3 phần bằng nhau.
-Phần 1: cho vào lượng dư nước thu được V lít khí hidro
-Phần 2 cho vào lượng dư dung dihcj NaOH thu được 1,6V lít khí hidro
-Phần 3 cho vào lượng dư dung dịch HCl thu được 2V lít khí hidro
Ccá thể tích khí cùng đo ở đktc và áp suất. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp.

Những câu hỏi liên quan
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau. - Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc). - Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,78; 0,54; 1,12 B. 0,39; 0,54; 1,40 C. 0,39; 0,54; 0,56 D. 0,78; 1,08; 0,56
Đọc tiếp
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.
- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc).
- Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc).
Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,78; 0,54; 1,12
B. 0,39; 0,54; 1,40
C. 0,39; 0,54; 0,56
D. 0,78; 1,08; 0,56
Chia hỗn hợp X gồm K, Al, Fe thành hai phần bằng nhau. Cho phần 1 vào dung dịch KOH dư thu được 0,784 lít khí H2 (đktc). Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl dư, thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,39; 0,54; 0,56 B. 0,39; 0,54; 1,40 C. 0,78; 1,08; 0,56. D. 0,78; 0,54; 1,12
Đọc tiếp
Chia hỗn hợp X gồm K, Al, Fe thành hai phần bằng nhau.
Cho phần 1 vào dung dịch KOH dư thu được 0,784 lít khí H2 (đktc).
Cho phần 2 vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl dư, thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,39; 0,54; 0,56
B. 0,39; 0,54; 1,40
C. 0,78; 1,08; 0,56.
D. 0,78; 0,54; 1,12
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí
H
2
(đktc).- Cho phần 2 vào một lượng dư
H
2
O
, thu được 0,448 lít khí
H
2
(đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí
H
2
(đktc). Tính khối lượng mỗi kim loại trong mỗi phần.
Đọc tiếp
Chia hỗn hợp X gồm K, Al và Fe thành hai phần bằng nhau.
- Cho phần 1 vào dung dịch KOH (dư) thu được 0,784 lít khí H 2 (đktc).
- Cho phần 2 vào một lượng dư H 2 O , thu được 0,448 lít khí H 2 (đktc) và m gam hỗn hợp kim loại Y. Hoà tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H 2 (đktc). Tính khối lượng mỗi kim loại trong mỗi phần.
Chia hỗn hợp X gồm K, AI và Fe thành hai phần bằng nhau. Cho phần một vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc). Cho phần hai vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc). Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là A. 0,39; 0,54; 1,40. B. 0,78; 0,54;1,12 C. 0,39; 0,54; 0,56 D. 0,78; 1,08;0,56
Đọc tiếp
Chia hỗn hợp X gồm K, AI và Fe thành hai phần bằng nhau.
Cho phần một vào dung dịch KOH (dư) thu được 0,784 lít khí H2 (đktc).
Cho phần hai vào một lượng dư H2O, thu được 0,448 lít khí H2 (đktc) và m gam hỗn hợp kim loại Y. Hòa tan hoàn toàn Y vào dung dịch HCl (dư) thu được 0,56 lít khí H2 (đktc).
Khối lượng (tính theo gam) của K, Al, Fe trong mỗi phần hỗn hợp X lần lượt là
A. 0,39; 0,54; 1,40.
B. 0,78; 0,54;1,12
C. 0,39; 0,54; 0,56
D. 0,78; 1,08;0,56
Chia m gam hỗn hợp X gồm Fe và Al thành hai phần bằng nhau. Biết các khí đều đo ở điều kiện tiêu chuẩn. Tính m. - Cho phần hai vào dung dịch NaOH dư, thu được 10,08 lít khí Hạ. - Cho phần một vào một lượng dư dung dịch HCl, thu được 13,44 lít khí H2.
Phần hai :
$2NaOH+ 2Al + 2H_2O \to 2NaAlO_2 + 3H_2$
$n_{H_2} = \dfrac{10,08}{22,4} = 0,45(mol)$
Theo PTHH : $n_{Al} = \dfrac{2}{3}n_{H_2} = 0,3(ol)$
Phần một :
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$Fe + 2HCl \to FeCl_2 + H_2$
$n_{H_2} = \dfrac{13,44}{22,4} = 0,6(mol)$
Theo PTHH : $n_{H_2} = \dfrac{3}{2}n_{Al} + n_{Fe}$
$\Rightarrow n_{Fe} = 0,15(mol)$
$\Rightarrow m = 2(0,3.27 + 0,15.56) = 33(gam)$
Đúng 2
Bình luận (0)
Chia 20 gam hỗn hợp X gồm Al, Fe, Cu thành hai phần bằng nhau. Phần 1 cho tác dụng với dung dịch HCl đặc, dư thu được 5,6 lít khí (đktc). Phần 2 cho tác dụng với dung dịch NaOH dư thu được 3,36 lít khí (đktc). Phần trăm khối lượng Cu có trong hỗn hợp là A. 8,5%. B. 13,5%. C. 17%. D. 28%.
Đọc tiếp
Chia 20 gam hỗn hợp X gồm Al, Fe, Cu thành hai phần bằng nhau. Phần 1 cho tác dụng với dung dịch HCl đặc, dư thu được 5,6 lít khí (đktc). Phần 2 cho tác dụng với dung dịch NaOH dư thu được 3,36 lít khí (đktc). Phần trăm khối lượng Cu có trong hỗn hợp là
A. 8,5%.
B. 13,5%.
C. 17%.
D. 28%.
Chia 20 gam hỗn hợp X gồm Al, Fe, Cu thành hai phần bằng nhau. Phần 1 cho tác dụng với dung dịch HCl đặc, dư thu được 5,6 lít khí (đktc). Phần 2 cho tác dụng với dung dịch NaOH dư thu được 3,36 lít khí (đktc). Phần trăm khối lượng Cu có trong hỗn hợp là
A. 8,5%.
B. 13,5%.
C. 17%.
D. 28%.
Hỗn hợp X gồm Al , fe và Cu. chia a gam X thành 3 phần bằng nhau
- Phần 1 cho tác dụng vào lượng dư dung dịch HCl thì thu được 5,6 lit khí H2
- phần 2 hòa tan hoàn toàn bằng lượng dư dung dịch H2SO4 đặc đun nóng thì thu được 7,84 lít khí SO2 (sản phẩm khử duy nhất) ,dung dịch y và chất rắn Z. Cho y tác dụng với lượng dư dung dịch NaOH thu được kết tủa T. Lọc lấy T đem nung trong không khí đến khối lượng không đổi thì thu được 12 g rắn G
- phần 3 đốt cháy trong bình có chứa lượng dư khí Clo thu...
Đọc tiếp
Hỗn hợp X gồm Al , fe và Cu. chia a gam X thành 3 phần bằng nhau - Phần 1 cho tác dụng vào lượng dư dung dịch HCl thì thu được 5,6 lit khí H2 - phần 2 hòa tan hoàn toàn bằng lượng dư dung dịch H2SO4 đặc đun nóng thì thu được 7,84 lít khí SO2 (sản phẩm khử duy nhất) ,dung dịch y và chất rắn Z. Cho y tác dụng với lượng dư dung dịch NaOH thu được kết tủa T. Lọc lấy T đem nung trong không khí đến khối lượng không đổi thì thu được 12 g rắn G - phần 3 đốt cháy trong bình có chứa lượng dư khí Clo thu được b gam chất rắn E biết các phản ứng xảy ra hoàn toàn. Tính giá trị của a và b Làm hộ em với ạ!!!。゚( ゚^∀^゚)゚。
Câu 1. Chia m gam hỗn hợp X gồm Na và Al thành hai phần bằng nhau.
- Cho phần một vào một lượng dư H2O, thu được 0,672 lít khí H2.
- Cho phần hai vào dung dịch NaOH dư, thu được 1,176 lít khí H2.
Biết các khí đều đo ở điều kiện tiêu chuẩn. Tính m.
Câu 2. Viết phương trình hoá học các phản ứng trong sơ đồ chuyển hoá sau:
1/ K + HCl --
2/ KOH + MgSO4 --
3/ KHCO3 –to --
4/ K2CO3 +...
Đọc tiếp
Câu 1. Chia m gam hỗn hợp X gồm Na và Al thành hai phần bằng nhau.
- Cho phần một vào một lượng dư H2O, thu được 0,672 lít khí H2.
- Cho phần hai vào dung dịch NaOH dư, thu được 1,176 lít khí H2.
Biết các khí đều đo ở điều kiện tiêu chuẩn. Tính m.
Câu 2. Viết phương trình hoá học các phản ứng trong sơ đồ chuyển hoá sau:
1/ K + HCl -->
2/ KOH + MgSO4 -->
3/ KHCO3 –to -->
4/ K2CO3 + HCl -->
Câu 3. Viết phương trình hóa học các phản ứng trong sơ đồ chuyển hóa sau:
X ® Al2O3 ® Y ® X ® NaAlO2 ® X
Hỗn hợp X gồm 2 kim loại Na và Al. Chia hỗn hợp X làm hai phần bằng nhau. Cho phần một vào nước dư, thu được V lít khí. Cho phần hai vào dung dịch NaOH dư, được 1,45V lít khí. Các khí đo cùng điều kiện nhiệt độ, áp suất. Tỉ lệ mol của hai kim loại trong X là
A. 5:8.
B. 3:5.
C. 3:7.
D. 1:2.
Giải thích:
Gọi số mol của Na và Al trong mỗi phần lần lượt là x và y mol
Nhận xét: Vì hai phần lượng khí H2 thu được chênh lệch nhau và phần 2 nhiều hơn phần 1 => ở phần 1 nhôm phản ứng dư. Mọi tính toán theo số mol của Na
Phần 1:
Na + H2O → NaOH + 0,5H2↑
x →x →0,5x (mol)
Al + NaOH + H2O → NaAlO2 + H2↑
x → 1,5x (mol)
Phần 2:
Na + H2O → NaOH + 0,5H2↑
x →x →0,5x (mol)
Al + NaOH dư + H2O → NaAlO2 + 1,5H2↑
y → 1,5y
Ta có: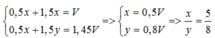
Đáp án A
Đúng 0
Bình luận (0)