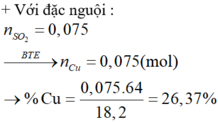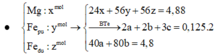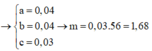cho 4,64 gam hỗn hợp X gồm Cu,Fe tác dụng hoàn toàn với dung dịch H2SO4 đặc nóng, dư , sau phản ứng thu được dung dịch Y và 2,464 lít khí SO2 do (đktc). tính khối lượng mỗi kim loại có trong hỗn hợp X

Những câu hỏi liên quan
Cho 12 gam hỗn hợp gồm Cu và Fe tác dụng hoàn toàn với dung dịch H2SO4 đặc, nóng dư thu được 5,6 lít khí SO2 đktc ?a. Viết phương trình phản ứng xảy ra ?b. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp đầu ?c. Tính khối lượng muối thu được sau phản ứng ?d. Tính thể tích H2SO4 2M cần dùng ?
Đọc tiếp
Cho 12 gam hỗn hợp gồm Cu và Fe tác dụng hoàn toàn với dung dịch H2SO4 đặc, nóng dư thu được 5,6 lít khí SO2 đktc ?
a. Viết phương trình phản ứng xảy ra ?
b. Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp đầu ?
c. Tính khối lượng muối thu được sau phản ứng ?
d. Tính thể tích H2SO4 2M cần dùng ?
a)
$Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + H_2O$
$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
b) n Cu =a (mol) ; n Fe = b(mol)
=> 64a + 56b = 12(1)
n SO2 = a + 1,5b = 5,6/22,4 = 0,25(2)
(1)(2) suy ra a = b = 0,1
%m Cu = 0,1.64/12 .100% = 53,33%
%m Fe = 100% -53,33% = 46,67%
c)
n CuSO4 = a = 0,1(mol)
n Fe2(SO4)3 = 0,5a = 0,05(mol)
m muối = 0,1.160 + 0,05.400 = 36(gam)
d) n H2SO4 = 2n SO2 = 0,5(mol)
V H2SO4 = 0,5/2 = 0,25(lít)
Đúng 2
Bình luận (1)
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37%. B. 48,21% và 9,23%. C. 42,86% va 48,21%. D. 48,21% và 42,56%.
Đọc tiếp
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%.
B. 48,21% và 9,23%.
C. 42,86% va 48,21%.
D. 48,21% và 42,56%.
Xét thí nghiệm 2: chú ý tính thụ động hóa của kim loại:
H2SO4 đặc, nguội không phản ứng với Al, Cr, Fe!
⇒ trong X chỉ có Cu phran ứng. Bảo toàn electron: n Cu = n SO 2 = 0 , 075 mol.
Đặt n Cr = x mol; n Fe = y mol → m X 52x + 56y + 0,075 × 64 = 18,2 gam.
x + y = 0,25 mol. Giải hệ có: x = 0,15 mol; y = 0,1 mol.
mCr trong X = 42,86% và %mCu trong X = 26,37%
Đáp án A
Đúng 0
Bình luận (0)
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37%. B. 48,21% và 9,23%. C. 42,86% va 48,21%. D. 48,21% và 42,56%.
Đọc tiếp
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%.
B. 48,21% và 9,23%.
C. 42,86% va 48,21%.
D. 48,21% và 42,56%.
Chọn đáp án A
Xét thí nghiệm 2: chú ý tính thụ động hóa của kim loại:
H2SO4 đặc, nguội không phản ứng với Al, Cr, Fe!
⇒ trong X chỉ có Cu phran ứng. Bảo toàn electron: n C u = n S O 2 = 0 , 075 m o l
Đặt nCr = x mol; nFe = y mol ⇒ m X = 52x + 56y + 0,075 × 64 = 18,2 gam.
nH2 = x + y = 0,25 mol. Giải hệ có: x = 0,15 mol; y = 0,1 mol.
⇒ % mCr trong X = 42,86% và %mCu trong X = 26,37%
Đúng 0
Bình luận (0)
Cho 12,8 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 l loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, Chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37% B. 42,86% và 48,21% C. 48,21% và 42,56% D. 48,21% và 9,23%
Đọc tiếp
Cho 12,8 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 l loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, Chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%
B. 42,86% và 48,21%
C. 48,21% và 42,56%
D. 48,21% và 9,23%
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là: A. 13,8;7,6;11,8 B. 11,8;9,6;11,8 C. 12,8;9,6;10,8 D. kết quả khác
Đọc tiếp
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là:
A. 13,8;7,6;11,8
B. 11,8;9,6;11,8
C. 12,8;9,6;10,8
D. kết quả khác
Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)
Đúng 0
Bình luận (0)
Cho 17,2 gam hỗn hợp kim loại gồm Fe cà Cu tác dụng vừa đủ với dd H2SO4 đặc nóng dư thu được 6,72 lít khí SO2 (đktc) là sản phẩm khử duy nhất. Tính khối lượng mỗi muối và khối lượng dung dịch H2SO4 80% phản ứng
`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2(SO_4)_3 + 3SO_2 \uparrow + 6H_2 O`
`0,05` `0,15` `0,025` `(mol)`
`Cu + 2H_2 SO_[4(đ,n)] -> CuSO_4 + SO_2 \uparrow + 2H_2 O`
`0,225` `0,45` `0,225` `(mol)`
`n_[SO_2]=[6,72]/[22,4]=0,3(mol)`
Gọi `n_[Fe]=x` ; `n_[Cu]=y`
`=>` $\begin{cases} \dfrac{3}{2}x+y=0,3\\56x+64y=17,2 \end{cases}$
`<=>` $\begin{cases}x=0,05\\y=0,225 \end{cases}$
`@m_[Fe_2(SO_4)_3]=0,025.400=10(g)`
`@m_[CuSO_4]=0,225.160=36(g)`
`@m_[dd H_2 SO_4]=[(0,15+0,45).98]/80 .100=73,5(g)`
Đúng 4
Bình luận (0)
Sửa đề: 80% ---> 98% (80% chưa đặc nên không giải phóng SO2 được)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(\rightarrow56a+64b=17,2\left(1\right)\)
PTHH:
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
a------>3a------------------->0,5a--------------->1,5a
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
b----->2b------------------->b------------->b
\(\rightarrow1,5a+b=\dfrac{6,72}{22,4}=0,3\left(2\right)\)
Từ \(\left(1\right)\left(2\right)\rightarrow\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,225\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe_2\left(SO_4\right)_3}=0,5.0,05.400=10\left(g\right)\\m_{CuSO_4}=0,225.160=36\left(g\right)\\m_{ddH_2SO_4}=\dfrac{\left(0,05.3+0,225.2\right).98}{98\%}=60\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Hoà tan hoàn toàn 16,2g hỗn hợp X gồm Cu và Fe bằng lượng dư dung dịch h2so4 đặc nóng thu được dung dịch Y và 8,96 lít khí so2 ( sản phẩm khử duy nhất,đo ở đktc)
a. Tính % theo khối lượng mỗi kim loại trong hỗn hợp X
b. Nếu đem 22g hỗn hợp X nói trên cho tác dụng với lượng dư dung dịch h2so4 loãng thì thể tích khí thu được (đo ở đktc) là bao nhiêu lít ( giả sử hỗn hợp X được trộn đều)
Giúp vs ạ
Đọc tiếp
Hoà tan hoàn toàn 16,2g hỗn hợp X gồm Cu và Fe bằng lượng dư dung dịch h2so4 đặc nóng thu được dung dịch Y và 8,96 lít khí so2 ( sản phẩm khử duy nhất,đo ở đktc) a. Tính % theo khối lượng mỗi kim loại trong hỗn hợp X b. Nếu đem 22g hỗn hợp X nói trên cho tác dụng với lượng dư dung dịch h2so4 loãng thì thể tích khí thu được (đo ở đktc) là bao nhiêu lít ( giả sử hỗn hợp X được trộn đều) Giúp vs ạ
\(n_{Cu}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m_X=64a+56b=16.2\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
Bảo toàn e :
\(2a+3b=0.4\cdot2=0.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.0475,b=0.235\)
\(\%Cu=\dfrac{0.0475\cdot64}{16.2}\cdot100\%=18.76\%\)
\(\%Fe=81.24\%\)
\(b.\)
\(\dfrac{a}{b}=\dfrac{0.0475}{0.235}=\dfrac{19}{94}\)
\(\Rightarrow n_{Cu}=19x\left(mol\right),n_{Fe}=94x\left(mol\right)\)
\(m_X=19x\cdot64+94x\cdot56=22\left(g\right)\)
\(\Rightarrow x=\dfrac{11}{3240}\)
\(n_{H_2}=n_{Fe}=\dfrac{11}{3240}\cdot94=\dfrac{517}{1620}\left(mol\right)\)
\(V_{H_2}=7.15\left(l\right)\)
Đúng 1
Bình luận (0)
Cho 4,88 gam hỗn hợp Mg và Fe vào dung dịch gồm AgNO3 và Cu(NO3)2, thu được chất rắn X gồm ba kim loại và dung dịch Y gồm hai muối. Đun nóng X với dung dịch H2SO4 đặc, dư thu được 2,8 lít khí SO2 (đktc). Cho dung dịch NaOH dư vào Y, lọc lấy kết tủa rồi nung trong không khí, thu được 4,8 gam oxit. Giả thiết các phản ứng xảy ra hoàn toàn. Khối lượng của Fe trong X là: A. 1,68 gam. B. 2,80 gam. C. 1,12 gam. D. 2,24 gam.
Đọc tiếp
Cho 4,88 gam hỗn hợp Mg và Fe vào dung dịch gồm AgNO3 và Cu(NO3)2, thu được chất rắn X gồm ba kim loại và dung dịch Y gồm hai muối. Đun nóng X với dung dịch H2SO4 đặc, dư thu được 2,8 lít khí SO2 (đktc). Cho dung dịch NaOH dư vào Y, lọc lấy kết tủa rồi nung trong không khí, thu được 4,8 gam oxit. Giả thiết các phản ứng xảy ra hoàn toàn. Khối lượng của Fe trong X là:
A. 1,68 gam.
B. 2,80 gam.
C. 1,12 gam.
D. 2,24 gam.
Cho 21,6 gam hỗn hợp X gồm Fe và MgSO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, sau phản ứng thu được 6,72 l hỗn hợp khí (đktc)a) Xác định khối lượng các chất trong Xb) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính Vc) Tính số mol KOH tối thiểu để hấp thụ hết V lít SO2 trênd) Cho 0,03 mol Ba(OH)2 tác dụng hoàn toàn với 0,1 V lít SO2 trên. Tính khối lượng kết tủa thu được
Đọc tiếp
Cho 21,6 gam hỗn hợp X gồm Fe và MgSO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, sau phản ứng thu được 6,72 l hỗn hợp khí (đktc)
a) Xác định khối lượng các chất trong X
b) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính V
c) Tính số mol KOH tối thiểu để hấp thụ hết V lít SO2 trên
d) Cho 0,03 mol Ba(OH)2 tác dụng hoàn toàn với 0,1 V lít SO2 trên. Tính khối lượng kết tủa thu được
Cho 30,4 gam hỗn hợp Fe, FeO Fe2O3 tác dụng với dung dịch H2SO4 đặc, nóng dư. Sau phản ứng thu được 2,24 lít khí SO2 (đktc) và dung dịch X . Tính khối lượng muối có trong dung dịch X
$n_{SO_2}=\dfrac{2,24}{22,4}=0,1(mol)$
Quy hỗn hợp về $Fe:x(mol),O:y(mol)$
$\to 56x+16y=30,4(1)$
Bảo toàn e: $3n_{Fe}=2n_O+2n_{SO_2}$
$\to 3x=2y+0,2(2)$
Từ $(1)(2)\to x=0,4(mol);y=0,5(mol)$
Bảo toàn Fe: $n_{Fe_2(SO_4)_3}=0,5x=0,2(mol)$
$\to m_X=0,2.400=80(g)$
Đúng 1
Bình luận (1)