để chuẩn bị cho buổi thực hành chúng ta cần 4,8 lít khí O2 ( ở đktc)
a) Hãy tính số gam KMnO4 cần dùng để điều chế được lượng oxi trên? biết hiệu suất phản ứng phân hủy là 80%
giúp tớ với,help me!
Tính khối lượng KMnO4 cần dùng để điều chế được lượng oxi là 11,2 lít , biết hiệu suất phản ứng phân hủy đạt 80% (các chất khí đo ở đktc)
\(n_{O_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
1<------------------------------------0,5
=> \(m_{KMnO_4\left(pthh\right)}=1.158=158\left(g\right)\)
=> \(m_{KMnO_4\left(tt\right)}=\dfrac{158.100}{80}=197,5\left(g\right)\)
Bài 4. Nung nóng KMnO4 để điều chế 6,72 lít O2 (ở đktc).
a. Tính khối lượng thuốc tím cần dùng?
b. Cần dùng bao nhiêu gam KClO3 để điều chế cũng với một thể tích khí O2 trên?
c. Nếu cho lượng khí O2 trên tác dụng hết với Cu. Hỏi sau phản ứng thu được bao nhiêu gam đồng (II) oxit.
Bài 5. Cho 16 gam đồng (II) oxit phản ứng hết V lít khí hidro H2 (đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Cu và H2O. Biết phản ứng xảy ra vừa đủ. a/ Tính giá trị V./ b/ Tính khối lượng Cu thu được sau phản ứng.
Bài 6. Cho11,6 gam oxit sắt từ Fe3O4 phản ứng hết V lít khí hidro H2 (đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Fe và H2O. Biết phản ứng xảy ra vừa đủ. a/ Tính giá trị V. b/ Tính khối lượng Fe thu được sau phản ứng.
Bài 7. Người ta dùng H2 (dư) tác dụng hết với x gam Fe2O3 nung nóng thu được y gam Fe. Cho lượng sắt này tác dụng với dung dịch H2SO4 loãng dư thì thu được 6,72 lít khí H2 (đktc). Tính giá trị x và y.
Bài 8. Cho 3,6 gam magie phản ứng hoàn toàn với dung dịch axit sunfuric loãng (H2SO4)
a.Viết phương trình phản ứng xảy ra và tính thể tích hidro thu được ở đktc.
b. Cho lượng khí H2 thu được tác dụng hết với CuO. Hỏi sau phản ứng thu được bao nhiêu gam Cu?
Bài 9. Cho 3,6 gam magie trên vào dung dịch chứa 14,6 gam axit clohidric (HCl)a. Hỏi sau phản ứng chất nào còn dư, dư bao nhiêu gam?b. Tính thể tích H2 (đktc)?
Bài 4. 2\(KMnO_4\) ---> \(K_2MnO_4\) + \(MnO_2\) + \(O_2\) (Lập và cân bằng phương trình)
0,6 mol 0,3 mol 0,3 mol 0,3 mol
a. + Số mol của \(O_2\)
\(n_{O_2}\) = \(\dfrac{V}{22,4}\) = \(\dfrac{6,72}{22,4}\) = 0,3 (mol)
+ Khối lượng của \(KMnO_4\) (thuốc tím) cần dùng:
\(m_{KMnO_4}\) = n . M = 0,6 . 158 = 94,8 (g)
b. 2\(KClO_3\) ---> 2\(KCl\) + 3\(O_2\) (Lập và cân bằng phương trình)
0,2 mol 0,2 mol 0,3 mol
Số g \(KClO_3\) dùng để điều chế:
\(m_{KClO_3}\) = n . M = 0,2 . 122,5 = 24,5 (g)
c. 2Cu + \(O_2\) ---> 2\(CuO\) (Lập và cân bằng phương trình)
0,6 mol 0,3 mol 0,6 mol
Số g của CuO sau phản ứng thu được:
\(m_{CuO}\) = n . M = 0,6 . 80 = 48 (g)
________________________________________
Bài 4 trước nha bạn, có gì sai thì nhắn mình :))
Bài 5. CuO + \(H_2\) ---> Cu + \(H_2O\) (Lập và cân bằng phương trình)
0,2 mol 0,2 mol 0,2 mol 0,2 mol
a. + Số mol của CuO:
\(n_{CuO}\) = \(\dfrac{m}{M}\) = \(\dfrac{16}{80}\) = 0,2 (mol)
+ Thể tích của \(H_2\)
\(V_{H_2}\) = n . 22,4 = 0,2 . 22,4 = 4,48 (lít)
b. Khối lượng Cu sau phản ứng:
\(m_{Cu}\) = n . M = 0,2 . 64 = 12,8 (g)
______________________________
Bài 5 nha, sai thì nhắn mình :))
Bài 6. \(Fe_3O_4\) + 4\(H_2\) ---> 3Fe + 4\(H_2O\) (Lập và cân bằng phương trình)
0,05 mol 0,2 mol 0,15 mol 0,2 mol
a. + Số mol của \(Fe_3O_4\)
\(n_{Fe_3O_4}\) = \(\dfrac{m}{M}\) = \(\dfrac{11,6}{232}\) = 0,05 (mol)
+ Thể tích của \(H_2\)
\(V_{H_2}\) = n . 22,4 = 0,2 . 22,4 = 4,48 (lít)
b. Khối lượng của Fe thu được sau phản ứng:
\(m_{Fe}\) = n . M = 0,15 . 56 = 8,4 (g)
_________________________________________
Bài 6 này :))
Trong phòng thí nghiệm, người ta điều chế Fe3O4 bằng cách dùng oxi để oxi hoá sắt ở nhiệt độ cao.
a/ Tính thể tích O2 ở ĐKTC cần dùng để điều chế được 2,32g Fe3O4.
b/ Tính số gam kalipemanganat KMnO4 cần dùng để có được lượng O2 dùng cho phản ứng trên.
PTHH: 3Fe + \(2O_2\) --->\(Fe_3O_4\)
theo pt: 3_____2_____________1
theo đề: x______y_____________0.01
nFe3O4 là: 0.01mol
\Rightarrow nO2= 0.01*2/1=0.02 mol
VO2= 0.02*22.4=0.448l
b, PTHH : 2KMnO4 ----> K2MnO4 + MnO2 + O2
theo pt: 2__________1________1______1
theo đề: x___________________________0.02
=> n KMnO4= 0.02*2/1= 0.04 mol
=>mKMnO4= 0.04*158=6.32g
a. số mol của là :
2.32 : 232 =0.01 mol
theo tỉ lệ mol ta có số mol của Fe là:
0.01 * 3 = 0.03 mol
khối lượng sắt là: 0.03*56=1.68g
số mol oxi là: 0.01*2=0.02mol
thể tích oxi là: 0.02*22.4= 0.448g
b. 2KMnO_4 ---> K2MnO4 + MnO2 + O2
---> nKMnO_4 = 2nO2 = 0,04 mol ---> mKMnO_4=0.04*158=6.32g
a, nFe3O4 = \(\dfrac{m}{M}\)= \(\dfrac{2,32}{232}\)=0,01(mol)
pt: 3Fe + 2O2 --to-> Fe3O4 (1)
Từ pứ (1) => \(n_{Fe}=3.n_{Fe3O4}=3.0,01=0,03\left(mol\right)\)
=> mFe= n.M=0,03.56=1,68(g)
Từ pứ (1)=> \(n_{^{O2}}=2.n_{^{Fe3O4}}=2.0,01=0,02\)
=>mO2=n.M=0,02.32=0,64(g)
Vậy cần 1,68g Fe và 0,64g O2 để điều chế 2,32g oxits sắt từ
Nung nóng ( kali nitrat )KNO3 tạo thành KNO2 ( Kali nitrit) và khí O2 a) Viết PTHH cho biết thuộc loại phản ứng nào. b) Tính lượng KNO3 cần dùng để điều chế được 1,68 lít O2 ở đktc biết H = 85% c) Tính VO2 ở đktc điều chế được khi phân hủy 10,1 gam KNO3 biết H = 80%
a) \(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
Phản ứng phân hủy
b) \(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
PTHH: 2KNO3 --to--> 2KNO2 + O2
0,15<--------------------0,075
=> \(m_{KNO_3\left(PTHH\right)}=0,15.101=15,15\left(g\right)\)
=> mKNO3 (thực tế) = \(\dfrac{15,15.100}{85}=17,824\left(g\right)\)
c) \(n_{KNO_3\left(pư\right)}=\dfrac{10,1.80\%}{101}=0,08\left(mol\right)\)
=> nO2 = 0,04 (mol)
=> VO2 = 0,04.22,4 = 0,896(l)
Trong phòng thí nghiệm, người ta thường dùng muối KN O 3 để điều chế khí oxi bằng phản ứng phân hủy. Để điều chế 1,12 lít khí O 2 (đktc) thì khối lượng muối cần dùng là
A. 20,2 gam
B. 10,1 gam
C. 5,05 gam
D. 7,07 gam
để điều chế được 6,72 lít khí oxi cần phân hủy bao nhiêu gam KMnO4 biết hiệu suất phân hủy là 90%
2KMnO4-to>K2MnO4+MnO2+O2
0,6------------------------------------0,3 mol
n O2=\(\dfrac{6,72}{22,4}\)=0,3 mol
=>m KMnO4pứ=0,6.158.\(\dfrac{100}{90}\)=105,33g
Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
a) Phương trình hóa học của phản ứng:
3Fe + 2O2 → Fe3O4.
nFe3O4 = 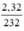 = 0,01 mol.
= 0,01 mol.
nFe = 3.nFe3O4 = 0,01 .3 = 0,03 mol.
nO2 = 2.nFe3O4 = 0,01 .2 = 0,02 mol.
mFe = 0,03.56 = 1,68g.
mO2 = 0,02.32 = 0,64g.
b) Phương trình phản ứng nhiệt phân KMnO4:
2KMnO4 → K2MnO4 + MnO2 + O2
nKMnO4 = 2.nO2 = 0,02.2 = 0,04 mol.
mKMnO4 = 0,04 .158 = 6,32g.
cho cacbon tác dụng với 33,6 lít khí oxi(đktc)
a,hãy tính khối lượng của cacbon đã phản ứng
b, tính khối lượng của KMnO4 cần dùng để phân hủy tạo ra lượng oxi trong phản ứng trên
a)\(n_{O_2}=\dfrac{33,6}{22,4}=1,5\left(m\right)\)
\(PTHH:C+O_2\xrightarrow[]{}CO_2\)
tỉ lệ :1 1 1(mol)
số mol :1,5 1,5 1,5
\(m_C=1,5.12=18\left(g\right)\)
b)\(PTHH:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
tỉ lệ :2 1 1 1(mol)
số mol :3 1,5 1,5 1,5
\(m_{KMnO_4}=3.158=474\left(g\right)\)
Để chuẩn bị cho thực hành cần cho 10 lọ khí oxi.Mỗi lọ có dung tích 112ml. a)giả sử điều chế khí oxi bằng KMnO4 tính khối lượng KMnO4 phải dùng biết oxi thu dcj ở ĐKTC là hao hụt 20 phần trăm . b)vẫn dcj khí oxi như trên đem oxinhoas hết sắt thì khối lượng oxi thu dcj là bao nhiêu
C1: trong phòng thí nghiệm, ng ta điều chế oxi bằng cách phân hủy hoàn toàn 15.8g KMnO4 a) Viết Phương trình phản ứng B) tính thể tích oxi điều chế đc(đktc)? C) tính khối lượng sắt cần dùng để phản ứng hết vs thể tích khí oxi thu đc hết ở trên
a) $2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
b) n KMnO4 = 15,8/158 = 0,1(mol)
Theo PTHH : n O2 = 1/2 n KMnO4 = 0,05(mol)
=> V O2 = 0,05.22,4 = 1,12(lít)
c)
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
Theo PTHH : n Fe = 3/2 nO2 = 0,075(mol)
=> m Fe = 0,075.56 = 4,2(gam)
Theo gt ta có: $n_{KMnO_4}=0,1(mol)$
a, $2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2$
b, Ta có: $n_{O_2}=0,05(mol)\Rightarrow V_{O_2}=1,12(mol)$
c, $3Fe+2O_2\rightarrow Fe_3O_4$
Ta có: $n_{Fe}=0,075(mol)\Rightarrow m_{Fe}=4,2(g)$