Cho 0.336 lít khí SO2 (đktc) vào 1 lít dung dịch Ca(OH)2 0,01M thu được , gam kết tủa. Tìm m?

Những câu hỏi liên quan
Cho 0.336 lít khí CO2 (đktc) vào 1 lít dung dịch Ca(OH)2 0,01M thu được , gam kết tủa. Tìm m?
\(n_{CO_2}=\dfrac{0,336}{22,4}=0,015\left(mol\right)\\ n_{Ca\left(OH\right)_2}=1.0,01=0,01\left(mol\right)\)
Xét \(T=\dfrac{0,01}{0,015}=\dfrac{2}{3}\) => Tạo cả 2 muối \(CaCO_3,Ca\left(HCO_3\right)_2\)
PTHH: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,01-------->0,01--->0,01
\(\rightarrow n_{CO_2\left(dư\right)}=0,015-0,01=0,005\left(mol\right)\)
PTHH: \(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
0,005<--0,005
\(\rightarrow m=\left(0,01-0,005\right).100=0,5\left(g\right)\)
Đúng 5
Bình luận (4)
Cho 8,96 lít khí SO2 ở điều kiện tiêu chuẩn vào cho 8,96 lít khí SO2 ở đktc vào V lít dung dịch Ca(OH)2 0,05 M thu được 12 gam kết tủa . Tính V
\(n_{CaSO_3}=\dfrac{12}{120}=0,1\left(mol\right)\)
\(n_{SO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)>n_{CaSO_3}=0,1\left(mol\right)\)
=> Kết tủa bị hòa tan 1 phần
Gọi số mol Ca(OH)2 là x (mol)
PTHH: Ca(OH)2 + SO2 --> CaSO3 + H2O
x-------->x-------->x
CaSO3 + SO2 + H2O --> Ca(HSO3)2
(x-0,1)-->(x-0,1)
=> x + (x-0,1) = 0,4
=> x = 0,25
=> \(V=\dfrac{0,25}{0,05}=5\left(l\right)\)
Đúng 4
Bình luận (0)
Cho V lít khí CO2 (đktc) hấp thụ hoàn toàn vào 3 lít dung dịch Ca(OH)2 0,01M thu được 1,5 gam kết tủa. Giá trị của V là A. 0,336. B. 2,016. C. 0,336 hoặc 2,016. D. 0,336 hoặc 1,008.
Đọc tiếp
Cho V lít khí CO2 (đktc) hấp thụ hoàn toàn vào 3 lít dung dịch Ca(OH)2 0,01M thu được 1,5 gam kết tủa. Giá trị của V là
A. 0,336.
B. 2,016.
C. 0,336 hoặc 2,016.
D. 0,336 hoặc 1,008.
Cho V lít khí CO2 (đktc) hấp thụ hoàn toàn vào 4 lít dung dịch Ba(OH)2 0,01M thu được 2,955 gam kết tủa. Giá trị của V là A. 0,336. B. 0,672. C. 0,336 hoặc 1,456. D. 0,672 hoặc 2,912
Đọc tiếp
Cho V lít khí CO2 (đktc) hấp thụ hoàn toàn vào 4 lít dung dịch Ba(OH)2 0,01M thu được 2,955 gam kết tủa. Giá trị của V là
A. 0,336.
B. 0,672.
C. 0,336 hoặc 1,456.
D. 0,672 hoặc 2,912
Hấp thụ hoàn toàn 8,96 lít khí SO2 ( đktc ) vào 500 ml dung dịch Ca(OH)2 aM thu được 24 gam kết tủa. Tính a ?
n SO2 = 8,96/22,4 = 0,4(mol)
n CaSO3 = 24/120 = 0,2(mol) < SO2 = 0,4 nên kết tủa bị hòa tan một phần
SO2 + Ca(OH)2 → CaSO3 + H2O
0,2.........0,2...............0,2.......................(mol)
2SO2 + Ca(OH)2 → Ca(HSO3)2
0,2............0,1........................................(mol)
=> n Ca(OH)2 = 0,2 + 0,1 = 0,3(mol)
=> a = 0,3/0,5 = 0,6(M)
Đúng 1
Bình luận (0)
Hấp thụ hết V lít CO2 (đktc) vào dung dịch chứa 500 ml dung dịch Ca(OH)2 0,01M, thu được 2 gam kết tủa. Tính giá trị của V.
Sửa đề : 500 ml dung dịch Ca(OH)2 0,1M . Nếu là 0,01M thì đề sai
\(n_{Ca\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{2}{100}=0,02\left(mol\right)\)
Bảo toàn nguyên tố Ca : \(n_{Ca\left(OH\right)_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}\)
=> \(n_{Ca\left(HCO_3\right)_2}=0,05-0,02=0,03\left(mol\right)\)
Bảo toàn nguyên tố C :
=> \(n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}=0,02+0,03.2=0,08\left(mol\right)\)
=> \(V_{CO_2}=0,08.22,4=1,792\left(l\right)\)
Đúng 2
Bình luận (0)
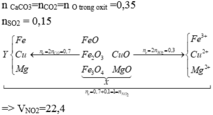
Cho m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO và Fe3O4 vào dung dịch H2SO4 đặc nóng thu được 3,36 lít khí SO2 (đktc). Mặt khác nung m gam hỗn hợp X với khí CO dư thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư thu được 35 gam kết tủa. Cho chất rắn Y vào dung dịch HNO3 đặc, nóng, dư thu được V lít khí NO2 (đktc) là sản phẩm khử duy nhất. Giá trị của V là A. 11,2. B. 22,4. C. 44,8. D. 33,6.
Đọc tiếp
Cho m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO và Fe3O4 vào dung dịch H2SO4 đặc nóng thu được 3,36 lít khí SO2 (đktc). Mặt khác nung m gam hỗn hợp X với khí CO dư thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư thu được 35 gam kết tủa. Cho chất rắn Y vào dung dịch HNO3 đặc, nóng, dư thu được V lít khí NO2 (đktc) là sản phẩm khử duy nhất. Giá trị của V là
A. 11,2.
B. 22,4.
C. 44,8.
D. 33,6.
Cho m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO và Fe3O4 vào dung dịch H2SO4 đặc nóng thu được 3,36 lít khí SO2 (đktc). Mặt khác nung m gam hỗn hợp X với khí CO dư thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư thu được 35 gam kết tủa. Cho chất rắn Y vào dung dịch HNO3 đặc, nóng, dư thu được V lít khí NO2 (đktc) là sản phẩm khử duy nhất. Giá trị của V là A.11,2. B. 22,4. C. 44,8. D. 33.6.
Đọc tiếp
Cho m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO và Fe3O4 vào dung dịch H2SO4 đặc nóng thu được 3,36 lít khí SO2 (đktc). Mặt khác nung m gam hỗn hợp X với khí CO dư thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư thu được 35 gam kết tủa. Cho chất rắn Y vào dung dịch HNO3 đặc, nóng, dư thu được V lít khí NO2 (đktc) là sản phẩm khử duy nhất. Giá trị của V là
A.11,2.
B. 22,4.
C. 44,8.
D. 33.6.
Đáp án C
X + CO tạo thành chất rắn Y gồm các kim loại Mg, Fe, Cu và hỗn hợp khí z gồm CO2 và CO dư
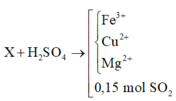
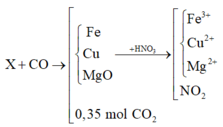
Áp dụng định luật bảo toàn mol electron
Trong thí nghiệm 1: ne nhường = ne nhận = 0,3(mol)
ne nhường trong thí nghiệm = ne nhường (1) + 2.nCO2 =1(mol) = ne nhận (2) = nNO2
Chú ý: Với các bài toán của phản ứng oxi hoá khử gồm nhiều quá trình ta thường sử dụng bảo toàn electron cho toàn bộ các quá trình, bỏ qua giai đoạn trung gian.
Đúng 0
Bình luận (0)
Hấp thụ V lít SO2 (đktc) vào dung dịch Ca(OH)2 thu được 2,4 gam kết tủa. Thêm tiếp dung dịch Ca(OH)2 dư vào bình, thu thêm được 3,6 gam kết tủa. Giá trị của V là:
A. 1,120
B. 2,240
C. 4,480
D. 1,792
\(Ca(HSO_3)_2+ Ca(OH)_2 \to 2CaSO_3\ + 2H_2O\\ n_{Ca(HSO_3)_2} = \dfrac{1}{2}n_{CaSO_3} = \dfrac{1}{2}.\dfrac{3,6}{120} = 0,015(mol)\\ Ca(OH)_2 + SO_2 \to CaSO_3 + H_2O\\ Ca(OH)_2 + 2SO_2 \to Ca(HSO_3)_2\\ n_{SO_2} = 2n_{Ca(HSO_3)_2} + n_{CaSO_3} = 0,015.2 + \dfrac{2,4}{120}=0,05(mol)\\ V = 0,05.22,4 = 1,12(lít)\)
Đúng 1
Bình luận (0)