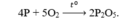PHOTPHO cháy mạnh trong khí oxi sinh ra chất gì?
A.SO2
B.P2O5
C.SO3
PH3

Những câu hỏi liên quan
Đốt cháy 6,2 gam photpho trong X khí oxi ở đktc a) Tìm V b) Tính khối lượng chất mới sinh ra.
a) \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
PTHH: 4P + 5O2 --to--> 2P2O5
0,2-->0,25----->0,1
=> V = 0,25.22,4 = 5,6 (l)
b) \(m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
Đúng 3
Bình luận (0)
Câu 1 ( điểm)Phot pho cháy mạnh trong khí oxi sinh ra chất gì ?A. P 2 O 5B. SO 2C. SO 3D. PH 3Câu 2 ( điểm)Số gam KMnO4 cần dùng để đièu chế được 2,479 lít khí oxi (đktc) là:A. 31,6gB. 14,3gC. 20,7gD. 42,8gCâu 3 ( điểm)Phát biểu nào sau đây về oxi là không đúng? ( BIẾT)A. Oxi là chất khí không không màu , không có mùi và vịB. Oxi cần thiết cho sự sốngC. Oxi là chất khí không không màu , tan vô hạn trong nước , nặng hơn không khíD. Oxi là phi kim hoạt động hoá học rất mạnh, nhất là ở nhịêt độ ca...
Đọc tiếp
Câu 1 ( điểm)
Phot pho cháy mạnh trong khí oxi sinh ra chất gì ?
A. P 2 O 5
B. SO 2
C. SO 3
D. PH 3
Câu 2 ( điểm)
Số gam KMnO4 cần dùng để đièu chế được 2,479 lít khí oxi (đktc) là:
A. 31,6g
B. 14,3g
C. 20,7g
D. 42,8g
Câu 3 ( điểm)
Phát biểu nào sau đây về oxi là không đúng? ( BIẾT)
A. Oxi là chất khí không không màu , không có mùi và vị
B. Oxi cần thiết cho sự sống
C. Oxi là chất khí không không màu , tan vô hạn trong nước , nặng hơn không khí
D. Oxi là phi kim hoạt động hoá học rất mạnh, nhất là ở nhịêt độ cao
Câu 4 ( điểm)
Nhận xét nào sau đây đúng với phương trình hóa học: ( HIỂU)
Fe 3 O 4 + 4H 2 3Fe + 4H 2 O
A. Điều chế khí hiđro
B. Phản ứng không xảy ra
C. Thể hiện tính khử của hiđro
D. Phản ứng phân hủy
Câu 5 ( điểm)
Để điều chế khí hiđro trong phòng thí nghiệm, ta có thể dùng kim loại nhôm tác dụng với:
A. H 2 SO 4 loãng hoặc HCl loãng
B. KClO 3 hoặc KMnO 4
C. CuSO 4 hoặcHCl loãng
D. Fe 2 O 3 hoặcCuO
Câu 6 ( điểm)
Dùng 4 gam khí hiđro để khử oxit sắt từ (Fe 3 O 4 ) thì số gam sắt thu được sau phản ứng là: Fe 3 O 4 + 4H 2 3Fe + 4H 2 O
A. 112 gam
B. 56 gam
C. 84 gam
D. 168 gam
Câu 7 ( điểm)
Ứng dụng nào không phải của H 2 ?
A. Dùng cho sự hô hấp của các sinh vật sống.
B. Làm nhiên liệu cho động cơ tên lửa.
C. Điều chế kim loại từ oxit của chúng.
D. Bơm vào khinh khí cầu.
Câu 8 ( điểm)
Người ta thu khí oxi bằng cách đẩy không khí dựa vào tính chất nào sau đây của oxi?
A. Khí O 2 nặng hơn khôngkhí
B. Khí O 2 dễ hoà tan trongnước.
C. Khí O 2 nhẹ hơn không khí
D. Khí O 2 là khí không mùi.
Câu 9 ( điểm)
Công thức hóa học lưu huỳnh tri oxit là:
A. S 2 O 5 .
B. SO 2
C. SO 3
D. S 2 O 3
Câu 10 ( điểm)
Khi đưa que đóm tàn đỏ vào miệng ống nghiệm chứa khí oxi có hiện tượng gì xảy ra ?
A. Tàn đóm tắt dần
B. Không có hiện tượng gì
C. Tàn đóm tắt ngay
D. Tàn đóm bùng cháy
Câu 11 ( điểm)
Ứng dụng cơ bản của O 2 ? ( BIẾT )
A. Dùng cho sự hô hấp của các sinh vật sống.
B. Dùng để đốt nhiên liệu cho động cơ tên lửa.
C. cung cấp khí oxi trong y tế.
D. cả 3 câu trên đều đúng
Câu 12 ( điểm)
Hiđro được dùng làm nhiên liệu cho động cơ tên lửa vì: ( HIỂU)
A. Do tính chất rất nhẹ.
B. Khi cháy không gây ô nhiễm môi trường.
C. A,B,C đúng
D. Khi cháy sinh nhiều nhiệt.
Câu 13 ( điểm)
Ứng dụng nào không phải của O 2 ? ( HIỂU )
A. Dùng cho sự hô hấp của các sinh vật sống.
B. cung cấp khí oxi trong y tế.
C. Dùng để đốt nhiên liệu cho động cơ tên lửa.
D. Bơm vào khinh khí cầu.
Câu 14 ( điểm)
Trong phòng thí nghiệm, khí oxi được điều chế từ nguyên liệu nào?
A. KMnO 4 hoặc KCl
B. KMnO 4 hoặc KClO 3
C. Không khí hoặc nước
D. Không khí hoặc KMnO 4
Câu 15 ( điểm)
Sự tác dụng của oxi với một chất gọi là :
A. sự thở
B. sự cháy
C. sự đốt nhiên liệu
D. sự oxi hóa
Câu 1:A
Câu 2:A
Câu 3:C
Câu 4:C
Câu 5:A
Câu 6:C
Câu 7:A
Câu 8:A
Câu 9:C
Câu 10:D
Câu 11:A
Câu 12:D
Câu 13:D
Câu 14:B
Câu 15:D
Đúng 0
Bình luận (0)
Câu 1: Đốt cháy 24,8 gam photpho trong bình chứa 34 gam khí oxi, tạo thành điphotpho pentaoxit. Sau khi phản ứng xảy ra hoàn toàn thì chất còn dư và khối lượng dư là:A. Photpho, dư 16,8 gam B. Khí oxi , dư 2gamC. Khí oxi, dư 8,4 gam D. Photpho, dư 4 gamCâu 2: Đốt cháy 3,1 gam phốt pho trong bình chứa 2,8 lít khí oxi (đktc). Sau phản ứng chất nào còn dư ?A. Hai chất vừa hết B. không xác định đượcC. Oxi dư ...
Đọc tiếp
Câu 1: Đốt cháy 24,8 gam photpho trong bình chứa 34 gam khí oxi, tạo thành điphotpho pentaoxit. Sau khi phản ứng xảy ra hoàn toàn thì chất còn dư và khối lượng dư là:
A. Photpho, dư 16,8 gam B. Khí oxi , dư 2gam
C. Khí oxi, dư 8,4 gam D. Photpho, dư 4 gam
Câu 2: Đốt cháy 3,1 gam phốt pho trong bình chứa 2,8 lít khí oxi (đktc). Sau phản ứng chất nào còn dư ?
A. Hai chất vừa hết B. không xác định được
C. Oxi dư D. phốt pho dư
Câu 3: Đốt cháy 6,2 g phốt pho trong bình chứa 6,72 lít (đktc) khí oxi. Khối lượng chất P2O5 tạo ra là:
A. 15,2 g B. 17,2 g C. 14,2 g D. 16,2 g
Câu 4: Đốt sắt trong khí O2 ta thu được oxit sắt từ Fe3O4. Muốn điều chế 23,2g Fe3O4 thì khối lượng Fe cần có là:
A. 13,8g B. 16,8g C. 14,8g D. 12,8g
Câu 5: Trong phòng thí nghiệm cần điều chế cùng thể tích O2 (ở cùng điều kiện). Dùng chất nào dưới đây để có khối lượng nhỏ nhất
A. KClO3 B. KMnO4 C. H2O D. KNO3
Câu 6: Cho các oxit sau CuO, Al2O3, K2O, SO3. Tỉ lệ % Oxi trong oxit nào lớn nhất ?
A. Al2O3 B. K2O C. CuO D. SO3
Câu 7: Quá trình nào dưới đây không làm giảm lượng oxi trong không khí ?
A. Sự hô hấp của các động vật B. Sự gỉ của cá vật dụng bằng sắt
C. Sự quang hợp của cây xanh D. Sự cháy của than, củi, bếp ga
Câu 8: Đốt cháy lưu huỳnh trong bình chứa 7 lít khí oxi. Sau phản ứng người ta thu được4,48 lít khí sunfurơ. Biết các khí ở đktc. Khối lượng lưu huỳnh đã cháy là:
A. 6,5 g B. 6,8 g C. 7g D. 6.4 g
Câu 9: Đốt cháy 6,2 g photpho trong bình chứa 6,72 lít khí oxi (đkc) tạo thành điphotpho pentaoxit.
a) Chất nào còn dư, chất nào thiếu?
A. Photpho còn dư, oxi thiếu B. Photpho còn thiếu, oxi dư
C. Cả hai chất vừa đủ D. Tất cả đều sai
b) Khối lượng chất tạo thành là bao nhiêu?
A. 15,4 g B. 14,2 g C. 16 g D. Tất cả đều sai
Câu 10: Có một số công thức hoá học oxit được viết thành dãy như sau, dãy nào không có công thức sai?
1. CO, O3, Ca2O, Cu2O, Hg2O, NO 2. CO2, N2O5, CuO, Na2O, Cr2O3, Al2O3
3. N2O5, NO, P2O5, Fe2O3, Ag2O, K2O 4. MgO, PbO, FeO, SO2, SO4, N2O
5. ZnO, Fe3O4, NO2, SO3, H2O2, Li2O
A. 1, 2 B. 2, 3, 4 C. 2, 3, 5 D. 1, 3, 5
Câu 1. B
Câu 2. D
Câu 3. C
Câu 4. B
Câu 5. C
Câu 6. D
Câu 7. C
Câu 8. D
Câu 9. a) A; b) B
Câu 10. C
Đúng 2
Bình luận (0)
Câu 1:Đốt cháy 12,4 gam photpho trong bình chứa khí oxi tạo thành điphotpho pentaoxit (chất rắn, màutrắng). Tính khối lượng chất rắn tạo thành sau phản ứng.
Câu 2:Đốt cháy 12,4 gam photpho trong bình chứa 5,6 lít khí oxi (đktc) tạo thành điphotpho pentaoxit (chất rắn, màu trắng). Tính khối lượng chất rắn tạo thành sau phản ứng.
Câu 1 :
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
Pt : \(4P+5O_2\underrightarrow{t^o}2P_2O_5|\)
4 5 2
0,4 0,2
\(n_{P2O5}=\dfrac{0,4.2}{4}=0,2\left(mol\right)\)
⇒ \(m_{P2O5}=0,2.142=28,4\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
Câu 2 :
\(n_P=\dfrac{12,4}{31}=0,4\left(mol\right)\)
\(n_{O2\left(dktc\right)}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Pt : \(4P+5O_2\underrightarrow{t^o}2P_2O_5|\)
4 5 2
0,4 0,25 0,1
Lập tỉ số só sánh : \(\dfrac{0,4}{4}>\dfrac{0,25}{5}\)
⇒ P dư , O2 phản ứng hết
⇒ Tính toán dựa vào số mol của O2
\(n_{P2O5}=\dfrac{0,25.2}{5}=0,1\left(mol\right)\)
⇒ \(m_{P2O5}=0,1.142=14,2\left(g\right)\)
\(n_{P\left(dư\right)}=0,4-\left(\dfrac{0,25.4}{5}\right)=0,2\left(mol\right)\)
⇒ \(m_{P\left(dư\right)}=0,2.31=6,2\left(g\right)\)
\(m_{rắn}=14,2+6,2=20,4\left(g\right)\)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 6,2 gam Photpho trong bình chứa 8,96 lít khí Oxi ( đktc ). Sản phẩm thu được là chât rắn, màu trắng (P2O5)
a) Viết PTHH xảy ra?
b) Photpho và khí Oxi, chất nào dư, dư bao nhiêu gam?
c) Tính khối lượng chất tạo thành (P2O5)?
d) Nếu hiệu suất của phản ứng là 80% thì khối lượng chất rắn (P2O5) thu được là bao nhiêu?
a, \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
b, \(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{4}< \dfrac{0,4}{5}\), ta được O2 dư.
Theo PT: \(n_{O_2\left(pư\right)}=\dfrac{5}{4}n_P=0,25\left(mol\right)\Rightarrow n_{O_2\left(dư\right)}=0,4-0,25=0,15\left(mol\right)\)
\(\Rightarrow m_{O_2\left(dư\right)}=0,15.32=4,8\left(g\right)\)
c, Theo PT: \(n_{P_2O_5}=\dfrac{1}{2}n_P=0,1\left(mol\right)\Rightarrow m_{P_2O_5}=0,1.142=14,2\left(g\right)\)
d, \(m_{P_2O_5}=14,2.80\%=11,36\left(g\right)\)
Đúng 1
Bình luận (0)
Câu 1 : a, Tính thể tích khí oxi và không khí cần thiết để đốt cháy 62g Photpho , biết rằng không khí có 20% về thể tích khí oxi ( Thể tích khí đo ở đktc )b, Nếu đốt cháy 31g Photpho trong 23g (lít ) khí O2- Chất nào còn dư ? Khối lượng là bao nhiêu...
Xem chi tiết
a)
\(n_P = \dfrac{62}{31} = 2(mol)\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ n_{O_2} = \dfrac{5}{4}n_P = 2,5(mol)\\ V_{O_2} = 2,5.22,4 = 56(lít)\\ V_{không\ khí} = \dfrac{56}{20\%} = 280(lít)\)
b)
\(n_P = \dfrac{31}{31} = 1(mol) ; n_{O_2} = \dfrac{23}{32} = 0,71875(mol)\\ \dfrac{n_P}{4} = 0,25 > \dfrac{n_{O_2}}{5} = 0,14375 \to P\ dư\\ n_{P\ pư} = \dfrac{4}{5}n_{O_2} = 0,575(mol)\\ m_{P\ dư} = 31 - 0,575.31 = 13,175(gam)\\ n_{P_2O_5} = \dfrac{2}{5}n_{O_2} = 0,2875(mol) \Rightarrow m_{P_2O_5} = 0,2875.142=40,825(gam)\)
Đúng 3
Bình luận (5)
Câu 1:
PTHH: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
a) Ta có: \(n_P=\dfrac{62}{31}=2\left(mol\right)\) \(\Rightarrow n_{O_2}=2,5\left(mol\right)\)
\(\Rightarrow V_{O_2}=2,5\cdot22,4=56\left(l\right)\) \(\Rightarrow V_{kk}=\dfrac{56}{20\%}=280\left(l\right)\)
b) Ta có: \(\left\{{}\begin{matrix}n_P=\dfrac{31}{31}=1\left(mol\right)\\n_{O_2}=\dfrac{2}{32}=0,0625\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{1}{4}>\dfrac{0,0625}{5}\) \(\Rightarrow\) Photpho còn dư, Oxi p/ư hết
\(\Rightarrow n_{P\left(dư\right)}=0,95\left(mol\right)\) \(\Rightarrow m_{P\left(dư\right)}=0,95\cdot31=29,45\left(g\right)\)
Theo PTHH: \(n_{P_2O_5}=0,025\left(mol\right)\) \(\Rightarrow m_{P_2O_5}=0,025\cdot142=3,55\left(g\right)\)
Đúng 1
Bình luận (2)
Đốt cháy 12,4g photpho trong bình chứa 17g khí oxi tạo thành chất rắn màu trắng là P2O5
a.Viết phương trình phản ứng
b.Tính khối lượng chất dư sau phản ứng
c.Tính khối lượng chất rắn tạo ra
\(n_P=\dfrac{12,4}{31}=0,4mol\)
\(n_{O_2}=\dfrac{17}{32}=0,53125mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
\(\dfrac{0,4}{4}\) < \(\dfrac{0,53125}{5}\) ( mol )
0,4 0,5 0,2 ( mol )
\(m_{O_2\left(dư\right)}=\left(0,53125-0,5\right).32=1g\)
\(m_{P_2O_5}=0,2.142=28,4g\)
Đúng 1
Bình luận (0)
Oxit sinh ra khi đốt cháy một lượng nhỏ photpho đơn chất (P) trong bình chứa khí chứa
O
2
dư là A.
PO
5
.
B.
P
2
O
7
.
C.
P
2
O
3
.
D.
P
2
O
5
.
Đọc tiếp
Oxit sinh ra khi đốt cháy một lượng nhỏ photpho đơn chất (P) trong bình chứa khí chứa O 2 dư là
A. PO 5 .
B. P 2 O 7 .
C. P 2 O 3 .
D. P 2 O 5 .
Đốt cháy 6,2 gam photpho trong bình chứa 7,84 lít khí oxi ở đktc
a. Viết ptpu xảy ra
b. tính khối lượng chất dư sau phản ứng ?
c. tính khối lượng chất rắn tạo ra ?
$a) 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5$
$n_P = \dfrac{6,2}{31} = 0,2(mol) ; n_{O_2} = \dfrac{7,84}{22,4} = 0,35(mol)$
$n_P : 4 = 0,05 < n_{O_2} :5 = 0,07$ nên $O_2$ dư
$n_{O_2\ pư} = \dfrac{5}{4}n_P = 0,25(mol)$
$\Rightarrow m_{O_2\ dư} = (0,35 - 0,25).32 = 3,2(gam)$
c) $n_{P_2O_5} = \dfrac{1}{2}n_P = 0,1(mol)$
$m_{P_2O_5} = 0,1.142 = 14,2(gam)$
Đúng 3
Bình luận (0)
\(n_P=\dfrac{6,2}{31}=0,2\left(mol\right)\\ n_{O_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\\a, 4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\\ V\text{ì}:\dfrac{0,35}{5}>\dfrac{0,2}{4}\Rightarrow O_2d\text{ư}\\ n_{O_2\left(d\text{ư}\right)}=0,35-\dfrac{5}{4}.0,2=0,1\left(mol\right)\\b, m_{O_2\left(d\text{ư}\right)}=0,1.32=3,2\left(g\right)\\ c,n_{P_2O_5}=\dfrac{n_P}{2}=\dfrac{0,2}{2}=0,1\left(mol\right)\\ m_{r\text{ắn}}=m_{P_2O_5}=142.0,1=14,2\left(g\right)\)
Đúng 2
Bình luận (0)