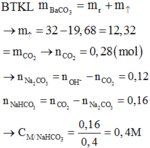hòa tan 6 g NaOH vào 1,5 l H2O . Xác định nồng độ mol/l dung dịch thu được . giả sử thể tích dung dịch không đổi

Những câu hỏi liên quan
hòa tan 6 g NaOH vào 1,5 l H2O . Xác định nồng độ mol/l dung dịch thu được . giả sử thể tích dung dịch không đổi
hòa tan 6 g NaOH vào 1,5 l H2O . Xác định nồng độ mol/l dung dịch thu được . giả sử thể tích dung dịch không đổi
nNaOH = 6/40 = 0,15
=> CM NaOH = 0,15/ 1,5 = 0,1M
Đúng 0
Bình luận (0)
Tính nồng độ mol và nồng độ % của dung dịch sau:
Hòa tan 8g NaOH vào 100g H2O(với 1g H2O =1ml H2O; thể tích dung dịch thay đổi không đáng kể)
Ta có: \(C\%_{NaOH}=\dfrac{8}{8+100}.100\%\approx7,41\%\)
\(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\)
V dd sau hòa tan = 100 (ml) = 0,1 (l)
\(\Rightarrow C_{M_{NaOH}}=\dfrac{0,2}{0,1}=2\left(M\right)\)
Đúng 2
Bình luận (0)
Câu 1 Hòa tan 20g CaCl2 vào 250g H2O .Tính nồng độ % của dung dịch thu được
Câu 2 Hòa tan 6,5 g Zn trong dung dịch HCl 2M vừa đủ
a) Tính VH2 thu được ở điều kiện xác định
b) Tính nồng độ mol của chất tan trong dung dịch sau phản ứng .Gọi Vdd thay đổi không đáng kể
cho 3,92 cao tan hết trong nước thu được 700 ml dung dịch a dẫn 1,12 l cacbon đioxit ( điều kiện tiêu chuẩn) vào dung dịch a.tính khối lượng các chất thu được sau phản ứng.tính nồng độ mol của dung dịch thu được (giả sử thể tích dung dịch không đổi)
\(n_{CaO}=\dfrac{3.92}{56}=0.07\left(mol\right)\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(0.07.....................0.07\)
\(n_{CO_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(T=\dfrac{0.05}{0.07}=0.7\)
\(\Rightarrow\text{Tạo ra muối TH}\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(0.05...............0.05.........0.05\)
\(m_{CaCO_3}=0.05\cdot100=5\left(g\right)\)
\(C_{M_{Ca\left(OH\right)_2\left(dư\right)}}=\dfrac{0.07-0.05}{0.7}=\dfrac{1}{35}\left(M\right)\)
Đúng 2
Bình luận (0)
Hòa tan 8 gam CuO bằng dung dịch HCl 1M tính thể tích dung dịch HCl 1M cẫn dùng .Tính nồng độ mol thu được sao phản ứng giả sử thể tích của dung dịch thay đổi không đáng kể
Xem chi tiết
\(CuO+2HCl\rightarrow CuCl_2+H_2O\\ n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\\ n_{HCl}=2.0,1=0,2\left(mol\right)\\ V_{ddHCl}=\dfrac{0,2}{1}=0,2\left(l\right)\\ V_{ddsau}=V_{ddHCl}=0,2\left(l\right)\\ n_{CuCl_2}=n_{CuO}=0,2\left(mol\right)\\ C_{MddCuCl_2}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Đúng 2
Bình luận (0)
Nhiệt phân 32,0 gam CaCO3 , sau một thời gian thu được khí X và 19,68 gam rắn Y. Hấp thu toàn bộ X vào 400 ml dung dịch NaOH 1M, kết thúc phản ứng thu được dung dịch Z. Giả sử thể tích dung dịch không đổi. Nồng độ mol/l của NaHCO3 trong dung dịch Z là A. 0,2M B. 0,4M C. 0,3M D. 0,6M
Đọc tiếp
Nhiệt phân 32,0 gam CaCO3 , sau một thời gian thu được khí X và 19,68 gam rắn Y. Hấp thu toàn bộ X vào 400 ml dung dịch NaOH 1M, kết thúc phản ứng thu được dung dịch Z. Giả sử thể tích dung dịch không đổi. Nồng độ mol/l của NaHCO3 trong dung dịch Z là
A. 0,2M
B. 0,4M
C. 0,3M
D. 0,6M
cho 3,92 g CaO tan hết trong nước thu được 700 mà dung dịch A. Dẫn 1,12l cacbon đioxit (đktc) vào dung dịch A. Tính khối lượng các chất thu được sau phản ứng. Tính nồng độ mol của dung dịch thu được (giả sử Thể tích dung dịch không đổi)
PTHH: \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
Ta có: \(\left\{{}\begin{matrix}n_{Ca\left(OH\right)_2}=n_{CaO}=\dfrac{3,92}{56}=0,07\left(mol\right)\\n_{CO_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Tạo muối trung hòa
PTHH: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
Ta có: \(n_{Ca\left(OH\right)_2\left(dư\right)}=0,07-n_{Ca\left(OH\right)_2\left(p/ứ\right)}=0,07-n_{CO_2}=0,02\left(mol\right)\)
\(\Rightarrow C_{M_{Ca\left(OH\right)_2\left(dư\right)}}=\dfrac{0,02}{0,7}\approx0,03\left(M\right)\)
Đúng 1
Bình luận (0)
Hòa tan muối nitrat của 1 kim loại hóa trị 2 vào nước thu được dung dịch A. Cho vào dung dịch A 200ml dung dịch K3PO4, phản ứng xảy ra vừa đủ, thu được kết tủa D và dung dịch C. Khối lượng kết tủa B và khối lượng muối nitrat trong dung dịch A khác nhau 3,64g.1. Tìm nồng độ mol/l của dung dịch A và C, giả thiết thể tích dung dịch không thay đổi do pha trộn và thể tích kết tủa không đáng kể.2. Cho dung dịch NaOH dư vào 100ml dung dịch A thu được kết tủa D, lọc kết tủa D rồi đem nung cho đến khi kh...
Đọc tiếp
Hòa tan muối nitrat của 1 kim loại hóa trị 2 vào nước thu được dung dịch A. Cho vào dung dịch A 200ml dung dịch K3PO4, phản ứng xảy ra vừa đủ, thu được kết tủa D và dung dịch C. Khối lượng kết tủa B và khối lượng muối nitrat trong dung dịch A khác nhau 3,64g.
1. Tìm nồng độ mol/l của dung dịch A và C, giả thiết thể tích dung dịch không thay đổi do pha trộn và thể tích kết tủa không đáng kể.
2. Cho dung dịch NaOH dư vào 100ml dung dịch A thu được kết tủa D, lọc kết tủa D rồi đem nung cho đến khi khối lượng không đổi cân được 2,4g chất rắn. Xác định kim loại trong muối nitrat