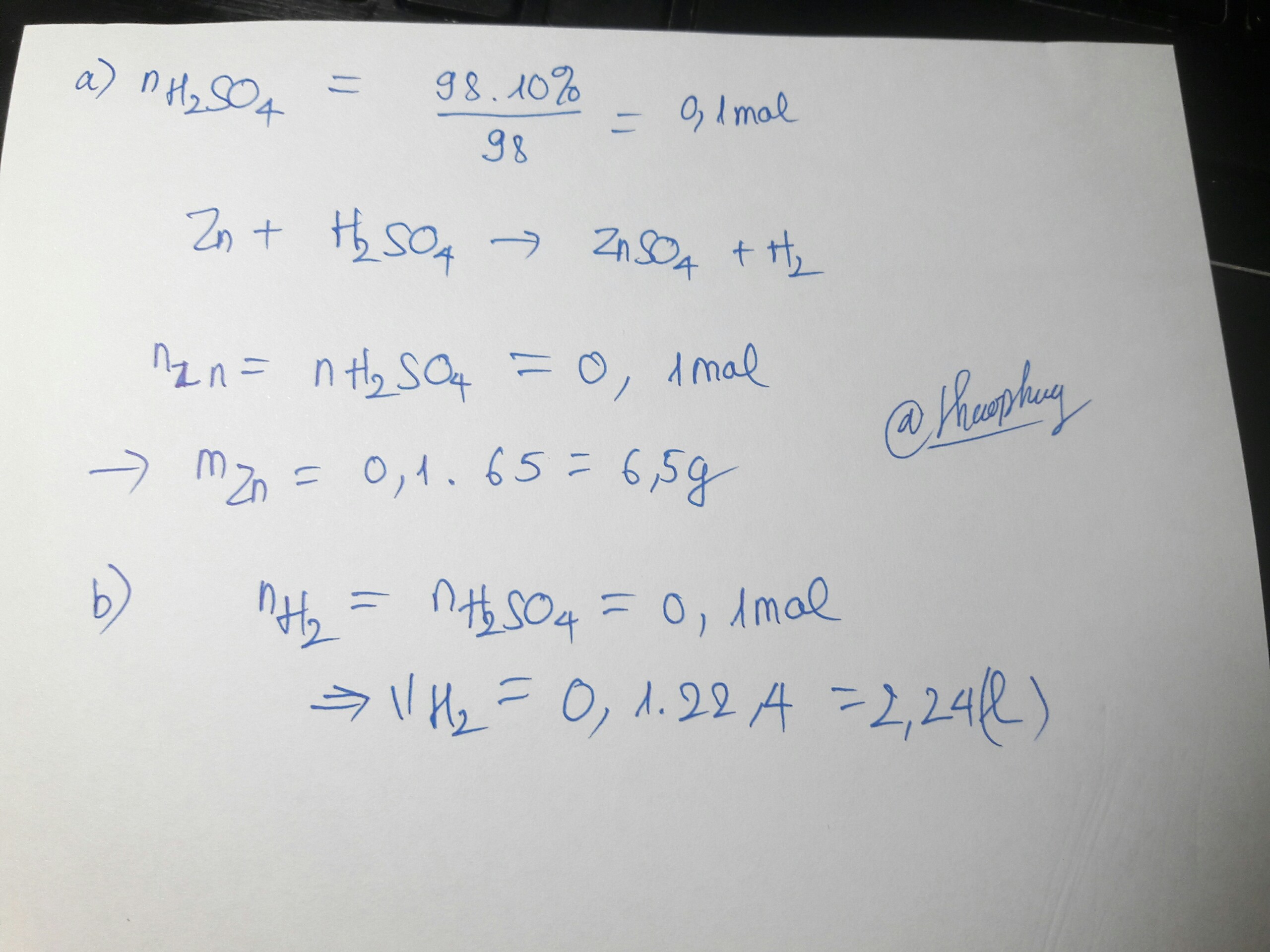Để điều chế khí H2 trong phòng thí ngiệm,người ta cho 6,5g Zn vào dd H2SO4. a/ Viết pt phản ứng b/ Tính khối lượng H2SO4 đã dùng c/ Nếu dùng lượng H2 nói trên đi qua bột FeO nung núng thì khối lượng kim loại Fe thu đc là bào nhiêu???

Những câu hỏi liên quan
trong phòng thí nghiệm, ngta dùng khí H2 để khử sắt (III) oxit (Fe2O3) và thu đc 22,4 g sắt (Fe) và nước (H2O)
a) tính khối lượng sắt (III) oxit đã phản ứng?
b) tính thể tích khí hidro đã sử dụng
c) để điều chế lượng khí hidro trên, người ta dùng kim loại kẽm (Zn) cho phản ứng với dung dịch axit sunfuric (H2SO4) . tính khối lượng kim loại kẽm cần dùng
PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
a+b) \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,2\left(mol\right)\\n_{H_2}=0,6\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,2\cdot160=32\left(g\right)\\V_{H_2}=0,6\cdot22,4=13,44\left(l\right)\end{matrix}\right.\)
c) PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Theo PTHH: \(n_{Zn}=n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,6\cdot65=39\left(g\right)\)
Đúng 3
Bình luận (0)
a,
nFe = 22,4/56 = 0,4 (mol)
PTHH
Fe2O3 + 3H2 ---to----) 2Fe + 3H2O (1)
theo phương trình (1) ,ta có:
nFe2O3 = 0,4 x 2 / 1 = 0,8 (mol)
mFe2O3 = 160 x 0,8 = 128 (g)
b,
theo pt (1)
nH2 = (0,4 x 3)/2 = 0,6 (mol)
=) VH2 = 0,6 x 22,4 = 13,44 (L)
c,
PTHH
Zn + H2SO4 -------------) ZnSO4 + H2 (2)
Số mol H2 cần dùng là 0,6 (mol)
Theo PT (2) :
nZn = nH2 ==) nZn = 0,6 x 65 = 39 (g)
Đúng 0
Bình luận (1)
Câu 9. 10/ Cho 16,2g ZnO t ác dụng vói khí H2 đun nóng. a/ Viết phương trình hóa học của phản ứng?b/ Tính thể tích H2 (đktc) đã dùng? c/ Tính khối lượng Zn điều chế được10 Trong ph òng th í nghiệm người ta dùng khí CO để khử Fe3O4 v à H2 để khử Fe2O3 ở nhiệt độ cao . trong mỗi pư trên điều có 0,1mol mỗi loại ôxit sắt tham giaa/ Tính thể tích CO và H2 (đktc) đã dùng? b/ Tính khối lượng kim loại Fe thu được sau mỗi pư
Đọc tiếp
Câu 9. 10/ Cho 16,2g ZnO t ác dụng vói khí H2 đun nóng. a/ Viết phương trình hóa học của phản ứng?
b/ Tính thể tích H2 (đktc) đã dùng? c/ Tính khối lượng Zn điều chế được
10 Trong ph òng th í nghiệm người ta dùng khí CO để khử Fe3O4 v à H2 để khử Fe2O3 ở nhiệt độ cao . trong mỗi pư trên điều có 0,1mol mỗi loại ôxit sắt tham gia
a/ Tính thể tích CO và H2 (đktc) đã dùng? b/ Tính khối lượng kim loại Fe thu được sau mỗi pư
nZnO = 16,2 : 81 = 0,2(mol)
pthh : ZnO + H2 -t--> Zn + H2O
0,2--->0,2-----> 0,2 (mol)
=> VH2 = 0,2 .22,4 = 4,48 (l)
=> mZn = 0,2 . 65 = 13 (g)
2
Fe3O4 + 4CO -t--> 3Fe + 4CO2
0,1-------> 0,4 -------->0,3 (mol)
Fe2O3 + 3H2 -t--> 2Fe + 3H2O
0,1------->0,3 -------->0,2 (mol)
=> VH2 = 0,3 .22,4 = 6,72(L)
=> VCO = 0,2 . 22,4 = 4,48 (L)
mFe= (0,3 + 0,2 ) . 56 = 28 (g)
Đúng 2
Bình luận (1)
9.
\(n_{ZnO}=\dfrac{16,2}{81}=0,2mol\)
\(ZnO+H_2\rightarrow\left(t^o\right)Zn+H_2O\)
0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
\(m_{Zn}=0,2.65=13g\)
10.
\(Fe_3O_4+4H_2\rightarrow\left(t^o\right)3Fe+4H_2O\)
0,1 0,4 0,3 ( mol )
\(V_{H_2}=0,4.22,4=8,96l\)
\(m_{Fe}=0,3.56=16,8g\)
\(Fe_3O_4+4CO\rightarrow\left(t^o\right)3Fe+4CO_2\)
0,1 0,4 0,3 ( mol )
\(V_{CO}=0,4.22,4=8,96l\)
\(m_{Fe}=0,3.56=16,8g\)
Đúng 1
Bình luận (2)
Cho 1 ít bột Al vào 150ml dd H2SO4. Phản ứng xong thu được 8,96(l) khí H2 (ở đktc). a/ Viết phương trình phản ứng. b/ Tính khối lượng Al tham gia phản ứng. c/Tính nồng độ mol/lit của dd H2SO4 đã dùng.
a) 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
b) \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
____\(\dfrac{4}{15}\)<----0,4<--------------------0,4
=> \(m_{Al}=\dfrac{4}{15}.27=7,2\left(g\right)\)
c) \(C_{M\left(H_2SO_4\right)}=\dfrac{0,4}{0,15}=2,667M\)
Đúng 1
Bình luận (0)
Hòa tan hết 13g Zn bằng dung dịch axit sunfuric loãng ( H2SO4)
a) Viết PT phản ứng
b)Tính thể tích khí H2 (đktc) và khối lượng muối kẽm sunfat (ZnSO4) tạo thành?
c) Dẫn hết lượng khí H2 sinh ra cho đi qua bột CuO nung nóng. Hãy tính khối lượng kim loại tạo thành sau phản ứng?
a, Ta có:
nZn = 13/65= 0,2(mol)
PTHH: Zn + H2SO4 → ZnSO4 + H2
0,2-----------------------------------0,2
Theo PT : nZnSO4 = 0,2.1/1 = 0,2(mol)
mZnSO4 = 0,2. 161 = 32,2(g)
b, Ta có:
Theo PT : nH2 = 0,2.1/1 = 0,2(mol)
VH2(đktc) = 0,2 . 22,4 = 4,48(l)
CuO+H2-to>Cu+H2O
0,2-----0,2
=>m Cu=0,2.64=12,8g
Đúng 1
Bình luận (1)
Cho một lượng bột zinc Zn vào dung dịch hydrochloric acid HCl thì phản ứng vừa đủ. Biết đã dùng 13 gam zinc. a) Tính khối lượng hydrochloric acid HCl phản ứng b) Tính thể tích khí hydrogen H2 (đkc) điều chế c) Dẫn toàn bộ lượng khí hydrogen thu được ở phản ứng trên qua bột iron (III) oxide đốt nóng thì phản ứng hoàn toàn. Tính khối lượng iron thu được
a, \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
_____0,2____0,4___________0,2 (mol)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
b, \(V_{H_2}=0,2.24,79=4,958\left(l\right)\)
c, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
____________0,2__2/15 (mol)
\(\Rightarrow m_{Fe}=\dfrac{2}{15}.56=\dfrac{112}{15}\left(g\right)\)
Đúng 2
Bình luận (0)
Số mol của 13 gam Zn:
\(n_{Zn}=\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
1 : 2 : 1 : 1 (g)
0,2\(\rightarrow\) 0,4 : 0,2 : 0,2 (mol)
a,Khối lượng của 0,4 mol HCl:
\(m_{HCl}=n.M=0,4.36,5=14,6\left(g\right)\)
b, Thể tích khí H2:
\(V_{H_2}=n.24,79=0,2.24,79=4,958\left(l\right)\)
\(3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\)
Khối lượng của \(\dfrac{2}{15}\) mol Fe:
\(n_{Fe}=\dfrac{m}{M}=\dfrac{2}{\dfrac{15}{56}}\approx7,5\left(g\right)\)
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm để điều chế khí hiđro người ta cho kim loại kẽm ( Zn ) tác dụng với đ axit sunfuric ( H2SO4 ) thu được 2,25 lít khí hiđro ( đktc ). Hãy tính a/ khối lượng Zn cần dùng b/ Khối lượng muối kẽm sunfat thu được
2,24 lít hidro chứ chắc không phải 2,25 em hi?
Đúng 0
Bình luận (0)
điều chế hidro trong phòng thí nghiệm bằng cách hòa tan hết Zn vào 98 gam dung dịch H2SO4 10%. Hãy tính:
a) khối lượng Zn đã tan hết
b) Thể tích khí H2 thu được sau phản ứng
Hòa tan hoàn toàn 14 gam sắt trong dung dịch H2SO4 loãng.
a) Viết phương trình phản ứng.
b) Tính khối lượng H2SO4 đã phản ứng?
c) Tính thể tích khí hiđro sinh ra ở đktc.
d) Nếu dùng toàn bộ lượng H2 bay ra ở trên đem khử bột CuO ở nhiệt độ cao thì thu được bao
nhiêu gam Cu?
Fe+H2SO4->FeSO4+H2
0,25--0,25-----0,25---0,25
CuO+H2-to>Cu+H2O
0,25----0,25
n Fe=0,25 mol
m H2SO4=0,25.98=24,5g
m H2=0,25.22,4=5,6l
m Cu=0,25.64=16g
Đúng 2
Bình luận (0)
dẫn khí hidro đi qua ống thủy tinh chứa 16 g bột CuO nung đến 400 độ C
a Tính khối lượng H2O tạo thành nếu lượng CuO phản ứng chiếm 80% lượng ban đầu
b Tính khối lượng chất rắn sau phản ứng Nếu đã dùng 3,718 l H2 ở điều kiện chuẩn và phản ứng xảy ra hoàn toàn
c Tính H% theo CuO nếu khối lượng chất rắn thu được sau phản ứng nặng 13,28 g
cop tên ng ta nè
a) CuO+H2−to→Cu+H2OCuO+H2−to→Cu+H2O
0,21>0,151⇒0,21>0,151⇒Sau phản ứng CuO dư
Chất rắn sau phản ứng là Cu, CuO dư
mcr=0,15.64+(0,2−0,15).80=13,6(g)mcr=0,15.64+(0,2−0,15).80=13,6(g)
c) Gọi x là số mol CuO phản ứng
mcr=(0,2−x).80+64x=13,28mcr=(0,2−x).80+64x=13,28
=> x=0,17 (mol)
Đúng 2
Bình luận (0)