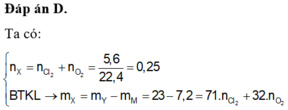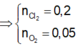cho a gam hỗn hợp kim loại gồm natri và sắt phản ứng với nước dư,sau phản ứng thu đc 4,48 lít khí ở đktc và 16,8 gam một chất rắn không tan.Giá trị của a là

Những câu hỏi liên quan
Câu 1: Cho a gam hỗn hợp kim loại Cu và Mg vào dung dịch HCl,sau phản ứng thu đc 5,6 lít khí Hidro (đktc) và 4 gam chất rắn không tan.Giá trị a và %m của kim loại Mg lần lượt là A.4;40% B.10;40% C.10;60% D.6;60%Câu 2: Trung hòa 200ml dung dịch H2SO4 1M bằng dung dịch NaOH 20%.Khối lượng dung dịch NaOH cần dùng là (biết H1;O16;Na23;S32) A.40 gam B.80 gam C.26 gam D.20 gamCâu 3: Hòa t...
Đọc tiếp
Câu 1: Cho a gam hỗn hợp kim loại Cu và Mg vào dung dịch HCl,sau phản ứng thu đc 5,6 lít khí Hidro (đktc) và 4 gam chất rắn không tan.Giá trị a và %m của kim loại Mg lần lượt là
A.4;40% B.10;40% C.10;60% D.6;60%
Câu 2: Trung hòa 200ml dung dịch H2SO4 1M bằng dung dịch NaOH 20%.Khối lượng dung dịch NaOH cần dùng là (biết H=1;O=16;Na=23;S=32)
A.40 gam B.80 gam C.26 gam D.20 gam
Câu 3: Hòa tan hết 3,6 gam một kim loại hóa trị II bằng dung dịch H2SO4 loãng.Sau phản ứng thu đc 3,36 lít H2(đktc).Kim loại đó là (biết Mg=24;Ca=40;Fe=56;Zn=65)
A.Fe B.Zn C.Ca D.Mg
Cho 7,2 gam kim loại M , có hoá trị không đổi trong hợp chất, phản ứng hoàn toàn với hỗn hợp khí X gồm Cl2 và O2. Sau phản ứng thu được 23,0 gam chất rắn Y và thể tích hỗn hợp khí đã phản ứng là 5,6 lít (ở đktc). Kim loại M là: A. Cu B. Ca C. Ba D. Mg.
Đọc tiếp
Cho 7,2 gam kim loại M , có hoá trị không đổi trong hợp chất, phản ứng hoàn toàn với hỗn hợp khí X gồm Cl2 và O2. Sau phản ứng thu được 23,0 gam chất rắn Y và thể tích hỗn hợp khí đã phản ứng là 5,6 lít (ở đktc). Kim loại M là:
A. Cu
B. Ca
C. Ba
D. Mg.
Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là A. Mg B. Al C. Ca D. Na
Đọc tiếp
Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là
A. Mg
B. Al
C. Ca
D. Na
Đáp án A
M → Mn+ + ne
1,25 → 1,25nx
Zn → Zn2+ + 2e
x → 2x
Cl2 + 2e → 2Cl-
0,2 → 0,4
2H+ + 2e → H2
0,5 ← 0,25
BT e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
(1)(2) ⇒ (1,25M +65)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)
Đúng 0
Bình luận (0)
Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là: A. Mg B. Al C. K D. Na
Đọc tiếp
Cho 19 gam hỗn hợp gồm kim loại M ( hóa trị không đổi ) và Zn (có tỉ lệ mol tương ứng là 1,25:1) và bình đựng 4,48 lít khí Cl2 (đktc), sau các phản ứng hoàn toàn thu được hỗn hợp chất rắn X. Cho X tan hết trong dung dịch HCl (dư) thấy có 5,6 lít khí H2 thoát ra (đktc). Kim loại M là:
A. Mg
B. Al
C. K
D. Na
Đáp án A
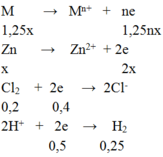
Bảo toàn e ⇒1,25nx + 2x = 0,4 + 0,5 = 0,9 (1)
Mặt khác: 1,25M + 65M = 19 (2)
Từ (1) và (2) ⇒ (1,25M +65M)/(1,25n + 2) = 19/0,9 ⇒ n = 2; M = 24(Mg)
Đúng 0
Bình luận (0)
Cho 12,4 gam hỗn hợp gồm 2 kim loại là A (hóa trị II) và đồng phản ứng với lượng dư dung dịch HCl, sau phản ứng thấy trong dung dịch có 6,4 gam chất rắn không tan và thoát ra 5,6 lít khí không màu ở đktc. Xác định tên kim loại A giup em a
Đọc tiếp
Cho 12,4 gam hỗn hợp gồm 2 kim loại là A (hóa trị II) và đồng phản ứng với lượng dư dung dịch HCl, sau phản ứng thấy trong dung dịch có 6,4 gam chất rắn không tan và thoát ra 5,6 lít khí không màu ở đktc. Xác định tên kim loại A
giup em a
2. Đốt cháy hoàn toàn 6,3 gam một kim loại R chưa biết hóa trị trong hỗn hợp khí Z gồm Cl2 và O2. Sau phản ứng thu được 20,15 gam chất rắn và thể tích hỗn hợp khí Z đã phản ứng là 5,6 lít (ở đktc)a. Xác định kim loại R.b. Nếu cho m gam hỗn hợp kim loại R ở trên, oxit của R và hidroxit tương ứng của R, tác dụng với lượng vừa đủ dung dịch H2SO4 19,6% thu được dung dịch Y có nồng độ 21,302% và 3,36 lít khí thoát ra (ở đktc). Cô cạn dung dịch Y thu được 80,37 gam muối khan. Hãy xác định m?
Đọc tiếp
2. Đốt cháy hoàn toàn 6,3 gam một kim loại R chưa biết hóa trị trong hỗn hợp khí Z gồm Cl2 và O2. Sau phản ứng thu được 20,15 gam chất rắn và thể tích hỗn hợp khí Z đã phản ứng là 5,6 lít (ở đktc)
a. Xác định kim loại R.
b. Nếu cho m gam hỗn hợp kim loại R ở trên, oxit của R và hidroxit tương ứng của R, tác dụng với lượng vừa đủ dung dịch H2SO4 19,6% thu được dung dịch Y có nồng độ 21,302% và 3,36 lít khí thoát ra (ở đktc). Cô cạn dung dịch Y thu được 80,37 gam muối khan. Hãy xác định m?
Cho 15 gam hỗn hợp bột kim loại Zn và Cu vào dung dịch HCl dư, sau khi phản ứng xảy ra hoàn toàn thu được 4,48 lít khí H2 (đktc) và m gam chất rắn không tan. Giá trị của m là:
A. 6,4
B. 8,5
C. 2,2
D. 2,0
Đáp án D.
Chất rắn không tan là Cu.
![]()
Zn + 2HCl → ZnCl2 + H2
0,2 ← 0,2 (mol)
mZn = 0,2.65 = 13 (g) => mCu = 15 – 13 = 2 (g)
Đúng 0
Bình luận (0)
Cho 2,016 lít (đktc) hỗn hợp khí gồm
C
l
2
và
O
2
tác dụng vừa đủ với 5,72 gam hỗn hợp gồm Cr và kim loại R (chỉ có một hóa trị), thu được 10,55 gam chất rắn X.Cho X vào 200 gam dung dịch NaOH 8% (loãng), thấy có một nửa lượng NaOH đã phản ứng, thu được dung dịch Y và chất rắn Z. Cho từng giọt
B
r
2
lỏng (dư) vào Y, tạo thành 3,24 gam natri cromat...
Đọc tiếp
Cho 2,016 lít (đktc) hỗn hợp khí gồm C l 2 và O 2 tác dụng vừa đủ với 5,72 gam hỗn hợp gồm Cr và kim loại R (chỉ có một hóa trị), thu được 10,55 gam chất rắn X.
Cho X vào 200 gam dung dịch NaOH 8% (loãng), thấy có một nửa lượng NaOH đã phản ứng, thu được dung dịch Y và chất rắn Z. Cho từng giọt B r 2 lỏng (dư) vào Y, tạo thành 3,24 gam natri cromat.
Biết các phản ứng xảy ra hoàn toàn, hiđroxit của R ít tan trong nước. Hãy cho biết R là kim loại nào sau đây?
A. Cu
B. Mg
C. Al
D. Zn
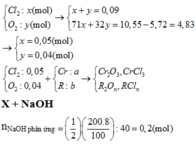
C r C l 3 + 4 N a O H → N a C r O 2 + 3 N a C l + 2 H 2 O 0 , 02 0 , 08 0 , 02 2 N a C r O 2 + 3 B r 2 + 8 N a O H → 2 N a 2 C r O 4 + 6 N a B r + 4 H 2 O 0 , 02 0 , 08 0 , 02


Đúng 0
Bình luận (0)
Cho một lượng hỗn hợp gồm Zn và Cu tác dụng với lượng dư dung dịch axit HCL , thu được 4,48 lít khí H2 (đktc) . Sau phản ứng thấy còn 19,5 gam một chất rắn không tan. Tính thành phần % về khối lượng mỗi kim loại trong hỗn hợp.
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: Zn + 2HCl -->ZnCl2 + H2
____0,2<----------------------0,2
=> mZn = 0,2.65 = 13 (g)
mCu = mrắn không tan = 19,5 (g)
\(\left\{{}\begin{matrix}\%Zn=\dfrac{13}{13+19,5}.100\%=40\%\\\%Cu=\dfrac{19,5}{13+19,5}.100\%=60\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
`n_(H_2)=4,48/22,4=0,2 (mol)`
Ta có PTHH: `Zn+2HCl --> ZnCl_2 +H_2`
Theo PT: `1`--------------------------------`1`
Theo đề: `0,2`------------------------------`0,2`
`m_(Zn)=0,2.65=13(g)`
Vì `Cu` không phản ứng với `HCl` nên `m_(chất rắn không tan)=m_(Cu)=19,5(gam)`
`%Zn=13/(13+19,5) .100%=40%`
`%Cu=100%-40%=60%`
Đúng 0
Bình luận (0)