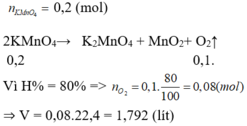Nhiệt phân 31.6g KMnO4 thu được 1,68 lít O2 (đktc) và m gam chất rắn . Tính hiệu suất của phản ứng và m

Những câu hỏi liên quan
Nung m gam KMnO4 một thời gian thu được 116,8 g chất rắn và 6,72 lít O2.Tính hiệu suất phản ứng nhiệt phân KMnO4
nO2 = 6.72/22.4 = 0.3 (mol)
BTKL :
mKMnO4 = 116.8 + 0.3*32 = 126.4 (g)
nKMnO4 = 126.4/158 = 0.8 (mol)
2KMnO4 -to-> K2MnO4 + MnO2 + O2
0.6_________________________0.3
H% = 0.6/0.8 * 100% = 75%
Đúng 1
Bình luận (0)
\(n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol) \\m = m_{chất\ rắn} + m_{O_2} = 116,8 + 0,3.32 = 126,4(gam)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,3.2 = 0,6(mol)\\ H = \dfrac{0,6.158}{126,4}.100\%= 75\%\)
Đúng 1
Bình luận (0)
Nung 15,8g KMnO4 thu được 0,784 lít O2 ở đktc. Xác định hiệu suất phản ứng nhiệt phân và số mol mỗi chất rắn sau phản ứng?
Nhiệt phân 31.6g KMnO4 được 29,04g chất rắn . Tính hiệu suất của phản ứng nhiệt phân
PTHH :
2KMnO4 -----> K2MnO4 + MnO2 + O2
x...........................x/2...............x/2............x/2
Gọi x là số mol KMnO4 phản ứng
=> mK2MnO4 = 98,5x (g)
mMnO2 = 43,5x (g)
mKMnO4 (dư) = 31,6 - 158x (g)
=> mCR (sau) = 98,5x + 43,5x + 31,6 - 158x
=> 29,04 = -16x + 31,6
=> 2,56 = 16x
=> 0,16 = x (mol)
Theo đề bài :
mKMnO4 = 31,6 (g)
=> nKMnO4 = 31,6 : 158 = 0,2 (mol)
=> H% = 0,16 : 0,2 . 100% = 80 %
Đúng 3
Bình luận (1)
Nhiệt phân 31,6 gam KMnO4 một thời gian thu được 29,2 gam chất rắn và V lít o2 hiệu suất phản ứng
mO2 = 31,6 - 29,2 = 2,4 g
nO2 = 2,4/32 = 0,075 mol
2KMnO4 → K2MnO4 + MnO2 + O2
0,15 ← 0,075
mKMnO4 = 0,15.158 = 23,7 g
H = \(\dfrac{23,7}{31,6}\)= 75%
Đúng 0
Bình luận (2)
Nhiệt phân hoàn toàn 31,6 gam KMnO4, thu được V lít O2 (đktc), biết hiệu suất phản ứng 80%. Giá trị của V là
A. 2,24
B. 1,792
C. 10,08
D. 8,96
nung nóng 63,2g KMnO4 thu được 3,36 lít khí (đktc) và được chất rắn B
a) tính hiệu suất phản ứng nhiệt phân
b) tính % khối lượng mỗi hợp chất trong B
a) $n_{O_2} = 0,15(mol)$
\(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
0,3 0,15 0,15 0,15 (mol)
$H = \dfrac{0,15.158}{63,2}.100\% = 37,5\%$
b)
$m_B = 63,2 - 0,15.32 = 58,4(gam)$
$\%m_{K_2MnO_4} = \dfrac{0,15.197}{58,4}.100\% = 50,59\%$
$\%m_{MnO_2} = \dfrac{0,15.87}{58,4}.100\% = 22,35\%$
$\%m_{KMnO_4\ dư} = 100\% -50,59\% -22,35\% = 27,06\%$
Đúng 1
Bình luận (0)
Nung nóng 79 gam KMnO4. Sau một thời gian thu được 3,36 lít khí (đktc) thì dừng lại, thu được chất rắn A
1. Tính số gam của A và hiệu suất phản ứng nhiệt phân
2. Tính phần trăm khối lượng của mỗi hợp chất trong A
3. Hòa tan hoàn toàn A vào acid HCl đặc, dư để phản ứng hoàn toàn. Tính thể tích khí bay ra (đktc)
1) \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
mA = mKMnO4(bđ) - mO2 = 79 - 0,15.32 = 74,2 (g)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3<-----------0,15<----0,15<---0,15
=> \(H=\dfrac{0,3.158}{79}.100\%=60\%\)
2)
\(\left\{{}\begin{matrix}\%m_{K_2MnO_4}=\dfrac{0,15.197}{74,2}.100\%=39,825\%\\\%m_{MnO_2}=\dfrac{0,15.87}{74,2}.100\%=17,588\%\\\%m_{KMnO_4\left(không.pư\right)}=\dfrac{79-0,3.158}{74,2}.100\%=42,587\%\end{matrix}\right.\)
3) \(n_{KMnO_4\left(không.pư\right)}=\dfrac{79}{158}-0,3=0,2\left(mol\right)\)
PTHH: 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,2----------------------------------->0,5
K2MnO4 + 8HCl --> 2KCl + MnCl2 + 2Cl2 + 4H2O
0,15-------------------------------->0,3
MnO2 + 4Hcl --> MnCl2 + Cl2 + 2H2O
0,15------------------->0,15
=> \(V_{Cl_2}=22,4\left(0,5+0,3+0,15\right)=21,28\left(l\right)\)
Đúng 3
Bình luận (2)
\(n_{KMnO_4}=\dfrac{79}{158}=0,5mol\)
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,5 0,15
a)\(m_{KMnO_4}=0,15\cdot197=29,55g\)
\(m_{MnO_2}=0,15\cdot87=13,05g\)
\(m_{CRắn}=m_{KMnO_4}+m_{MnO_2}=29,55+13,05=42,6g\)
\(n_{KMnO_4pư}=0,15\cdot2=0,3mol\)
\(H=\dfrac{0,3}{0,5}\cdot100\%=60\%\)
b)\(m_{O_2}=0,15\cdot32=4,8g\)
\(\%m_{K_2MnO_4}=\dfrac{29,55}{42,6}\cdot100\%=69,37\%\)
\(\%m_{MnO_2}=100\%-69,37\%=30,63\%\)
Đúng 1
Bình luận (0)
nhiệt phân 31.6g KMn04 thu đc 1.792 lít 02 đktc tính hiệu suất của phản ứng
Có: \(M_{KMnO_4}=39+55+16.4=158\left(đvc\right)\)
\(\Rightarrow n_{KMnO_4}=\dfrac{m_{KMnO_4}}{M_{KMnO_4}}=\dfrac{31,6}{158}=0,2\)(g/mol)
\(n_{O_2}=\dfrac{V_{O_2}}{22,4}=\dfrac{1,792}{22,4}=0,08\)
Ta có \(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
| Theo phương trình | 2 | 1 | 1 | 1 |
| Theo bài ra | 0,2(mol) | 0,08(mol) | ||
| Phản ứng | 0,16(mol) | 0,08(mol) | ||
| sau phản ứng | 0,04(mol) | 0(mol) |
Số gam \(KMnO_4\) theo lý thuyết phản ứng là 31,6 ( gam)
Số gam \(KMnO_4\) theo thực tế phản ứng là 0,16.158=25,28 (gam)
Hiệu suất của phản ứng là \(\dfrac{25,28}{31,6}.100\%=80\%\)
Vậy hiệu suất của phản ứng là 80%
Đúng 1
Bình luận (0)
Sửa đề: 31,5 gam KMnO4
PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{O_2\left(lý.thuyết\right)}=\dfrac{1}{2}n_{KMnO_2}=\dfrac{1}{2}\cdot\dfrac{31,5}{126}=0,25\left(mol\right)\\n_{O_2\left(thực\right)}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow H\%=\dfrac{0,08}{0,25}\cdot100\%=32\%\)
Đúng 1
Bình luận (0)
Cho phương trình 2KMnO4 →to→K2MnO4 + MnO2 +O2 ↑
Nhiệt phân 31,6 gam KmnO4 , thu được V lít O2 (đktc) biết hiệu suất phản ứng là 80% . Giá trị của V là bao nhiêu ?
\(n_{KMnO_4\left(lt\right)}=\dfrac{31.6}{158}\cdot80\%=0.16\left(mol\right)\)
\(2KMnO_4\underrightarrow{^{^{t^0}}}K_2MnO_4+MnO_2+O_2\)
\(0.16.............................................0.08\)
\(V_{O_2}=0.08\cdot22.4=1.792\left(l\right)\)
Đúng 3
Bình luận (0)
n KMnO4 = 31,6/158 =0,2(mol)
$2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2$
n O2(lt) = 1/2 n KMnO4 = 0,1(mol)
n O2(tt) = 0,1.80% = 0,08(mol)
V O2 = 0,08.22,4 = 1,792 lít
Đúng 2
Bình luận (0)