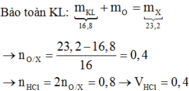nung nóng 16,8 gam hỗn hợp gồm Mg,Al,Cu,Zn với 1 lượng dư khí O2 thu được 23,2 gam chất rắn X.Cần V ml dung dịch HCl 2M (vừa đủ) đee hòa tan X.Biết các phản ứng xảy ra hoàn toàn.Giá trị của V là

Những câu hỏi liên quan
Nung nóng 16,8 gam hỗn hợp gồm Mg, Cu, Al với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X (MgO, CuO, Al2O3). Tính thể tích dung dịch HCl 2M vừa đủ để hòa tan hết chất rắn X ?
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$2Cu + O_2 \xrightarrow{t^o} 2CuO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$MgO + 2HCl \to MgCl_2 + H_2O$
$CuO + 2HCl \to CuCl_2 + H_2O$
$Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O$
Gọi $n_{MgO} = a(mol) ; n_{CuO} = b(mol) ; n_{Al_2O_3} = c(mol)$
Bảo toàn khối lượng : $m_{O_2} = 23,2 - 16,8 = 6,4(gam)$
$n_{O_2} = 0,2(mol)$
$\Rightarrow 0,5a + 0,5b + 1,5c = 0,2(1)$
Theo PTHH :
$n_{HCl} =2 n_{MgO} + 2n_{CuO} + 6n_{Al_2O_3} = 0,8(theo (1))$
Suy ra : $V_{dd\ HCl} = \dfrac{0,8}{2} = 0,4(lít)$
Đúng 1
Bình luận (0)
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản ứng với chất rắn X là: A. 400 ml B. 200 ml C. 800 ml D. 600 ml
Đọc tiếp
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản ứng với chất rắn X là:
A. 400 ml
B. 200 ml
C. 800 ml
D. 600 ml
Đáp án A
mO = 23,2 – 16,8 = 6,4g ⇒ nO= 0,4 mol
2H+ + O2- → H2O
⇒ nHCl = 2nO = 2. 0,4 = 0,8 mol
⇒ VHCl = 0,8/2 = 0,4l = 400ml
Đúng 0
Bình luận (0)
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản ứng với chất rắn X là A. 400 ml. B. 600 ml. C. 200 ml. D. 800 ml.
Đọc tiếp
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản ứng với chất rắn X là
A. 400 ml.
B. 600 ml.
C. 200 ml.
D. 800 ml.
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản ứng với chất rắn X là A. 400 ml B. 600 ml. C. 200 ml D. 800 ml
Đọc tiếp
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản ứng với chất rắn X là
A. 400 ml
B. 600 ml.
C. 200 ml
D. 800 ml
Nung nóng 16,8 gam hỗn hợp Au, Ag, Cu, Fe, Zn với một lượng dư khí O2 , đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản úng với chất rắn X là A. 600 m B. 200 ml C. 800 ml D. 400 ml
Đọc tiếp
Nung nóng 16,8 gam hỗn hợp Au, Ag, Cu, Fe, Zn với một lượng dư khí O2 , đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dung dịch HCl 2M vừa đủ để phản úng với chất rắn X là
A. 600 m
B. 200 ml
C. 800 ml
D. 400 ml
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dd HCl 2M vừa đủ để phản ứng với chất rắn X là: A. 600 ml B. 200 ml C. 800 ml D. 400 ml
Đọc tiếp
Nung nóng 16,8 gam hỗn hợp gồm Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thể tích dd HCl 2M vừa đủ để phản ứng với chất rắn X là:
A. 600 ml
B. 200 ml
C. 800 ml
D. 400 ml
nHCl = nCl- = 2nO = (23,2 - 16,8).2 : 18 = 0,8-> V = 400ml
=> Đáp án A
Đúng 0
Bình luận (0)
Nung nóng 16,8 gam hỗn hợp Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thế tích dung dịch H2SO4 0,1M vừa đủ để phản ứng với chất rắn X là A. 6 lít. B. 2 lít. C. 8 lít. D. 4 lít.
Đọc tiếp
Nung nóng 16,8 gam hỗn hợp Au, Ag, Cu, Fe, Zn với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X. Thế tích dung dịch H2SO4 0,1M vừa đủ để phản ứng với chất rắn X là
A. 6 lít.
B. 2 lít.
C. 8 lít.
D. 4 lít.
Đáp án D
Các phương trình phản ứng:
Hỗn hợp kim loại tác dụng với oxi:
Au, Ag không tác dụng với oxi
![]()
Phương trình phản ứng :
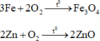
Rắn X gồm Au, Ag, CuO, Fe3O4 và ZnO tác dụng với dung dịch H2SO4 loãng:
Au, Ag không tác dụng với dung dịch H2SO4 loãng
![]()
Phương trình phản ứng
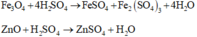
Tính toán:
Gọi M là kim loại chung cho Cu, Fe và Zn với hóa trị n
Sơ đồ phản ứng :
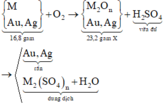
Bảo toàn khối lượng cho giai đoạn hỗn hợp kim loại tác dụng với oxi:
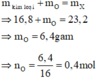
Theo sơ đồ thì cuối cùng O chuyển hết về O trong H2O. Bảo toàn nguyên tố O ta có:
n H 2 O = n O ⇒ n H 2 O = 0 , 4 mol
Bảo toàn nguyên tố H ta có:
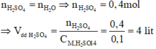
Đúng 0
Bình luận (0)
Nung nóng 19 gam hỗn hợp Fe, Al, Zn, Mg với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 27 gam chất rắn X. Thể tích dung dịch H2SO4 1M vừa đủ để phản ứng với chất rắn X là A. 800 ml. B. 200 ml. C. 500 ml. D. 400 ml.
Đọc tiếp
Nung nóng 19 gam hỗn hợp Fe, Al, Zn, Mg với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 27 gam chất rắn X. Thể tích dung dịch H2SO4 1M vừa đủ để phản ứng với chất rắn X là
A. 800 ml.
B. 200 ml.
C. 500 ml.
D. 400 ml.
Ta có nO = (27-19) : 16 = 0,5
=> nH2SO4 = 0,5 mol
=> V = 500ml
=> Đáp án C
Đúng 0
Bình luận (0)
Nung nóng m gam hỗn hợp X gồm Mg, Al, Cu trong O2 dư, thu được 16,2 gam hỗn hợp Y gồm các oxit. Hòa tan hết Y bằng lượng vừa đủ dung dịch HCl thu được dung dịch chứa 38,2 gam muối. Biết các pứ xảy ra hoàn toàn.a) Tính giá trị mb) hòa tan hết 16,2 gam hỗn hợp Y bằng một lượng dung dịch vừa đủ gồm HCl 1M và H2SO4 0,5M thu được dung dịch chứa a gam muối ( không có muối axit). tính giá trị a
Xem chi tiết
\(a.\\ m+m_{\left[O\right]}=16,2\\ n_{Cl^-}=2\dfrac{m_{\left[O\right]}}{16}\\ m+35,5\dfrac{m_{\left[O\right]}}{16}\cdot2=38,2\\ m=9,8;m_{\left[O\right]}=6,4\\ b.\\ V_{dd.acid}=v\left(L\right)\\ n_{H^+}=v+v=2v\left(mol\right)\\ n_{\left[O\right]}=\dfrac{6,4}{16}=0,4=\dfrac{2v}{2}\\ v=0,4\\ a=9,8+0,4\cdot35,5+0,4\cdot96=62,4g\)
Đúng 0
Bình luận (1)
`a)`
Bảo toàn KL:
`m_Y+m_{HCl}=m_{\text{muối}}+m_{H_2O}`
`->36,5n_{HCl}-18n_{H_2O}=38,2-16,2=22`
Mà bảo toàn H: `n_{HCl}=2n_{H_2O}`
`->n_{HCl}=0,8(mol);n_{H_2O}=0,4(mol)`
Bảo toàn O: `n_{O(Y)}=n_{H_2O}=0,4(mol)`
`->n_{O_2}=0,5n_{O(Y)}=0,2(mol)`
Bảo toàn KL: `m_X+m_{O_2}=m_Y`
`->m=16,2-0,2.32=9,8(g)`
`b)`
Đặt `V_{dd\ ax it}=x(l)`
`->n_{HCl}=x(mol);n_{H_2SO_4}=0,5x(mol)`
`n_{O(Y)}=0,4(mol)`
Bảo toàn electron: `n_{O(Y)}=1/2n_{H(ax it)}`
`->0,4=1/2(x+0,5x.2)`
`->x=0,4(l)`
`->n_{HCl}=0,4(mol);n_{H_2SO_4}=0,2(mol)`
Bảo toàn O: `n_{H_2O}=n_{O(Y)}=0,4(mol)`
Bảo toàn KL:
`m_Y+m_{HCl}+m_{H_2SO_4}=m_{\text{muối}}+m_{H_2O}`
`->a=16,2+0,4.36,5+0,2.98-0,4.18=43,2(g)`
Đúng 0
Bình luận (1)