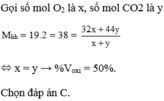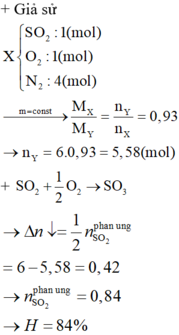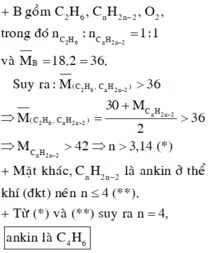Hỗn hợp X gồm oxi và clo có tỉ khối so với heli là 14. Khối lượng mol trung bình của hỗn hợp khí X tỷ lệ % theo thể tích của O2 trong hỗn hợp X là?

Những câu hỏi liên quan
Một hỗn hợp khí O 2 và C O 2 có tỷ khối so với hiđro là 19. Khối lượng mol trung bình của hỗn hợp khí trên và tỷ lệ % theo thể tích của O 2 là
A. 40 g/mol và 40%.
B. 38 g/mol và 40%.
C. 38 g/mol và 50%.
D. 36 g/mol và 50%.
Một hỗn hợp X gồm CH4 và O2 (không có phản ứng xảy ra) có tỉ khối so với hidro là 11,68. a/ Tính khối lượng mol trung bình của hỗn hợp. b/Tính thành phần phần trăm theo thể tích của mỗi khí trong hỗn hợp.c/ Chứng minh rằng hỗn hợp luôn nặng hơn H2.
Đọc tiếp
Một hỗn hợp X gồm CH4 và O2 (không có phản ứng xảy ra) có tỉ khối so với hidro là 11,68.
a/ Tính khối lượng mol trung bình của hỗn hợp.
b/Tính thành phần phần trăm theo thể tích của mỗi khí trong hỗn hợp.
c/ Chứng minh rằng hỗn hợp luôn nặng hơn H2.
Hỗn hợp khí X gồm SO2 và không khí có tỉ lệ thể tích tương ứng là 1:5. Đun nóng hỗn hợp X với xúc tác V2O5 trong một bình kín có dung tích không đổi thu được hỗn hợp khí Y. Tỉ khối hơi của X so với Y là 0,93. Không khí có 20% thể tích là O2 và 80% thể tích là N2. Hiệu suất của phản ứng oxi hóa SO2 là A. 84%. B. 75%. C. 80%. D. 42%.
Đọc tiếp
Hỗn hợp khí X gồm SO2 và không khí có tỉ lệ thể tích tương ứng là 1:5. Đun nóng hỗn hợp X với xúc tác V2O5 trong một bình kín có dung tích không đổi thu được hỗn hợp khí Y. Tỉ khối hơi của X so với Y là 0,93. Không khí có 20% thể tích là O2 và 80% thể tích là N2. Hiệu suất của phản ứng oxi hóa SO2 là
A. 84%.
B. 75%.
C. 80%.
D. 42%.
1) Có một hỗn hợp khí gồm oxi và ozon. Hỗn hợp khí này có tỉ khối đối vs hidro là 18. Hãy xác đimhj thành phần phần trăm theo thể tích của hỗn hợp khí2) Hỗn hợp khí A gồm O2 và O3, tỉ khối hơi của hỗn hợp khí A và khí H2 là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hh khí B đối vs H2 là 3,6.@a) Tính thành phần % theo thể tích của mỗi khí có trong hh khí A và Bb) Một mol khí A có thể đốt cháy hoàn toàn bao nhiêu mol khí COGiải theo pp tăng giảm khối lượng hoặc phương pháp trung bình
Đọc tiếp
1) Có một hỗn hợp khí gồm oxi và ozon. Hỗn hợp khí này có tỉ khối đối vs hidro là 18. Hãy xác đimhj thành phần phần trăm theo thể tích của hỗn hợp khí
2) Hỗn hợp khí A gồm O2 và O3, tỉ khối hơi của hỗn hợp khí A và khí H2 là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hh khí B đối vs H2 là 3,6.
@
a) Tính thành phần % theo thể tích của mỗi khí có trong hh khí A và B
b) Một mol khí A có thể đốt cháy hoàn toàn bao nhiêu mol khí CO
Giải theo pp tăng giảm khối lượng hoặc phương pháp trung bình
Hỗn Hợp X gồm các khí SO2 và O2, tỉ khối của X so với H2 là 24. Ở đktc thể tích của hỗ hợp X là 13,44 lít
1. Tính Khối Lượng của Hỗn Hợp X
2. Tính thành phần % theo thể tích mỗi khí có trong X
3. Tính Khối lượng các chất trong X
\(n_{hh}=\dfrac{13,44}{22,4}=0,6mol\)
\(\overline{M_x}=24.2=48\)
\(\left\{{}\begin{matrix}SO_2:64\\O_2:32\end{matrix}\right.\) 48 = \(\dfrac{16}{16}=1\)
\(\Rightarrow n_{SO_2=}n_{O_2}=0,3mol\)
1. \(m_{hh}=0,3.64+0,3.32=28,8g\)
2. \(\%V_{SO_2}=\dfrac{0,3.22,4}{13,44}.100\%=50\%\)
\(\Rightarrow\%V_{O_2}=50\%\)
3. \(m_{SO_2}=0,3.64=19,2g\)
\(m_{O_2}=0,3.32=9,6g\)
Đúng 2
Bình luận (0)
Trong một bình kín dung tích không đổi chứa hỗn hợp A gồm etan và một ankin X (thể khí ở điều kiện thường) có tỉ lệ số mol là 1 : 1. Thêm oxi vào bình thì được hỗn hợp khí B có tỉ khối so với hiđro là 18. Đốt cháy hoàn toàn hỗn hợp B sau đó đưa bình về 0oC thấy hỗn hợp khí Z trong bình có tỉ khối so với hiđro là 21,4665. X là A. C2H2. B. C3H4. C. C4H6. D. C5H8.
Đọc tiếp
Trong một bình kín dung tích không đổi chứa hỗn hợp A gồm etan và một ankin X (thể khí ở điều kiện thường) có tỉ lệ số mol là 1 : 1. Thêm oxi vào bình thì được hỗn hợp khí B có tỉ khối so với hiđro là 18. Đốt cháy hoàn toàn hỗn hợp B sau đó đưa bình về 0oC thấy hỗn hợp khí Z trong bình có tỉ khối so với hiđro là 21,4665. X là
A. C2H2.
B. C3H4.
C. C4H6.
D. C5H8.
Một hỗn hợp X gồm H2 và O2 (ko cs phản ứng xảy ra) có tỉ khối so vs ko khí là 0,3276
a) Tính khối lượng mol trung bình của hỗn hợp
b) Tính thành phần phần trăm theo số mol của mỗi khí trong hỗn hợp (= 2 cách khác nhau)
theo đề ra ta có
dx/kok = \(\dfrac{M_X}{29}\) = 0,3276 => Mx =9,5
gọi x và y lần lượt là số mol của H2 và O2
nx = x + y
mx = 2x + 32y
\(\overline{M}\) = \(\dfrac{2x+32y}{x+y}=9,2\)
x = 22,5 y =77,5
Đúng 0
Bình luận (0)
1)Đốt cháy hoàn toàn m gam cacbon trong V lít khí oxi(đktc), thu được hỗn hợp khí A có tỉ khối hơi với oxi là 1,25. a) Xác định thành phần phần trăm theo thể tích các khí có trong hỗn hợp A. b) Tính m và V. Biết rằng khi dẫn hỗn hợp khí A vào bình đựng dung dịch Ca(OH)2 dư tạo thành 6g kết tủa trắng.2) Hỗn hợp khí A gồm có O2 và O3 tỉ khối hơi đối với hiđrô là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hỗn hợp...
Đọc tiếp
1)Đốt cháy hoàn toàn m gam cacbon trong V lít khí oxi(đktc), thu được hỗn hợp khí A có tỉ khối hơi với oxi là 1,25. a) Xác định thành phần phần trăm theo thể tích các khí có trong hỗn hợp A. b) Tính m và V. Biết rằng khi dẫn hỗn hợp khí A vào bình đựng dung dịch Ca(OH)2 dư tạo thành 6g kết tủa trắng.
2) Hỗn hợp khí A gồm có O2 và O3 tỉ khối hơi đối với hiđrô là 19,2. Hỗn hợp khí B gồm có H2 và CO, tỉ khối của hỗn hợp khí B so với hidrô là 3,6. a) Tính thành phần phần trăm theo thể tích các khí trong hỗn hợp A và hỗn hợp B. b) Tính số mol hỗn hợp khí A cần dùng để đốt cháy hoàn toàn 1 mol hỗn hợp khí B. Các thể tích được đo ở cùng điều kiện nhiệt độ, áp suất.
Giải theo phương pháp tăng giảm khối lượng hoặc phương pháp trung bình
Hỗn hợp khí X gồm (CH4 ,CO2 ,O2) cùng đo ở điều kiện nhiệt độ và áp suất ,trong đó tỉ lệ số mol CH4 và CO2 lần lượt là 1:1 biết tỉ khối hỗn hợp X so với Hidro là 15,5
-tính phần trăm thể tích mỗi khí ý trong hỗn hợp X
-Tính phần trăm khối lượng mỗi khí trong hỗn hợp X