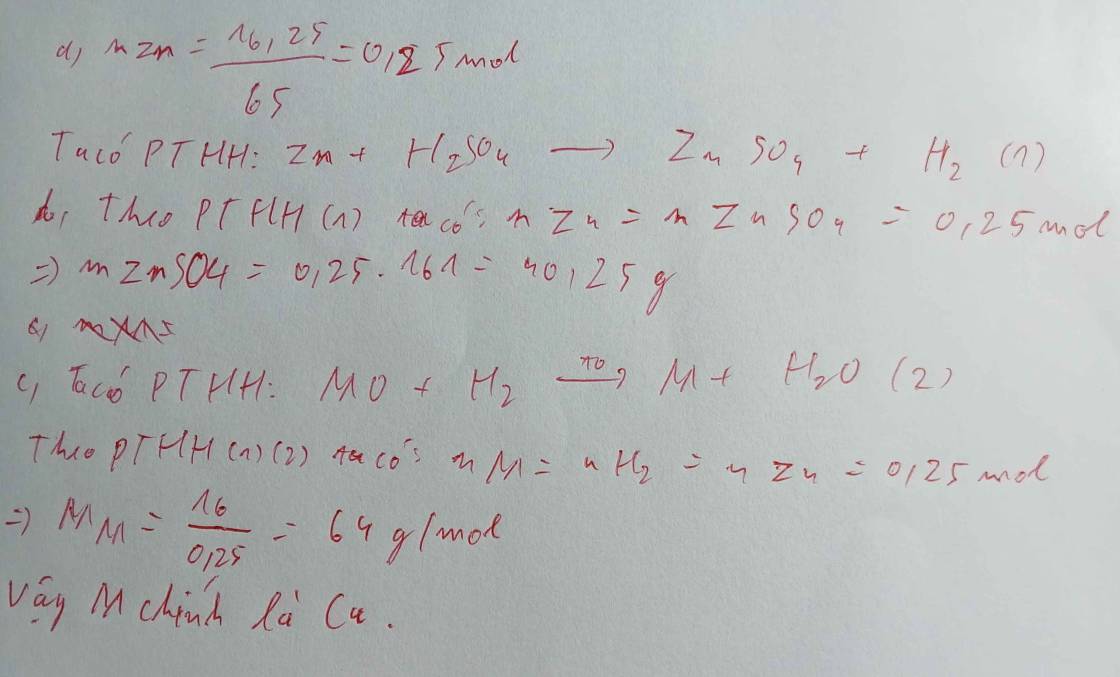cho 6,5 g kẽm phản ứng hoàn toàn với 200 ml dd axit sunfuric loãng sau phản ứng thu được ZnSO4 và hidro . a) viết phương trình phản ứng . b) tính V hidro .c) tính nồng độ mol của dd H2SO4 ở trên(nhờ các vị hảo hán giúp vs :))) )

Những câu hỏi liên quan
Cho 19,5 g Kẽm phản ứng hoàn toàn với dung dịch axit sunfuric loãng H2SO4 (dư). a/ Viết phương trình hóa học cho phản ứng trên. b/ Tính thể tích Hidro sinh ra (đktc). c/ Tính khối lượng muối ZnSO4 tạo ra. d/ Dẫn toàn bộ khí sinh ra ở trên đi qua 64 gam sắt (III)Oxit nung nóng, sau một thời gian thu được a gam chất rắn, biết hiệu suất phản ứng là 30%.Tính a gam.
Đọc tiếp
Cho 19,5 g Kẽm phản ứng hoàn toàn với dung dịch axit sunfuric loãng H2SO4 (dư).
a/ Viết phương trình hóa học cho phản ứng trên.
b/ Tính thể tích Hidro sinh ra (đktc).
c/ Tính khối lượng muối ZnSO4 tạo ra.
d/ Dẫn toàn bộ khí sinh ra ở trên đi qua 64 gam sắt (III)Oxit nung nóng, sau một thời gian thu được a gam chất rắn, biết hiệu suất phản ứng là 30%.Tính a gam.
a, \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
b, \(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
c, \(n_{ZnSO_4}=n_{Zn}=0,3\left(mol\right)\Rightarrow m_{ZnSO_4}=0,3.161=48,3\left(g\right)\)
d, \(n_{Fe_2O_3}=\dfrac{64}{160}=0,4\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Xét tỉ lệ: \(\dfrac{0,4}{1}>\dfrac{0,3}{3}\), ta được Fe2O3 dư.
Mà: H% = 30% \(\Rightarrow n_{H_2\left(pư\right)}=0,3.30\%=0,09\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{Fe}=\dfrac{2}{3}n_{H_2}=0,06\left(mol\right)\\n_{Fe_2O_3\left(pư\right)}=\dfrac{1}{3}n_{H_2}=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{Fe_2O_3\left(dư\right)}=0,4-0,03=0,37\left(mol\right)\)
\(\Rightarrow a=m_{Fe}+m_{Fe_2O_3\left(dư\right)}=62,56\left(g\right)\)
Đúng 1
Bình luận (0)
cho 16,25 game kẽm tác dụng hoàn toàn với axit sunfuric loãng (H2SO4) , sau phản ứng thu được muối ZnSO4 , khí Hidro (dktc)
a) viết pthh
b) tính khối lg muối thu được
c) dẫn toàn bộ khí hidro thu được ở trên đi qua oxit MO dư, đun nóng. sau phản ứng thu được 16 gam khối lượng M. xác định M là kim loại nào
Hòa Tan hoàn toàn 7,2 g kim loại Mg vào 200 ml dd axit clohidric ( HCL ) sau phản ứng thu được magie clorua MgCl2 và khí hidro ( đktc )
a viết PTHH
b tính khối lượng magie clorua tạo thành
c tính nồng độ mol của dd axit đã dùng
a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, \(m_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
Theo PT: \(n_{MgCl_2}=n_{Mg}=0,3\left(mol\right)\Rightarrow m_{MgCl_2}=0,3.95=28,5\left(g\right)\)
c, \(n_{HCl}=2n_{Mg}=0,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,2}=3\left(M\right)\)
Đúng 2
Bình luận (0)
cho 10,4 g hỗn hợp 2 kim loại Fe và Mg tác dụng hoàn toàn với 200 ml dung dịch axit sunfuric loãng sau phản ứng thu được 6,72l khí hidro (ở đktc). Tính a) Khối lượng mỗi kim loại hỗn hợp ban đầu b) Nồng độ mol của dung dịch axit đã dùng
Gọi x, y lần lượt là sô mol của Fe và Mg
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH:
Fe + H2SO4 ---> FeSO4 + H2 (1)
Mg + H2SO4 ---> MgSO4 + H2 (2)
a. Theo PT(1): \(n_{H_2}=n_{Fe}=x\left(mol\right)\)
Theo PT(2): \(n_{H_2}=n_{Mg}=y\left(mol\right)\)
\(\Rightarrow x+y=0,3\) (*)
Theo đề, ta có: 56x + 24y = 10.4 (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}x+y=0,3\\56x+24y=10,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right);m_{Mg}=0,2.24=4,8\left(g\right)\)
b. Ta có: \(n_{hh}=0,1+0,2=0,3\left(mol\right)\)
Theo PT(1,2): \(n_{H_2SO_4}=n_{hh}=0,3\left(mol\right)\)
Đổi 200ml = 0,2 lít
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,3}{0,2}=1,5M\)
Đúng 0
Bình luận (0)
cho 6,5 gam kẽm phản ứng hoàn toàn với dung dịch HCl thu được 6ml dung dịch muối kẽm clorua cà khí hidroa) viết phương trình hóa học cho phản ứng trênb) tính nồng độ mol của muối kẽm thu được và thể tích khí hidro sinh rac) nếu cho toàn bộ lượng khí hidro sinh ra ở phản ứng trén tác dụng với 2,24 lít khí oxi thì chất nào dư bao nhiêu (cho biết các khí đo ở cùng điều kiện tiêu chuẩn )biết Zn65H1 O16
Đọc tiếp
cho 6,5 gam kẽm phản ứng hoàn toàn với dung dịch HCl thu được 6ml dung dịch muối kẽm clorua cà khí hidro
a) viết phương trình hóa học cho phản ứng trên
b) tính nồng độ mol của muối kẽm thu được và thể tích khí hidro sinh ra
c) nếu cho toàn bộ lượng khí hidro sinh ra ở phản ứng trén tác dụng với 2,24 lít khí oxi thì chất nào dư bao nhiêu (cho biết các khí đo ở cùng điều kiện tiêu chuẩn )
biết Zn=65
H=1
O=16
a,\(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,1--------------->0,1------>0,1
b, => \(\left\{{}\begin{matrix}C_{M\left(ZnCl_2\right)}=\dfrac{0,1}{\dfrac{6}{1000}}=\dfrac{50}{3}M\\V_{H_2}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
c, \(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
LTL: \(\dfrac{0,1}{2}< 0,1\)=> O2 dư
Theo pt: \(n_{O_2}=\dfrac{1}{2}n_{H_2}=\dfrac{1}{2}.0,1=0,05\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{O_2\left(dư\right)}=\left(0,1-0,05\right).32=1,6\left(g\right)\\V_{O_2\left(dư\right)}=\left(0,1-0,05\right).22,4=1,12\left(l\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 13g kẽm phản ứng hoàn toàn vừa đủ với dung dịch axit sunfuric 20 %a. Tính thể tích khí hidro sinh ra ( đktc ) b.Tính khối lượng dung dịch axit sunfuric cần dùng c. Tính nồng độ mol của dd axit sunfuric biết khối lượng riêng của axit là 1,14 g / mlMk cần gấp câu c ạ!!!!! Thanks trc
Đọc tiếp
Cho 13g kẽm phản ứng hoàn toàn vừa đủ với dung dịch axit sunfuric 20 %
a. Tính thể tích khí hidro sinh ra ( đktc ) b.Tính khối lượng dung dịch axit sunfuric cần dùng c. Tính nồng độ mol của dd axit sunfuric biết khối lượng riêng của axit là 1,14 g / ml
Mk cần gấp câu c ạ!!!!! Thanks trc![]()
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH: Zn + H2SO4 ---> ZnSO4 + H2
0,2--->0,2--------->0,2------>0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\\ m_{H_2SO_4}=\dfrac{0,2.98}{20\%}=98\left(g\right)\\ \rightarrow V_{ddH_2SO_4}=\dfrac{98}{1,14}=86\left(ml\right)=0,086\left(l\right)\\ \rightarrow C_{M\left(H_2SO_4\right)}=\dfrac{0,2}{0,086}=2,33M\)
Đúng 1
Bình luận (0)
Cho 3,6 gam magie phản ứng hoàn toàn với dung dịch axit sunfuric loãng (H2SO4) a.Viết phương trình phản ứng xảy ra và tính thể tích hidro thu được ở đktc. b. Cho lượng khí H2 thu được tác dụng hết với CuO. Hỏi sau phản ứng thu được bao nhiêu gam Cu?
Đọc tiếp
Cho 3,6 gam magie phản ứng hoàn toàn với dung dịch axit sunfuric loãng (H2SO4)
a.Viết phương trình phản ứng xảy ra và tính thể tích hidro thu được ở đktc.
b. Cho lượng khí H2 thu được tác dụng hết với CuO. Hỏi sau phản ứng thu được bao nhiêu gam Cu?
a)
\(Mg + H_2SO_4 \to MgSO_4 + H_2\\ n_{H_2} = n_{Mg} = \dfrac{3,6}{24} = 0,15(mol)\\ b)\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{Cu} = n_{H_2} = 0,15(mol)\\ \Rightarrow m_{Cu} = 0,15.64 = 9,6(gam)\)
Đúng 4
Bình luận (0)
a, Theo gt ta có: $n_{Mg}=0,15(mol)$
$Mg+H_2SO_4\rightarrow MgSO_4+H_2$
Ta có: $n_{H_2}=n_{Mg}=0,15(mol)\Rightarrow V_{H_2}=3,36(l)$
b, $CuO+H_2\rightarrow Cu+H_2O$
Do đó $n_{Cu}=0,15(mol)\Rightarrow m_{Cu}=9,6(g)$
Đúng 2
Bình luận (0)
a. PTPƯ: Mg + \(H_2SO_4\) ---> \(MgSO_4\) + \(H_2\) (Lập và cân bằng phương trình)
0,15 mol 0,15 mol 0,15 mol 0,15 mol
+ Số mol của Mg:
\(n_{Mg}\) = \(\dfrac{m}{M}\) = \(\dfrac{3,6}{24}\) = 0,15 (mol)
+ Thể tích của \(H_2\)
\(V_{H_2}\) = n . 22,4 = 0,15 . 22,4 = 3,36 (lít)
b. CuO + \(H_2\) ---> Cu + \(H_2O\) (Lập một phương trình mới)
0,3 mol 0,3 mol 0,1 mol 0,3 mol
+ Số g sau phản ứng của Cu:
\(m_{Cu}\) = n . M = 0,3 . 64 = 19,2 (g)
________________________________
Có gì không đúng thì nhắn mình nha bạn :))
Đúng 1
Bình luận (1)
Hòa tan hoàn toàn 6,5 gam kim loại kẽm bằng 1 lượng vừa đủ dung dịch axit clohidric (HCl), sau phản ứng thu được khí Hidro và muối kẽm clorua (ZnCl2).
a) Viết phương trình hóa học xảy ra?
b) Tính thể tích khí hidro thu được sau phản ứng ở đktc?
c) Tính khối lượng HCl đã phản ứng?
a. \(n_{Zn}=\dfrac{6.5}{65}=0,1\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,1 0,2 0,1
b. \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
c. \(m_{HCl}=0,2.36,5=7,3\left(g\right)\)
Đúng 4
Bình luận (0)
\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1
\(V_{H_2}=0,1\cdot22,4=2,24l\)
\(m_{HCl}=0,2\cdot36,5=7,3g\)
Đúng 2
Bình luận (0)
Cho m (g) Kẽm tác dụng vừa đủ với 150 ml dd HCl 4M a, Viết phương trình phản ứng và tính thể tích H2 thu được ở đktc b. Tính giá trị m. C. Tính nồng độ mol/l của dung dịch thu được sau phản ứng.
a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{HCl}=0,15.4=0,6\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b, \(n_{Zn}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\Rightarrow m_{Zn}=0,3.65=19,5\left(g\right)\)
c, \(n_{ZnCl_2}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\Rightarrow C_{M_{ZnCl_2}}=\dfrac{0,3}{0,15}=2\left(M\right)\)
Đúng 2
Bình luận (0)