Cho sơ đồ phản ứng sau:
A→B+C
B+H2O→D
D+C→A+H2O
Biết rằng hợp chất A chứa 3 nguyên tố Ca, C, O với tỉ lệ canxi chiếm 40%, ôxi 48%, cacbon 12% về khối lượng.
(。^▽^)
cho sơ đồ phản ứng sau:
A--->B+C
B+H2O---->D
D+C---->A+H2O
Biết rằng hợp chất A chứa 3 nguyên tố CA, C, O với tỉ lệ canxi chiếm 40%, ỗi 48%, cacbon12% về khối lượng
bài này mk ko hỉu lắm
@Hoàng Thị Anh Thư chị ơi giảng hộ em vs
Các bạn giải cho mình bài này nhé :
Hợp chất A chứa 3 nguyên tố Ca, C, O với tỉ lệ 40% canxi, 12% cacbon, 48% oxi về khối lượng. Tìm CTHH của A.
Gọi CTHH của A là CaxCyOz
Theo đề bài ta có :
mCaxCyOz = 40x : 40% = 100x
mCaxCyOz = 12y : 12% = 100y
mCaxCyOz = 16z : 48% = 100z : 3
=> 100x = 100y =100z : 3
=> x = y = z : 3
=> x = 1 ; y = 1 ; z = 3
Ta có CTHH của A là CaCO3
Gọi công thức của A là Ca x C y O z thì ta có:
\(\Rightarrow\left\{\begin{matrix}40x=0,4\left(40x+12y+16z\right)\\12y=0,12\left(40x+12y+16z\right)\\16z=0,48\left(40x+12y+16z\right)\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}x=1\\y=1\\z=3\end{matrix}\right.\)
Vậy CT là CaCO3
Gọi CTHH là CaxCyOz
Theo bài ra ta có:
mca : mc : mo = %Ca : %C : %O
40x : 12y : 16z = 40 : 12 : 48
x : y : z = 40/40 : 12/12 : 48/16
x : y : z = 1 : 1 : 3
Lấy x=1; y=1; z=3
-> CTHH đơn giản nhất CaCo3
Cho sơ đồ phản ứng sau: A -> B + H2O
B + H2O -> D
D + C -> A + H2O
Biết rằng hỗn hợp A chứa 3 nguyên tố Ca,C,O với tỉ lệ Canxi là 40%, Oxi là 48% và Cacbon là 12% về khối lượng.
![]()
a) Hãy tìm CTHH đơn giản nhất của một loại ôxit của nitơ , biết rằng trong ôxit này có 7g nitơ kết hợp với 20g ôxi
b)Hợp chất A có thành phần % theo khối lượng các nguyên tố: 40% Ca, 12%C, 48% O
Các bạn giải từng bước bài này giúp mik nha ❤️❤️❤️
1. Cho 10(g) canxi cacbonat vào 200(g) dung dịch HCL 5%
A) viết phương trình phản ứng
B) tính C% các chất trong dung dịch thu được
2. Hợp chất A chứa 3 nguyên tố canxi , cacbon, oxi , có % về khối lượng của các canxi cacbon, oxi, lần lượt là 40%,12%,48%. Tìm công thức phân tử A
Câu 1:
\(a)pthh:CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\left(1\right)\)
b) \(n_{CaCO_3}=\dfrac{m}{M}=\dfrac{10}{100}=0,1\left(mol\right)\)
\(m_{HCl}=\dfrac{m_{d^2}\cdot C\%}{100}=\dfrac{200\cdot5}{100}=10\left(g\right)\\ \Rightarrow n_{HCl}=\dfrac{m}{M}=\dfrac{10}{36,5}=0,27\left(mol\right)\)
 \(\Rightarrow m_{HCl\left(dư\right)}=n\cdot M=0,07\cdot36,5=2,555\left(g\right)\\
m_{CaCl_2}=n\cdot M=0,1\cdot111=11,1\left(g\right)\\
m_{CO_2}=n\cdot M=0,1\cdot44=4,4\left(g\right)\)
\(\Rightarrow m_{HCl\left(dư\right)}=n\cdot M=0,07\cdot36,5=2,555\left(g\right)\\
m_{CaCl_2}=n\cdot M=0,1\cdot111=11,1\left(g\right)\\
m_{CO_2}=n\cdot M=0,1\cdot44=4,4\left(g\right)\)
\(\Rightarrow m_{d^2\text{ }sau\text{ }pứ}=\left(m_{CaCO_3}+m_{d^2\text{ }HCl}\right)-m_{CO_2}\\ =\left(10+200\right)-4,4=205,6\left(g\right)\)
\(\Rightarrow C\%\left(HCl_{dư}\right)=\dfrac{m_{HCl}\cdot100}{m_{d^2}}=\dfrac{2,555\cdot100}{205,6}=12,43\%\\C\%\left(CaCl_2\right)=\dfrac{m_{CaCl_2}\cdot100}{m_{d^2}}=\dfrac{11,1\cdot100}{205,6}=5,4\% \)
Câu 2:
Gọi CTHH của hợp chất là \(Ca_xC_yO_z\)
\(\text{Ta có tỉ lệ: }40x:12y:16z=40:12:48\\ \Rightarrow x:y:z=\dfrac{40}{40}:\dfrac{12}{12}:\dfrac{48}{16}\\ \Rightarrow x:y:z=1:1:3\\ \Rightarrow\left\{{}\begin{matrix}x=1\\y=1\\z=3\end{matrix}\right.\\ \Rightarrow Ca_xC_yO_z=CaCO_3\)
Vậy...........
Hợp chất A có khối lượng mol phân tử 100g, có thành phần các nguyên tố Ca, C , O với tỉ lệ về khối lượng %Ca = 40%, C =12% , O = 48%. Tìm công thức hóa học của A ?
Giả sử ta có CTHH : Ca\(_x\)C\(_y\)O\(_z\)
Theo đề bài, ta có:
m\(_{Ca}\)=%Ca.M\(_{Ca_x}\)\(_{C_y}\)\(_{O_z}\):100%=40%.100:100%=40(g)
n\(_{Ca}\)=\(\dfrac{m}{M}\)=\(\dfrac{40}{40}\)=1(mol)
m\(_C\)=%C.M\(_{Ca_xC_yO_z}\):100%=12%.100:100%=12(g)
n\(_C\)=\(\dfrac{m}{M}\)=\(\dfrac{12}{12}\)=1(mol)
m\(_O\)=101-(14+40)=49(g)
n\(_O\)=\(\dfrac{m}{M}\)=\(\dfrac{49}{16}\)=3(mol)
Vậy công thức hóa học là: CaCO\(_3\)
\(m_{Ca}=40\%\times100=40\left(g\right)\) => \(n_{Ca}=\dfrac{40}{40}=1\left(mol\right)\)
\(m_C=12\%\times100=12\left(g\right)=>n_C=\dfrac{12}{12}=1\left(mol\right)\)
\(m_O=48\%\times100=48\left(g\right)=>n_O=\dfrac{48}{16}=3\left(mol\right)\)
Vậy CTHH của A là: \(CaCO_3\)
\
-Khối lượng của mỗi nguyên có trong 1 mol hợp chất:
mCa=\(\frac{40.100}{100}\)=40 g
mC=\(\frac{12.100}{100}\)=12 g
mO=\(\frac{48.100}{100}\)=48 g
-Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất
nCa=\(\frac{40}{40}\)=1 mol
nC=\(\frac{12}{12}\)=1 mol
nO=\(\frac{48}{16}\)=3 mol
-Trong 1 phân tử hợp chất có:
1 nguyên tử Ca
1 nguyên tử C
3 nguyên tử O
- Công thức hóa học của hợp chất: CaCO3
Canxi cacbonat là thành phần chính của đá vôi. Khi nung đá vôi xảy ra phản ứng hóa học sau:
Canxi cacbonat → Canxi oxit + cacbon đioxit.
Biết rằng khi nung 280kg đá vôi tạo ra 140kg canxi oxit CaO (vôi sống) và 110kg khí cacbon đioxit CO2.
a) Viết công thức về khối lượng của các chất trong phản ứng.
b) Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôi.
a) mCaCO3 = mCaO + mCO2
b) Khối lượng của CaCO3 đã phản ứng:
140 + 110 = 250 kg
Tỉ lệ phần trăm khối lượng CaCO3 chứa trong đá vôi:
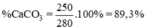
xác định CTHH và phân loại đọc tên các chất X,Y,Z,T,M.Biết:
-Hợp chất khí X có tỉ lệ về khối lượng của C với O là :mc:mo=3:8;hợp chất Y có tỉ lệ về khối lượng của Fe với O là:mfe:mo=21:8,Hợp chất Z có tỉ lệ về % khối lượng 40% Ca,12% C và 48% O.Biết MT= 98g/mol,Hợp chất M có tỉ lệ về % khối lượng 80%R,20%O.Biết MT=80g/mol
camon mn nhìu ạ
check lại giúp mình đoạn cuối với :)
Sao ở câu trước MT = 98 (g/mol) mà câu sau MT = 80 (g/mol)
Bài 6: Hãy tính số mol của các lượng chất sau:
a/ 14 g canxi oxit ( CaO )
b/ 3.1023 nguyên tử cacbon ( C )
c/ 9.1023 phân tử nước ( H2O )
d/ 16 g khí Oxi ( O2 )
Biết C = 12 ; O = 16 ; Ca = 40 ; H = 1
\(a,n_{CaO}=\dfrac{14}{40}=0,35(mol)\\ b,n_{C}=\dfrac{3.10^{-23}}{6.10^{-23}}=0,5(mol)\\ c,n_{H_2O}=\dfrac{9.10^{-23}}{6.10^{-23}}=1,5(mol)\\ d,n_{O_2}=\dfrac{16}{32}=0,5(mol)\)