Đốt cháy hoàn toàn 7,8 gam hợp chất A thu được 26,4 gam CO2 và 5,4 gam H2O.
a/ Tính % khối lượng C, H trong A.
b/ A có chứa oxi không? Tại sao?
c/ Tỉ khối hơi của A so với không khí là 2,69. Xác định CTHH của A.
Đốt cháy hoàn toàn 7,8 g hợp chất hữu cơ X thu được 26,4 g C O 2 và 5,4 g H 2 O . Tỉ khối hơi của X so với không khí là 2,69 ( M k k = 29). Lập công thức phân tử cúa X (H=1, C=12, O=16)
Đốt cháy hoàn toàn 6,9 gam hợp chất hữu cơ A sau phản ứng thu được 13,2 gam khí CO2 và 8,1 gam nước a) Chứng minh A không phải là hidrocacbon b) Xác định CTPT của A. Biết tỉ khối hơi của A so với khí oxi bằng 1,4375 c) Cho hết lượng chất A trên vào Axit axetic thu được hỗn hợp B. Đun nóng hỗn hợp B với H2SO4 xúc tác. - Hỏi PƯHH có xảy ra không? Viết PTHH, cho biết tên phản ứng và tên sản phẩm hữu cơ (nếu có) - Trong trường hợp có xảy ra phản ứng và thu được 7,92 gam sản phẩm hữu cơ thì hiệu suất của phản ứng là bao nhiêu?
nCO2 = 0,08 => nC = 0,08 mol
nH2O = 0,08 => nH = 0,08.2 = 0,16 mol
mX = mC + mH + mO => mO = mX - mC - mH = 1,76-0,08.12-0,16.1 =0,64 gam
nO= 0,64 : 16 = 0,04
Gọi công thức đơn giản nhất của X là CxHyOz => CTPT của X có dạng (CxHyOz )n
x:y:z = nC : nH : nO = 0,08 : 0,16 : 0,04 = 2:4:1
CTĐGN : C2H4O
Mx = 3,04.29 = 88 ==> (C2H4O)n = 88 => n =2
Vậy CTPT của X là C4H8O2
Đốt cháy a gam chất hữu cơ A cần vừa đủ 6,72 lít O2 (đktc), thu được 13,2 gam CO2 và 5,4 gam H2O.
a/ Tìm a.
b/ Tính % khối lượng nguyên tố C, H, O trong A.
c/ Xác định CTHH của A biết tỉ khối của A đối với heli bằng 7,5.
Số mol O2, CO2 và H2O đều bằng 0,3 (mol).
a/ BTKL: a+0,3.32=13,2+5,4 \(\Rightarrow\) a=9 (g).
b/ mC=n\(CO_2\).12=0,3.12=3,6 (g) \(\Rightarrow\) %mC=(3,6/9).100%=40%.
mH=2n\(H_2O\)=2.0,3=0,6 (g) \(\Rightarrow\) %mH=(0,6/9).100%\(\approx\)6,67%.
\(\Rightarrow\) %mO\(\approx\)100%-(40%+6,67%)\(\approx\)53,33%.
c/ Gọi CTHH của A là CxHyOz.
MA=7,5.4=30 (g/mol).
x:y:z=\(\dfrac{3,6}{12}:\dfrac{0,6}{1}:\dfrac{4,8}{16}=1:2:1\).
\(\Rightarrow\) CTPT của A là (CH2O)n mà MA=30 (g/mol), suy ra CTHH của A là CH2O.
Đốt cháy hoàn toàn 5,84 gam hợp chất hữu cơ A thu được 7,04 gam CO2; 2,16 gam H2O và 896 ml N2 (đktc). Tỉ khối hơi của A so với không khí không vượt quá 3. Xác định CTPT của A
Ta có: \(n_{CO_2}=\dfrac{7,04}{44}=0,16\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{2,16}{18}=0,12\left(mol\right)\Rightarrow n_H=0,12.2=0,24\left(mol\right)\)
\(n_{N_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\Rightarrow n_N=0,04.2=0,08\left(mol\right)\)
Ta có: mC + mH + mN = 0,16.12 + 0,24.1 + 0,08.14 = 3,28 (g) < 5,84 (g)
→ A chứa C, H, O và N.
⇒ mO = 5,84 - 3,28 = 2,56 (g) ⇒ nO = 0,16 (mol)
Gọi CTPT của A là CxHyOzNt.
⇒ x:y:z:t = 0,16:0,24:0,16:0,08 = 2:3:2:1
→ CTPT của A có dạng (C2H3O2N)n (n nguyên dương)
Mà: \(M_A< 29.3=87\Rightarrow\left(12.2+3+16.2+14\right)n< 87\)
\(\Rightarrow n< 1,2\Rightarrow n=1\)
Vậy: CTPT của A là C2H3O2N.
Đốt cháy hoàn toàn 2,2 gam hợp chất hữu cơ (A) thu được 4,4 gam CO2 và 1,8
gam H2O.
a. Xác định công thức đơn giản nhất của chất (A).
b.Tìm CTPT của (A) biết tỉ khối hơi của (A) so với H2 bằng 22.
a)
$n_C = n_{CO_2} = \dfrac{4,4}{44} = 0,1(mol)$
$n_H = 2n_{H_2O} = 2.\dfrac{1,8}{18} = 0,2(mol)$
$\Rightarrow n_O = \dfrac{2,2 - 0,1.12 - 0,2.1}{16} = 0,05(mol)$
$n_C : n_H : n_O = 0,1 : 0,2 : 0,05 = 2 : 4 : 1$
Vậy CTĐGN là $C_2H_4O$
b)
CTPT của A là $(C_2H_4O)_n$
Ta có:
$M_A = (12.2 + 4 + 16)n = 22.2 \Rightarrow n = 1$
Vậy CTPT của A là $C_2H_4O$
\(n_{CO_2}=\dfrac{4.4}{44}=0.1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(m_O=2.2-0.1\cdot12-0.1\cdot2=0.8\left(g\right)\)
\(n_O=\dfrac{0.8}{16}=0.05\left(mol\right)\)
\(n_C:n_H:n_O=0.1:0.2:0.05=2:4:1\)
CT đơn giản nhất : \(C_2H_4O\)
\(M_A=22\cdot2=44\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow44n=44\)
\(\Leftrightarrow n=1\)
\(A:C_2H_4O\)
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam C O 2 và 5,4 gam H 2 O . Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A?
A. C 2 H 6
B. C 2 H 4
C. C 3 H 8
D. C 3 H 6
n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
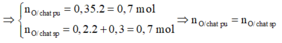
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
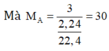
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.
1/ Đốt cháy hoàn toàn 9,2 gam một hợp chất hữư cơ A, sau phản ứng tạo ra 17,6 gam CO2 và 10,8 gam H2O.
a) Xác định công thức phân tử của A. Biết tỉ khối hơi của A so với khí hiđro là 23.
b) Viết các công thức cấu tạo có thể có của A.
2/ Đốt cháy hoàn toàn 1 lít khí hiđrocacbon cần 6 lít khí oxi, sinh ra 4 lít khí cacbonic. Các thể tích khí đo ở cùng nhiệt độ và áp suất.
a) Xác định công thức phân tử của hiđrocacbon.
b) Viết các công thức cấu tạo có thể có của hiđrocacbon đó.
1) Bảo toàn C: \(n_C=\dfrac{17,6}{44}=0,4\left(mol\right)\)
Bảo toàn H: \(n_H=\dfrac{10,8}{18}.2=1,2\left(mol\right)\)
Bảo toàn O: \(n_O=\dfrac{9,2-0,4.12-1,2}{16}=0,2\left(mol\right)\)
\(M_A=23.2=46\left(\dfrac{g}{mol}\right)\)
CTPT: CxHyOz
=> x : y : z = 0,4 : 1,2 : 0,2 = 2 : 6 : 1
=> (C2H6O)n = 46
=> n = 1
CTPT: C2H6O
CTCT:
(1) CH3-CH2-OH
(2) CH3-O-CH3
2) Ta có:
\(V_{C_xH_y}:V_{O_2}:V_{CO_2}=1:6:4\)
=> \(n_{C_xH_y}:n_{O_2}:n_{CO_2}=1:6:4\)
Bảo toàn C: \(x=n_C=n_{CO_2}=4\left(mol\right)\)
Bảo toàn O: \(n_{O\left(H_2O\right)}=2n_{O_2}-2n_{CO_2}=2.6-2.4=4\left(mol\right)\)
Bảo toàn H: \(n_H=2n_{H_2O}=2n_{O\left(H_2O\right)}=2.4=8\left(mol\right)\)
=> Trong 1 mol A chứa 4 mol C và 8 mol H
=> CTPT: C4H8
CTCT:
(1) CH2=CH-CH2-CH3
(2) CH3-CH=CH-CH3