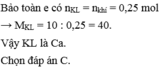Cho 11,5g một kim loại A ( I ) tác dụng hết với nước tạo ra 5,6 lít khí Hiddro ( đktc) . Tìm kim loại A

Những câu hỏi liên quan
Cho 10 gam một kim loại kiềm thổ tác dụng hết với nước thoát ra 5,6 lít khí (đktc). Kim loại kiềm thổ đó là
A. Ba.
B. Mg.
C. Ca.
D. Sr.
Cho 10 gam một kim loại kiềm thổ M tác dụng hết với nước thoát ra 5,6 lít khí (đktc). Kim loại kiềm thổ đó là
A. Ba
B. Mg
C. Ca
D. Sr
Bài 1: Cho 5.52g một kim loại kiềm tác dụng với nước tạo ra 2.688 lít khí H2 (đktc). Xác định tên kim loại đó.
Bài 2: Cho 1.84g một kim loại kiềm tác dụng với nước tạo ra 896ml khí H2 (đktc). Xác định tên kim loại đó.
Bài 1:
Gọi kim loại kiềm là R
\(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
Giả sử R hóa trị I:
\(R+H_2O\rightarrow ROH+\dfrac{1}{2}H_2\\ \Rightarrow n_R=0,12.2=0,24\left(mol\right)\\ \Rightarrow M_R=\dfrac{5,52}{0,24}=23\left(đvC\right)\)
Giả sử đúng, tên kim loại đó là sodium (Na)
Bài 2: Tự làm tương tự bài 1 nhé=0
Đúng 2
Bình luận (0)
Cho 10 gam một kim loại kiềm thổ tác dụng hết với nước thoát ra 5,6 lít khí (đktc). Tên của kim loại kiềm thổ đó là ?
vi la kiem tho nen Pu voi nuoc la : R +2 H2O ->R(oh)2 +H2
nH2 = nR = 0.25mol => M(R) = 10/0.25 = 40 => R la Ca
Chon C
Đúng 0
Bình luận (0)
câu 26
cho 0,6gam một kim loại A hoa trị II tác dụng với nước tạo ra 0,336 lít khí H2 (đktc). tìm tên kim loại đó
nH2=0,336/22,4=0,015mol
A+2H2O-> A(OH)2 +H2
0,015 0,015
M(A)= 0,6/0,015=40(Ca)
Đúng 4
Bình luận (0)
Cho 10 gam một kim loại kiềm thổ tác dụng hết với nước thoát ra 5,6 khí (đktc). Kim loại kiềm
thổ đó là :
A. Ca
B. Ba
C. Sr
D. Mg
Đáp án A
M + 2 H2O → M(OH)2 + H2 => nH2 = nM = 0,25 mol
=> M= 40g ( Ca)
Đúng 0
Bình luận (0)
. Cho 8 gam một kim loại R thuộc nhóm IIA tác dụng hết với nước tạo ra 4,48 lít khí hiđro (đktc). Tìm tên kim loại R. (biết Mg=24, Be=9, Ca=40, Ba=137)
$R + 2HCl \to RCl_2 + H_2$
$n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
Theo PTHH : $n_R = n_{H_2} = 0,2(mol)$
$\Rightarrow M_R = \dfrac{8}{0,2} = 40$
Vậy R là Canxi
Đúng 1
Bình luận (0)
Câu 1.
a. Cho 0,6g một kim loại M có hóa trị II tác dụng với nước tạo ra 0,336 lít khí H2 (đktc). Xác định kim loại M..
b. Lấy toàn bộ lượng kim loại trên tác dụng hết với 125ml dung dịch CuSO4. Tính nồng độ mol của dung dịch CuSO4.
a) \(n_{H_2}=\dfrac{0,336}{22,4}=0,015\left(mol\right)\)
PTHH: M + 2H2O ---> M(OH)2 + H2
0,015<-----------------------0,015
=> \(M_M=\dfrac{0,6}{0,015}=40\left(g/mol\right)\)
=> M là Ca
b) PTHH: \(Ca+2H_2O+C\text{uS}O_4\rightarrow C\text{aS}O_4\downarrow+Cu\left(OH\right)_2\downarrow+H_2\uparrow\)
0,015----------->0,015
=> \(C_{M\left(C\text{uS}O_4\right)}=\dfrac{0,015}{0,125}=0,12M\)
Đúng 0
Bình luận (0)
Câu 1.
a. Cho 0,6g một kim loại M có hóa trị II tác dụng với nước tạo ra 0,336 lít khí H2 (đktc). Xác định kim loại M..
b. Lấy toàn bộ lượng kim loại trên tác dụng hết với 125ml dung dịch CuSO4. Tính nồng độ mol của dung dịch CuSO4.
a) $n_{H_2} = 0,015(mol)$
$M + 2H_2O \to M(OH)_2 + H_2$
Theo PTHH : $n_M = n_{H_2} = 0,015(mol) \Rightarrow M = \dfrac{0,6}{0,015} = 40(Canxi)$
b) $Ca(OH)_2 + CuSO_4 \to Cu(OH)_2 + CaSO_4$
Theo PTHH : $n_{CuSO_4} = n_{Ca(OH)_2} = 0,015(mol)$
$\Rightarrow C_{M_{CuSO_4}} = \dfrac{0,015}{0,125} = 0,12M$
Đúng 0
Bình luận (0)