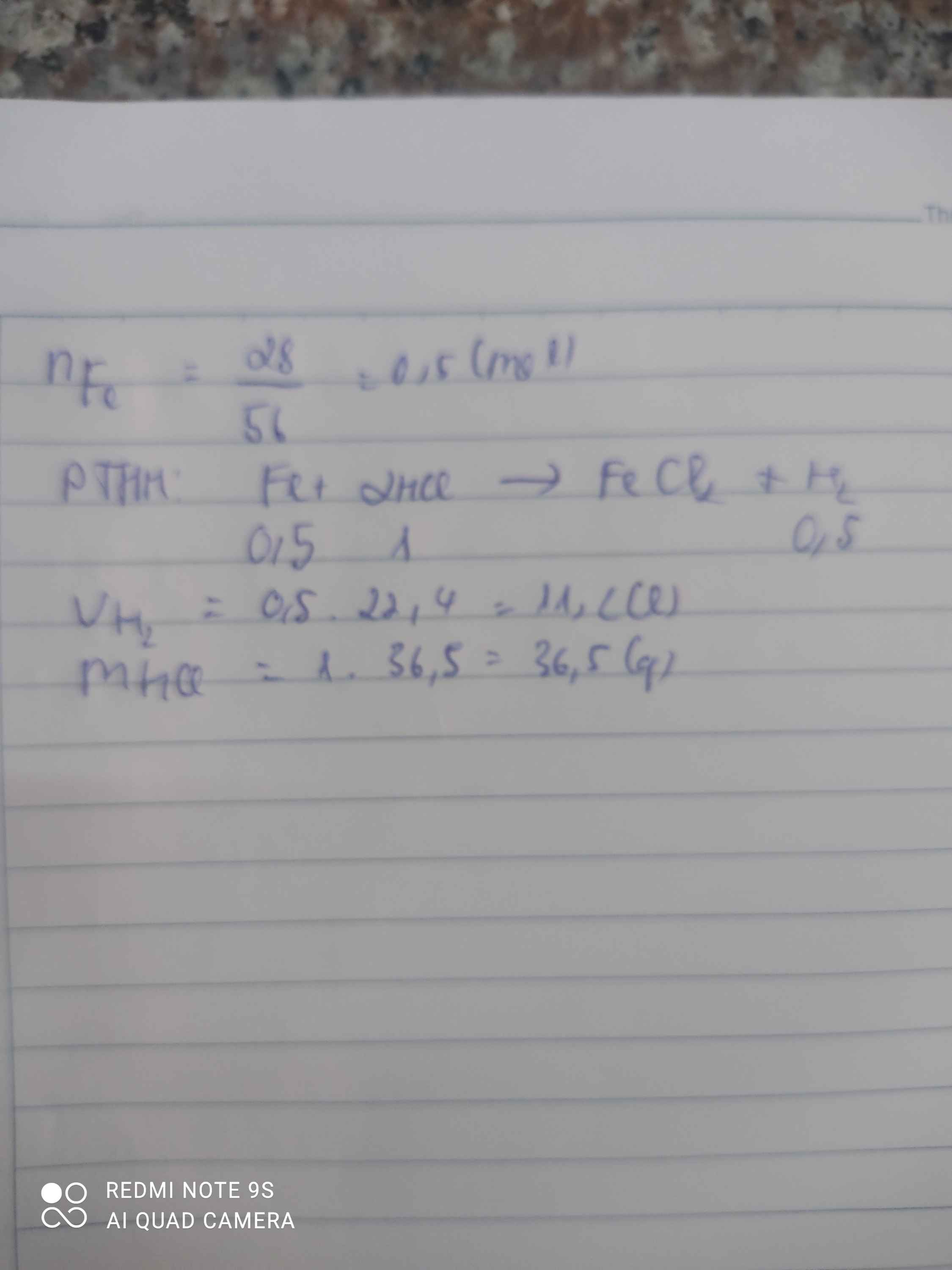Cho 2,8 gam kim loại sắt tác dụng hoàn toàn với dung dịch axit HCl. a)Viết phương trình hoá học b)Tính thể tích Hiđro thu được ở điều kiện tiêu chuẩn

Những câu hỏi liên quan
Câu 2 Cho kim loại sắt (Fe) tác dụng với vừa đủ với 10,65 g axit clohiđric (HCl) thu được muối FeCl2 và khí hidro (H2)
a - Viết phương trình hoá học xảy ra.
b - Tính thể tích khí hiđro (ở điều kiện tiêu chuẩn) thu được.
c - Tính số gam Cu thu được khi dùng lượng khí H2 điều chế được ở trên để khử 16g đồng (II) oxit (CuO).
Câu 2 Cho kim loại sắt (Fe) tác dụng với vừa đủ với 10,65 g axit clohiđric (HCl) thu được muối FeCl2 và khí hidro (H2)
a - Viết phương trình hoá học xảy ra.
b - Tính thể tích khí hiđro (ở điều kiện tiêu chuẩn) thu được.
c - Tính số gam Cu thu được khi dùng lượng khí H2 điều chế được ở trên để khử 16g đồng (II) oxit (CuO).
a)\(n_{HCl}=\dfrac{10,65}{36,5}=0,3mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,15 0,3 0,15 0,15
b)\(V_{H_2}=0,15\cdot22,4=3,36l\)
c)\(n_{CuO}=\dfrac{16}{80}=0,2mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,2 0,15 0,15
\(m_{Cu}=0,15\cdot64=9,6g\)
Đúng 2
Bình luận (3)
\(a,Fe+2HCl\rightarrow FeCl_2+H_2\)
\(b,n_{HCl}=\dfrac{m}{M}=\dfrac{10,65}{36,5}\approx0,3mol\)
\(\rightarrow n_{H_2}=0,15mol\Rightarrow V_{H_2}=0,15.22,4=3,36l\)
Đúng 0
Bình luận (0)
Cho kim loại sắt tác dụng với vừa đủ với 12,775 g axit clohiđric (HCl). a - Viết phư¬ơng trình hoá học xảy ra. b - Tính thể tích khí hiđro thu được (ở điều kiện tiêu chuẩn) c - Tính số gam Cu thu được khi dùng lượng khí H2 điều chế được ở trên để khử 16g đồng (II) oxit .
8/ Cho 19,5 gam kẽm tác dụng hoàn toàn với 200 ml dung dịch HCl
a. Viết phương trình hoá học xảy ra.
b. Tính thể tích hiđro sinh ra ở điều kiện tiêu chuẩn.?
`a)PTHH:`
`Zn + 2HCl -> ZnCl_2 + H_2`
`0,3` `0,3` `(mol)`
`n_[Zn]=[19,5]/65=0,3(mol)`
`b)V_[H_2]=0,3.22,4=6,72(l)`
Đúng 3
Bình luận (0)
Để điều chế hiđro trong phòng thí nghiệm người ta dùng 13g kẽm tác dụng hoàn toàn với dung dịch HCl a) Viết phương trình hoá học sảy ra b)Tính thể tích hiđro sinh ra ở điều kiện tiêu chuẩn c)Nếu cho toàn bộ lượng khí hiđro ở trên khử 0,3 mol CuO ,tính lượng đồng kim loại sinh ra
a.b.
\(n_{Zn}=\dfrac{13}{65}=0,2mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
c.
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,3 > 0,2 ( mol )
0,2 0,2 ( mol )
\(m_{Cu}=0,2.64=12,8g\)
Đúng 1
Bình luận (0)
Cho 6 gam kim loại magie tác dụng hoàn toàn với dung dịch axit HCl.
a) Tính thể tích hiđro thu được ở đktc?
b) Tính khối lượng axit HCl phản ứng?
c) Lượng khí hiđro thu được ở trên cho tác dụng với 16 gam sắt (III) oxit. Tính khối lượng sắt thu được sau phản ứng
\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 0,25.........0,5.........0,25.......0,25\left(mol\right)\\ a.V_{H_2\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\\ b.m_{HCl}=0,5.36,5=18,25\left(g\right)\\ c.n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\\ Fe_2O_3+3H_2\underrightarrow{^{to}}2Fe+3H_2O\\ Vì:\dfrac{0,25}{3}< \dfrac{0,1}{1}\\ \Rightarrow Fe_2O_3dư\\ n_{Fe}=\dfrac{2}{3}.0,25=\dfrac{1}{6}\left(mol\right)\\ \Rightarrow m_{Fe}=\dfrac{1}{6}.56\approx9,333\left(g\right)\)
Đúng 0
Bình luận (0)
a,\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,25 0,5 0,25
\(\Rightarrow V_{H_2}=0,25.22,4=5,6\left(l\right)\)
b,\(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
c,\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 → 2Fe + 3H2O
Mol: 0,25 \(\dfrac{1}{6}\)
Ta có: \(\dfrac{0,1}{1}>\dfrac{0,25}{3}\)⇒ Fe2O3 dư, H2 hết
\(m_{Fe}=\dfrac{1}{6}.56=9,33\left(g\right)\)
Đúng 0
Bình luận (0)
\(n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,25 0,5 0,25
a) \(n_{H2}=\dfrac{0,25.1}{1}=0,25\left(mol\right)\)
\(V_{H2\left(dktc\right)}0,25.22,4=5,6\left(l\right)\)
b) \(n_{HCl}=\dfrac{0,25.2}{1}=0,5\left(mol\right)\)
⇒ \(m_{HCl}=0,5.36,5=18,25\left(g\right)\)
c) \(n_{Fe2O3}=\dfrac{16}{160}=0,1\left(mol\right)\)
Pt : \(3H_2+Fe_2O_3\rightarrow\left(t_o\right)2Fe+3H_2O|\)
3 1 2 3
0,25 0,1 \(\dfrac{1}{6}\)
Lập tỉ số so sánh : \(\dfrac{0,25}{3}< \dfrac{0,1}{1}\)
⇒ H2 phản ứng hết , Fe2O3 dư
⇒ Tính toán dựa vào số mol của H2
\(n_{Fe}=\dfrac{0,25.2}{3}=\dfrac{1}{6}\left(mol\right)\)
⇒ \(m_{Fe}=\dfrac{1}{6}.56=9,3\left(g\right)\)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Cho 19,5g tác dụng hết với 200ml dung dịch HCl
a) Viết phương trình phản ứng
b) TÍnh thể tích khí hiđro thu được ở điều kiện tiêu chuẩn
c) Tính C% của dung dịch axit đã dùng
19,5g gì :) ?, với cả đề cho Vdd thì sao tính đuợc C% :))
Đúng 2
Bình luận (0)
cho 28 gam sắt tác dụng với axit HCl (dư) sau phản ứng thu được (II) clorua (FeCl2) và khí hiđro
a viết phương trình phản ứng
b tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn?
c tính khối lượng axit HCl đã tham gia phản ứng
\(n_{Fe}=\dfrac{28}{56}=0,5mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,5 1 0,5
\(V_{H_2}=0,5\cdot22,4=11,2l\)
\(m_{HCl}=1\cdot36,5=36,5g\)
Đúng 4
Bình luận (0)
Cho 8,4 gam sắt (Fe) tác dụng với dung dịch chứa 14,6 gam axit clohiđric(HCL)
a, Viết Phương Trình Hóa học
b, Chất nào còn dư sau phan ung? khoi luong Dư bao nhiêu gam
c, Tính thể tích khí hiđro sinh ra ở điều kiện tiêu chuẩn d,tinh the tich khi hidro sinh ra [dktc]
mFe= 8,4/56= 0,15 mol
m HCl = 14,6/36,5=0,4 mol
PTHH: Fe +2HCl →FeCl2 +H2
Bđ: 0,15 0,4 0 0 mol
Pứ: o,15→0,3 0,15 0,15 mol
Sau pứ:0 0,1 0,15 0,15 mol
a. HCl dư: m =0,1.36,5=3,65 g
b. m FeCl2 = 0,15.127=19,05 g
c. m H2 = 0,15.2= 0,3 g
V H2= 0,15.22,4=3,36 (l)
Đúng 1
Bình luận (0)