Một binh kín chứa một lượng khí ở nhiệt độ 27 độ C và áp suất 1 atm. Hãy vẽ đồ thị biểu diễn sự biến thiên của áp suất theo nhiệt độ trong quá trình nung nóng đẳng tích lên tới nhiệt độ 127 độ C trong hệ tọa độ áp suất-nhiệt độ tuyệt đối (p, T)

Những câu hỏi liên quan
Xét một lượng khí không đổi chứa trong một bình kín, ban đầu khí trong bình có nhiệt độ 27 độ C và áp suất 2.10^ 5 Pa, sau đó người ta nung nóng khi đến nhiệt độ 627 độ C . Tìm áp suất của khí trong bình lúc này và vẽ đồ thị biểu diễn quá trình trên trong hệ tọa độ (p, T) ?
Trạng thái 1: \(\left\{{}\begin{matrix}p_1=2\cdot10^5Pa\\T_1=27^oC=300K\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=???\\T_2=627^oC=900K\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{2\cdot10^5}{300}=\dfrac{p_2}{900}\)
\(\Rightarrow p_2=6\cdot10^5Pa\)
Đúng 2
Bình luận (0)
Câu 1Nén khí đẳng nhiệt từ thể tích 10 lít đến thể tích 4 lít thì áp suất của khí tăng lên bao nhiêu lần ?Câu 2Một khối khí có áp suất 1,5 atm và thể tích 5 lít được biến đổi đẳng nhiệt đến áp suất 4atm. Tính thể tích khí sau khi biến đổi và vẽ đồ thị biểu diễn trong hệ toạ độ (p, V).Câu 3Nén đẳng nhiệt một khối khí từ thể tích 9 lít đến thể tích 6 lít thì áp suất của khí tăng thêm một lượng 5.104Pa. Tính áp suất của khí trước và sau khi nén. Câu 4Một lượng khí lí tưởng ở nhiệt độ 170C và áp suấ...
Đọc tiếp
Câu 1
Nén khí đẳng nhiệt từ thể tích 10 lít đến thể tích 4 lít thì áp suất của khí tăng lên bao nhiêu lần ?
Câu 2
Một khối khí có áp suất 1,5 atm và thể tích 5 lít được biến đổi đẳng nhiệt đến áp suất 4atm. Tính thể tích khí sau khi biến đổi và vẽ đồ thị biểu diễn trong hệ toạ độ (p, V).
Câu 3
Nén đẳng nhiệt một khối khí từ thể tích 9 lít đến thể tích 6 lít thì áp suất của khí tăng thêm một lượng 5.104Pa. Tính áp suất của khí trước và sau khi nén.
Câu 4
Một lượng khí lí tưởng ở nhiệt độ 170C và áp suất 1,5 atm được nung nóng đẳng tích đến áp suất 2,5atm. Tính nhiệt độ của khí sau khi nung và vẽ đồ thị biểu diễn sự biến đổi trạng thái trong hệ (p-T).
Câu 5
Một khối khí ở nhiệt độ 170C áp suất 1,5 atm được nung nóng đẳng tích đến 1170C thì áp suất của khí đó là bao nhiêu? Vẽ đồ thị biểu diễn sự biến đổi trạng thái của khí trong hệ toạ độ (p, T).
Câu 1 : Thể tích giảm đi 10/4 = 2,5 lần nên áp suất tăng 2,5 lần
Một bình chứa 14 g khí nitơ ở nhiệt độ 27
°
C và áp suất 1 atm. Sau khi hơ nóng, áp suất trong bình chứa khí tăng lên tới 5 at. Hãy tính nhiệt lượng cần cung cấp cho khí nitơ và độ tăng nội năng của khíBiết nhiệt dung riêng của nitơ trong quá trình nung nóng đẳng nhiệt là
c
V
742 J/(kg.K). Coi sự nở vì nhiệt của bình là không đáng kể.
Đọc tiếp
Một bình chứa 14 g khí nitơ ở nhiệt độ 27 ° C và áp suất 1 atm. Sau khi hơ nóng, áp suất trong bình chứa khí tăng lên tới 5 at. Hãy tính nhiệt lượng cần cung cấp cho khí nitơ và độ tăng nội năng của khí
Biết nhiệt dung riêng của nitơ trong quá trình nung nóng đẳng nhiệt là c V = 742 J/(kg.K). Coi sự nở vì nhiệt của bình là không đáng kể.
Do bình không dãn nở vì nhiệt, nên công do khí sinh ra : A' = p ∆ V = 0. Theo nguyên lí I, ta có :
∆ U = Q (1)
Nhiệt lượng do khí nhận được : Q = m c V ( T 2 - T 1 ) (2)
Mặt khác, do quá trình là đẳng tích nên :
![]()
Từ (2) tính được : Q = 15,58. 10 3 J.
Từ (1) suy ra: ∆ U = 15,58. 10 3 J.
Đúng 0
Bình luận (0)
Nung nóng khí trong bình kín từ nhiệt độ 27 ° C và áp suất 2 atm. Bỏ qua sự nở vì nhiệt của bình chứa. Khi nhiệt độ khí là 327 ° C , tính áp suất khí trong bình.
- Chỉ ra đây là quá trình đẳng tích
- Áp dụng định luật Sác – lơ:
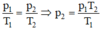
Thay số được p 2 = 4atm.
Đúng 0
Bình luận (0)
Trong xilanh của một động cơ có chứa một lượng khí ở nhiệt độ 470C và áp suất 0,7 atm.Sau khi bị nén thể tích của khí giảm đi 5 lần và áp suất tăng lên tới 8 atm. Tính nhiệt độ của khí ở cuối quá trình nén? A. 7310C B. 320 K C. 3200C D. 731K
Đọc tiếp
Trong xilanh của một động cơ có chứa một lượng khí ở nhiệt độ 470C và áp suất 0,7 atm.Sau khi bị nén thể tích của khí giảm đi 5 lần và áp suất tăng lên tới 8 atm. Tính nhiệt độ của khí ở cuối quá trình nén?
A. 7310C
B. 320 K
C. 3200C
D. 731K
Đáp án D
TT1
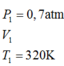
TT2

áp dụng PTTT khí lí tưởng
ta có:
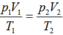
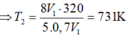
Đúng 0
Bình luận (0)
Thế nào là quá trình đẳng tích? Phát biểu và viết biểu thức định luật Sác lơ
Một cái bơm chứa 100 cm3 không khí ở nhiệt độ 27oC và áp suất 1(atm). Tính áp suất của không khí trong bơm khi không khí bị nén xuống còn 40cm3 và nhiệt độ tăng lên tới 370C
1/ Quá trình biến đổi trạng thái khi thể tích không đổi gọi là đẳng tích
Định luật: Trong quá trình đẳng tích của một lượng khí nhất định, áp suất tỉ lệ thuận với nhiệt độ tuyệt đối
Biểu thức:
\(\frac{P}{T}=\) hằng số
+Lưu ý: Nếu gọi \(P_1,T_1\) là áp suất và nhiệt độ tuyệt đối của 1 lượng khí ở trạng thái 1
Nếu gọi \(P_2,T_2\) là áp suất và nhiệt độ tuyệt đối của 1 lượng khí ở trạng thái 2
Ta có biểu thức: \(\frac{P_1}{T_1}=\frac{P_2}{T_2}\)
2/ Phương trình trạng thái khí lí tưởng:
\(\frac{p_1V_1}{T_1}=\frac{p_2V_2}{T_2}\)
Tính ra \(p_2=2,58atm\)
Đúng 0
Bình luận (0)
Một khối khí lí tưởng có thể tích 10 lít, áp suất 2 atm, nhiệt độ 87 độ C thực hiện biến đổi theo 2 quá trình liên tiếp: quá trình 1 đẳng áp, nhiệt độ tuyệt đối giảm 2 lần. Quá trình 2: đẳng nhiệt, áp suất sau cùng là 0,5 atm. Thể tích sau cùng của khối khí trên là bao nhiêu
Tóm tắt đề bài như sau:
\(\left\{{}\begin{matrix}V=10\left(l\right)\\p=2\left(atm\right)\\T=87+273=360\left(K\right)\end{matrix}\right.\underrightarrow{Đẳngáp}\left\{{}\begin{matrix}V_1=?\\p_1=2\left(atm\right)\\T_1=\dfrac{T}{2}=180\left(K\right)\end{matrix}\right.\) \(\underrightarrow{Đẳngnhiet}\left\{{}\begin{matrix}V_2=?\\p_2=0,5\left(atm\right)\\T_2=180\left(K\right)\end{matrix}\right.\)
Phương trình trạng thái khí lí tưởng ( Claperon Mendeleep ): \(\dfrac{pV}{T}=const\)
Đẳng áp: \(\dfrac{V}{T}=\dfrac{V_1}{T_1}\Leftrightarrow V_1=\dfrac{10.180}{360}=5\left(l\right)\)
Đẳng nhiệt: \(p_1V_1=p_2V_2\Rightarrow V_2=\dfrac{p_1V_1}{p_2}=\dfrac{2.5}{0,5}=20\left(l\right)\)
Vậy thể tích sau cùng của khối khí trên là V2=20(l)
Đúng 2
Bình luận (3)
Một lượng khí ở nhiệt độ 127°C chiếm thể tích 4 lít, có áp suất 2atm. Khí được biến đổi theo chu trình kín gồm 3 giai đoạn: -Giai đoạn 1: dãn nở đẳng nhiệt, thể tích tăng gấp 2 lần -Giai đoạn 2: nén đẳng áp -Giai đoạn 3: nung nóng đẳng tíchTìm nhiệt độ, áp suất thấp nhất trong chu trình đó(ghi ra từng trạng thái cho từng giai đoạn)
Đọc tiếp
Một lượng khí ở nhiệt độ 127°C chiếm thể tích 4 lít, có áp suất 2atm. Khí được biến đổi theo chu trình kín gồm 3 giai đoạn:
-Giai đoạn 1: dãn nở đẳng nhiệt, thể tích tăng gấp 2 lần
-Giai đoạn 2: nén đẳng áp
-Giai đoạn 3: nung nóng đẳng tích
Tìm nhiệt độ, áp suất thấp nhất trong chu trình đó
(ghi ra từng trạng thái cho từng giai đoạn)
3. Một binh kín chứa khí lí tưởng ở áp suất 5 atm và nhiệt độ 37°C. Tính áp suất của khi khi nhiệt độ trong bình là 17"C..
Ta có: \(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{5}{37+273}=\dfrac{p_2}{17+273}\)
\(\Rightarrow p_2=4,68atm\)
Đúng 2
Bình luận (0)

















