Hòa tan 12g hh Al Và Ag vào dd H2SO4 dư thu được 13,44 lít khí (đktc). Tính thành phần % theo khối lượng mỗi hợp chất ban đầu.
Hòa tan 12g hỗn hợp gồm Al, Ag vào dung dịch H 2 SO 4 loãng, dư. Phản ứng kết thúc thu được 13,44 lít khí H 2 (đktc). Thành phần % khối lượng của Al, Ag trong hỗn hợp lần lượt là
A. 70% và 30%
B. 90% và 10%
C. 10% và 90%
D. 30% và 70%
Đáp án B
Cho Al và Ag phản ứng với H 2 S O 4 loãng, dư chỉ có Al phản ứng.
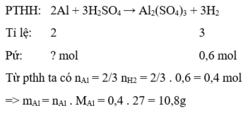
% m A l = 10,8 12 .100 % = 90 % .
% m A g = 100 % - 90 % = 10 %
Hòa tan 12g hỗn hợp gồm Al, Ag vào dung dịch H2SO4 loãng, dư. Phản ứng kết thúc thu được 13,44 lít khí H2 (đktc). Thành phần % khối lượng của Al, Ag trong hỗn hợp lần lượt là
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
_____0,4<-----------------------------------0,6
=> \(\%Al=\dfrac{0,4.27}{12}.100\%=90\%\)
%Ag = 100% - 90% = 10%
hòa tan 12g hỗn hợp gồm Al, Ag vào dd H2SO4 loãng dư. Pư kết thúc thu đc 13,44 l khí H2(đktc).Thành phần % khối lượng của Ag trong hỗn hợp là bn?
Hòa tan 12g hỗn hợp gồm Al,Ag vào đ H2SO4 loãng,dư/Phản ứng kết thúc thu đc 13,44 lít khí H2 (đktc).Thành phần % khối lượng của Al,Ag trong hỗn hợp là bao nhiêu ?(Giai chi tiết)
Hóa 9
910% và 100%
Sai thôi nha , mk hok ngu Hóa lém ( mặc dù đã hok lp 10 )
Ag ko t/d với H2SO4 loãng
2AL + 3H2SO4 -> AL2(S04)3 + 3H2
Số mol của H2 = 13,44/22,4 =0,6
Khối lượng của AL = 0,6 x 2/3 = 0,4
% khối lượng của AL trog hỗn hợp là : (10,8/12) x 100% = 90%
% khối lượng của Ag trog hỗn hợp là ; 100% - 90% = 10%
Hòa tan 12g hh Fe,Cu trong dd H2SO4 dư (loãng) thu đc 2,24l khí ở đktc. Chất rắn còn lại hòa tan trong H2SO4 98% ( dư 10% về khối lượng ) đc V lít khí A ở đktc
a) Tính % m trong hỗn hợp ban đầu
b) Tính V và mdd H2SO4 đã dùng
a/nH2= 0,1(mol)
Fe + H2SO4 -> FeSO4 + H2
0,1_________________0,1(mol)
=> mFe=0,1.56=5,6(g)
=> %mFe= (5,6/12).100\(\approx\) 46,667%
=> %mCu \(\approx\) 100% - 46,667% \(\approx\) 53,333%
b) mCu= 12-5,6=6,4(g) -> nCu= 0,1(mol)
Cu + 2 H2SO4(đ) -to-> CuSO4 + SO2 + 2 H2O
0,1___0,2__________________0,1(mol)
V=V(SO2,đktc)=0,1.22,4=2,24(l)
mH2SO4(p.ứ)=0,2.98=19,6(g)
=> mH2SO4(bđ)= 19,6 x 100/90 \(\approx21,778\left(g\right)\)
=> mddH2SO4 \(\approx\) (21,778 x 100)/98\(\approx22,222\left(g\right)\)
a)Gọi x,y lần lượt là số mol của Al, Fe trong hỗn hợp ban đầu (x,y>0)
Sau phản ứng hỗn hợp muối khan gồm: \(\left\{{}\begin{matrix}AlCl_3:x\left(mol\right)\\FeCl_2:y\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}27x+56y=13,9\\133,5x+127y=38\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,0896\\y\approx0,205\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,0896\cdot27\cdot100\%}{13,9}\approx17,4\%\\\%m_{Fe}=\dfrac{0,205\cdot56\cdot100\%}{13,9}\approx82,6\%\end{matrix}\right.\)
Theo Bảo toàn nguyên tố Cl, H ta có:\(n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{3n_{AlCl_3}+2n_{FeCl_2}}{2}\\ =\dfrac{3\cdot0,0896+2\cdot0,205}{2}=0,3394mol\\ \Rightarrow V_{H_2}=0,3394\cdot22,4\approx7,6l\)
Hòa tan 1,52 gam kim lọai Mg và Cu vào dd HNO3 đặc, nóng dư thu được duy nhất 1,344 lít (đktc) khí màu nâu. a. Tính thành phần % theo khối lượng của mỗi chất ban đầu. b. Tính khối lượng muối tạo thành.
a) Gọi số mol Mg, Cu là a,b
=> 24a + 64b = 1,52
\(n_{NO_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mg0 - 2e --> Mg+2
a---->2a---->a
Cu0 - 2e --> Cu+2
b---->2b---->b
N+5 +1e--> N+4
___0,06<--0,06
Bảo toàn e: 2a + 2b = 0,06
=> \(\left\{{}\begin{matrix}a=0,01\\b=0,02\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%Mg=\dfrac{24.0,01}{1,52}.100\%=15,79\%\\\%Cu=\dfrac{64.0,02}{1,52}.100\%=84,21\%\end{matrix}\right.\)
b) \(m_{Mg\left(NO_3\right)_2}=0,01.148=1,48\left(g\right)\)
\(m_{Cu\left(NO_3\right)_2}=0,02.188=3,76\left(g\right)\)
1/ Cho 0,83g hổn hợp gồm Al và Fe tác dụng với dd H2SO4 loãng dư, sau phản ứng thu được 0,56 lit khí ( đktc)
a) Viết phương trình phản ứng.
b) Tính thành phần % theo khối lượng của hổn hợp ban đầu.
2/ Hòa tan 4,5g hợp kim Al - Mg trong dd H2SO4 loãng dư, thấy có 5,04 lít khí H2 bay ra ( đktc).
a) Viết phương trình phản ứng hóa học xãy ra.
b) Tính thành phần % khối lượng của mỗi kim loại trong hổn hợp ban đầu.
Dạng: PHƯƠNG PHÁP HAI DÒNG
1/ Cho 9,2g một kim loại A phản ứng với khí clo (dư) tạo thành 23,4g muối. Xác định tên kim loại A, biết A có hóa trị I
Câu 1:
Đặt \(n_{Al}=x(mol);n_{Fe}=y(mol)\Rightarrow 27x+56y=0,83(1)\)
\(n_{H_2}=\dfrac{0,56}{22,4}=0,025(mol)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ Fe+H_2SO_4\to FeSO_4+H_2\\ \Rightarrow 1,5x+y=0,025(2)\\ (1)(2)\Rightarrow x=y=0,01(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,01.27}{0,83}.100\%=32,53\%\\ \Rightarrow \%_{Fe}=100\%-32,53\%=67,47\%\)
Câu 2:
Đặt \(n_{Al}=x(mol);n_{Mg}=y(mol)\Rightarrow 27x+24y=4,5(1)\)
\(n_{H_2}=\dfrac{5,04}{22,4}=0,225(mol)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ Mg+H_2SO_4\to MgSO_4+H_2\\ \Rightarrow 1,5x+y=0,225(2)\\ (1)(2)\Rightarrow x=0,1(mol);y=0,075(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,1.27}{4,5}.100\%=60\%\\ \Rightarrow \%_{Mg}=100\%-60\%=40\%\)
Dạng PP hai dòng:
\(PTHH:2A+Cl_2\to 2ACl\\ \Rightarrow n_A=n_{ACl}\\ \Rightarrow \dfrac{9,2}{M_A}=\dfrac{23,4}{M_A+35,5}\\ \Rightarrow M_A=23(g/mol)\)
Vậy A là natri
Cho 26,7 g hh A gồm Mg, Fe, Al tan hết trong dd H2SO4 lấy dư .sau phản ứng xong thu được 17,92 lít khí( ĐKTC). Biết thể tích khí thoát ra do Sắt hòa tan gấp 2 lần thể tích khí tạo ra khi Magie tan
a) Tính thành phần phần trăm khối lượng mỗi chất trong hh A
b) Tính khối lượng H2SO4
b) Tính khối lượng H2SO4 dư sau pư, biết H2SO4 đã lấy dư so với lượng pư là 10%