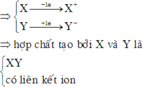lớp vỏ của nguyên tử x có các electron phân bố như sau 2e/8e/7e nguyên tử x thuộc Nguyên tố hóa học nào

Những câu hỏi liên quan
Nguyên tử của nguyên tố X có tổng số hạt electron trong các phân lớp p là 7 . Số hạt mang điện của 1 nguyên tử Y nhiều hơn số hạt mang điện của 1 nguyên tử X là 8 hạt a/ tìm các nguyên tố X và Y b/ phân bố các electron vào orbital ở lớp vỏ nguyên tử, từ đó xác định số electron độc thân của X và Y
Nguyên tử nguyên tố X có electron cuối cùng thuộc phân lớp s, nguyên tử nguyên tố Y có electron cuối cùng thuộc phân lớp p. Biết rằng tổng số electron trong nguyên tử của X và Y là 20. Bản chất của liên kết hóa học trong hợp chất X – Y là: A. Sự góp chung đôi electron. B. Sự góp đôi electron từ một nguyên tử. C. Sự tương tác yếu giữa hai nguyên tử có chênh lệch độ âm điện lớn. D. Lực hút tĩnh điện giữa hai ion trái dấu
Đọc tiếp
Nguyên tử nguyên tố X có electron cuối cùng thuộc phân lớp s, nguyên tử nguyên tố Y có electron cuối cùng thuộc phân lớp p. Biết rằng tổng số electron trong nguyên tử của X và Y là 20. Bản chất của liên kết hóa học trong hợp chất X – Y là:
A. Sự góp chung đôi electron.
B. Sự góp đôi electron từ một nguyên tử.
C. Sự tương tác yếu giữa hai nguyên tử có chênh lệch độ âm điện lớn.
D. Lực hút tĩnh điện giữa hai ion trái dấu
Đáp án D
X có e cuối thuộc phân lớp s ⇒ nhóm A (I hoặc II).
Y có e cuối thuộc phân lớp p ⇒ nhóm A (III → VIII).
eX + eY = 20 ⇒ pX + pY = 20
Ta có: X chỉ có thể là: H (p = 1); He (p = 2); Na (p = 11) và K (p = 19).
⇒ Ta thấy chỉ có Na (p = 11) ⇒ pY = 9 (Flo) thỏa mãn.
⇒ X - Y: NaF (liên kết ion)
Đúng 0
Bình luận (0)
Nguyên tử nguyên tố X có electron cuối cùng thuộc phân lớp s, nguyên tử nguyên tố Y có electron cuối cùng thuộc phân lớp p. Biết rằng tổng số electron trong nguyên tử của X và Y là 20. Bản chất của liên kết hóa học trong hợp chất X – Y là: A. sự góp chung đôi electron B. sự góp đôi electron từ một nguyên tử C. sự tương tác yếu giữa hai nguyên tử có chênh lệch độ âm điện lớn D. lực hút tĩnh điện giữa hai ion trái dấu
Đọc tiếp
Nguyên tử nguyên tố X có electron cuối cùng thuộc phân lớp s, nguyên tử nguyên tố Y có electron cuối cùng thuộc phân lớp p. Biết rằng tổng số electron trong nguyên tử của X và Y là 20. Bản chất của liên kết hóa học trong hợp chất X – Y là:
A. sự góp chung đôi electron
B. sự góp đôi electron từ một nguyên tử
C. sự tương tác yếu giữa hai nguyên tử có chênh lệch độ âm điện lớn
D. lực hút tĩnh điện giữa hai ion trái dấu
Đáp án : D
X có e cuối thuộc phân lớp s => nhóm A(I hoặc II)
Y có e cuối thuộc phân lớp p => nhóm A (III à VIII)
, eX + eY = 20 => pX + pY = 20
Ta có : X chỉ có thể là : H( p =1) ; He (p =2) ; Na(p = 11) và K(p = 19)
=> Ta thấy Chỉ có Na (p = 11) => pY = 9 (Flo) thỏa mãn
=> X – Y : NaF ( liên kết ion )
Đúng 0
Bình luận (0)
Một nguyên tử X có tổng số electron ở các phân lớp s là 6 và tổng số electron lớp ngoài cùng là 6. Cho biết X thuộc về nguyên tố hóa học nào sau đây? A. Flo (Z 9) B. Lưu huỳnh (Z 16) C. Clo (Z 17) D. Oxi (Z 8)
Đọc tiếp
Một nguyên tử X có tổng số electron ở các phân lớp s là 6 và tổng số electron lớp ngoài cùng là 6. Cho biết X thuộc về nguyên tố hóa học nào sau đây?
A. Flo (Z = 9)
B. Lưu huỳnh (Z = 16)
C. Clo (Z = 17)
D. Oxi (Z = 8)
Các nguyên tố thuộc cùng một nhóm A có tính chất hóa học tương tự nhau, vì vỏ nguyên tử các nguyên tố nhóm A có:
A. Số electron như nhau.
B. Số lớp electron như nhau.
C. Số electron thuộc lớp ngoài cùng như nhau.
D. Cùng số electron s hay p.
Chọn câu C: có số electron lớp ngoài cùng như nhau.
Đúng 0
Bình luận (0)
Nguyên tố X và Y thuộc nhóm A;nguyên tử nguyên tố X có 7 electron trên các phân lớp s, nguyên tử nguyên tố Y có 17 electron trên các phân lớp p.Công thức hợp chất tạo bởi X và Y; liên kết hóa học trong hợp chất đó là: A. XY; liên kết ion. B. Y2X; liên kết ion. C. X5Y; liên kết cộng hoá trị. D. X7Y; liên kết cộng hoá trị.
Đọc tiếp
Nguyên tố X và Y thuộc nhóm A;nguyên tử nguyên tố X có 7 electron trên các phân lớp s, nguyên tử nguyên tố Y có 17 electron trên các phân lớp p.Công thức hợp chất tạo bởi X và Y; liên kết hóa học trong hợp chất đó là:
A. XY; liên kết ion.
B. Y2X; liên kết ion.
C. X5Y; liên kết cộng hoá trị.
D. X7Y; liên kết cộng hoá trị.
Đáp án A
Nguyên tử nguyên tố X có 7 electron trên các phân lớp s
⇒ X: 1s22s23s24s25s1
Vì thuộc nhóm A nên X thuộc nhóm IA
nguyên tử nguyên tố Y có 17 electron trên các phân lớp p
⇒ Y: 2p63p64p5 ⇒ 4s24p5
Vì Y thuộc nhóm A ⇒ X thuộc nhóm VIIA
⇒ Hợp chất XY: liên kết ion
Đúng 0
Bình luận (0)
Một nguyên tử X có tổng số electron ở các phân lớp s là 6 và tổng số electron ở lớp ngoài cùng là 6. Cho biết X thuộc về nguyên tố hóa học nào sau đây? A. Oxi (Z 8). B. Lưu huỳnh (Z 16). C. Flo (Z 9). D. Clo (Z 17).
Đọc tiếp
Một nguyên tử X có tổng số electron ở các phân lớp s là 6 và tổng số electron ở lớp ngoài cùng là 6. Cho biết X thuộc về nguyên tố hóa học nào sau đây?
A. Oxi (Z = 8).
B. Lưu huỳnh (Z = 16).
C. Flo (Z = 9).
D. Clo (Z = 17).
X có tổng số electron ở các phân lớp s là 6 và tổng số electron lớp ngoài cùng là 6.
→ Cấu hình electron của X là: 1s22s22p63s23p4
→ Số hiệu nguyên tử của X = số electron = 16 → Chọn B.
Đúng 0
Bình luận (0)
Nguyên tố X và Y thuộc nhóm A; nguyên tử nguyên tố X có 7 electron trên các phân lớp s, nguyên tử nguyên tố Y có 17 electron trên các phân lớp p. Công thức hợp chất tạo bởi X và Y; liên kết hóa học trong hợp chất đó là A. XY; liên kết ion. B. Y2X; liên kết ion. C. X5Y; liên kết cộng hoá trị. D. X7Y; liên kết cộng hoá trị.
Đọc tiếp
Nguyên tố X và Y thuộc nhóm A; nguyên tử nguyên tố X có 7 electron trên các phân lớp s, nguyên tử nguyên tố Y có 17 electron trên các phân lớp p. Công thức hợp chất tạo bởi X và Y; liên kết hóa học trong hợp chất đó là
A. XY; liên kết ion.
B. Y2X; liên kết ion.
C. X5Y; liên kết cộng hoá trị.
D. X7Y; liên kết cộng hoá trị.
Nguyên tố X và Y thuộc nhóm A; nguyên tử nguyên tố X có 7 electron trên các phân lớp s, nguyên tử nguyên tố Y có 17 electron trên các phân lớp p. Công thức hợp chất tạo bởi X và Y; liên kết hóa học trong hợp chất đó là A. XY; liên kết ion. B. Y2X; liên kết ion. C. X5Y; liên kết cộng hoá trị. D. X7Y; liên kết cộng hoá trị.
Đọc tiếp
Nguyên tố X và Y thuộc nhóm A; nguyên tử nguyên tố X có 7 electron trên các phân lớp s, nguyên tử nguyên tố Y có 17 electron trên các phân lớp p. Công thức hợp chất tạo bởi X và Y; liên kết hóa học trong hợp chất đó là
A. XY; liên kết ion.
B. Y2X; liên kết ion.
C. X5Y; liên kết cộng hoá trị.
D. X7Y; liên kết cộng hoá trị.