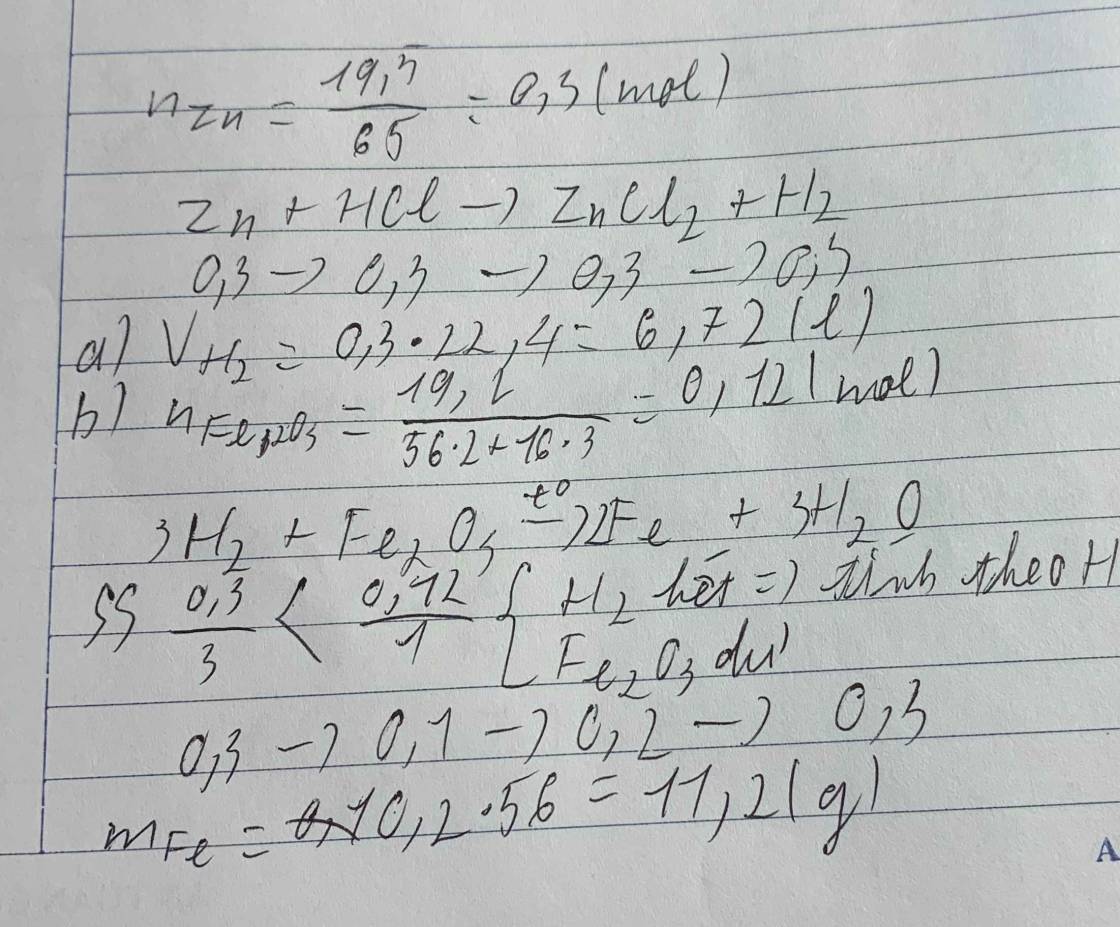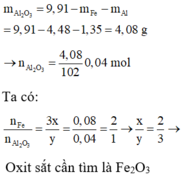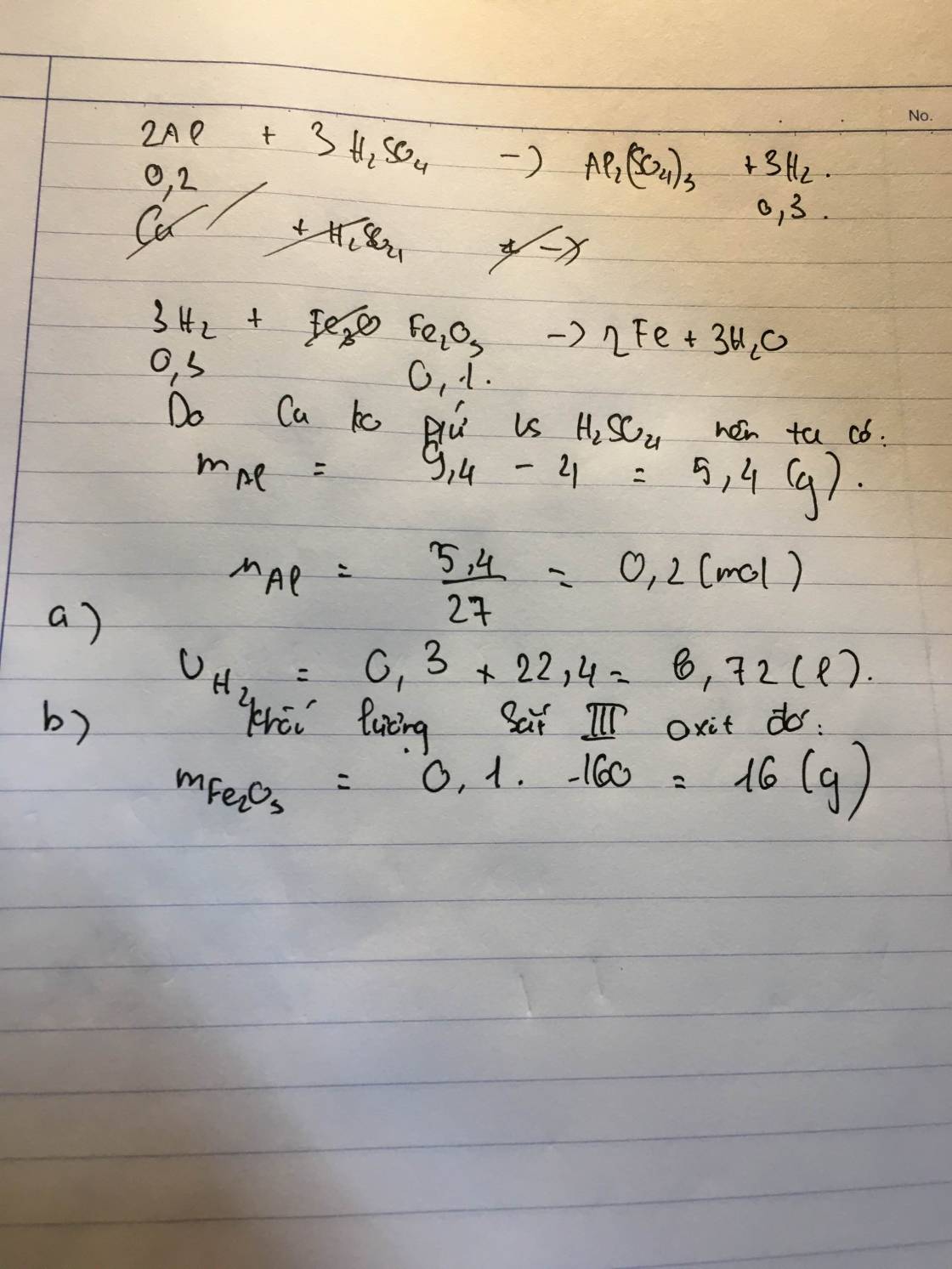Cho 1,5 g một oxit sắt tác dụng với khí H2 nhiệt độ cao thu được 1,05 g sắt. Tim CTHH của oxit sắt

Những câu hỏi liên quan
khử một oxit sắt bằng hidro ở nhiệt độ cao. Phản ứng xong thu được 0,84g sắt và 0.36 g nước. a. xác định CTHH của oxit sắt. b. Tính thể tích H2 tham gia phản ứng
Cho oxit sắt có công thức là: \(Fe_xO_y\)
\(n_{H2O}=\frac{0,36}{18}=0,02\left(mol\right)\)
\(n_{Fe}=\frac{0,84}{56}=0,015\left(mol\right)\)
Bảo toàn \(H,\) ta có:
\(N_{h2}=n_{H2O}=0,02\left(,ol\right)\)
Bảo toàn khối lượng, ta có:
\(m_{Fe_zO_y}=m_{H2O}+m_{Fe}-m_{H2}\)
\(\Rightarrow m_{Fe_zO_y}=0,84+0,36-0,02.2=1,16g\)
a) Phương trình:\(Fe_xO_y\)\(+\)\(yH_2\)\(→^{t^o}\)\(xFe\)\(+\)\(yH_2O\)
Ta nhận thấy: \(n_{Fe_zO_y}=\frac{^nFe}{x}=\frac{0,015}{x}\left(mol\right)\)
\(\Rightarrow M_{Fe_zO_y}=\frac{1,16}{\frac{0,015}{x}}=\frac{232}{3}\left\{x\right\}\)
\(\Rightarrow56x+16y=\frac{232}{3}x\)
\(\Rightarrow16y=\frac{64}{3}x\)
Ta có: \(x\le3,y\le4|x,y>0\)
+) Với \(x=1\rightarrow y=\frac{4}{3}\)( loại )
+) Với \(x=2\rightarrow y=\frac{8}{3}\)( loại )
+) Với \(x=3\rightarrow y=4\)( nhận )
Vậy oxit có công thức: \(Fe_3O_4\)
b) \(V_{H2}=0,02.22,4=0,448\left(l\right)\)
Cho 19,5 g kẽm tác dụng hết với dung dịch axit clohiđric. a. Tính thể tích khí H2 sinh ra (ở đktc). b. Nếu dùng thể tích H2 trên để khử 19,2 g sắt (III) oxit ở nhiệt độ cao thì thu được bao nhiêu gam sắt
Dùng khí H2 để khử hoàn toàn 4,64g một oxit sắt chưa rõ công thức ở nhiệt độ cao, sau phản ứng thu được 3,36g Fe. Xác định CTHH của oxit sắt
\(m_O=4.64-3.36=1.28\left(g\right)\)
\(n_{Fe}=\dfrac{3.36}{56}=0.06\left(mol\right)\)
\(n_O=\dfrac{1.28}{16}=0.08\left(mol\right)\)
\(n_{Fe}:n_O=0.06:0.08=3:4\)
\(CT:Fe_3O_4\)
Đúng 1
Bình luận (0)
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau: - Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc). - Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra. Công thức của oxit sắt là A. Fe2O3. B. Fe3O4. C. FeO. D. Không xác định được.
Đọc tiếp
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau:
- Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc).
- Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra.
Công thức của oxit sắt là
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Không xác định được.
Đáp án A
Ta có sơ đồ phản ứng:
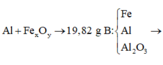
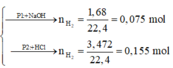
Phần 1:
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
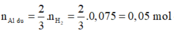
![]()
Phần 2:
2Al + 6HCl → 2AlCl3 + 3H2↑ (1)
0,05 → 0,075
Fe + 2HCl → FeCl2 + H2↑ (2)
![]()
![]()
![]()
![]()
Ta có phương trình phản ứng:
![]()
Khối lượng các chất trong 1 phần hỗn hợp B là 19,82/2 = 9,91 g
![]()
![]()
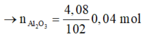
Ta có:
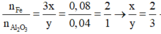
=> Oxit sắt cần tìm là Fe2O3
Đúng 0
Bình luận (0)
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau: - Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc). - Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra. Công thức của oxit sắt là A. Fe2O3. B. Fe3O4. C. FeO. D. Không xác định được.
Đọc tiếp
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau:
- Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc).
- Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra.
Công thức của oxit sắt là
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Không xác định được.
dùng khí h2 vừa đủ để khử hoàn toàn 34,8g một oxit sắt ở nhiệt độ cao. Sau khi phản ứng kết thúc thu được 25,2g sắt, làm lạnh hơi nước thu được sau phản ứng. a. tính thể tích khí H2 đã phản ứng ở đktc b. xác định CTHH của oxit sắt đó c. tính thể tích nước thu đc ở thể lỏng ( giải thích các bước làm )
a) \(n_O=\dfrac{34,8-25,2}{16}=0,6\left(mol\right)\)
=> \(n_{H_2O}=0,6\left(mol\right)\) (bảo toàn O)
=> \(n_{H_2}=0,6\left(mol\right)\) (bảo toàn H)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
b) \(n_{Fe}=\dfrac{25,2}{56}=0,45\left(mol\right)\)
nFe : nO = 0,45 : 0,6 = 3 : 4
=> CTHH: Fe3O4
c) \(m_{H_2O}=0,6.18=10,8\left(g\right)\)
Mà \(d_{H_2O}=1\left(g/ml\right)\)
=> \(V_{H_2O}=10,8\left(ml\right)\)
Đúng 2
Bình luận (0)
Cho 2,24l h2 tác dụng vừa đủ với 5,8g fexoy ở nhiệt độ cao. Xác định cthh của oxit sắt.
FexOy + yH2 ---> xFe + yH2O
0,1/y 0,1 mol
Suy ra: 56x + 16y = 58y hay 56x = 42y hay 4x = 3y hay x:y = 3:4
Fe3O4.
Đúng 0
Bình luận (0)
Cho 180g sắt (III) oxit Fe2O3 tác dụng vừa đủ với 70g cacbon oxit CO ở nhiệt độ cao, thu được sắt Fe và 110g khí cacbonic CO2. Khối lượng sắt thu được là : A. 40g B. 80g C. 120g D. 140g Giúp mình đi mà .
Bảo toàn KL: \(m_{Fe_2O_3}+m_{CO}=m_{Fe}+m_{CO_2}\)
\(\Rightarrow m_{Fe}=180+70-110=140\left(g\right)\)
Chọn D
Đúng 1
Bình luận (0)
3. Cho 9,4 g hỗn hợp nhôm và đồng tác dụng với axit sunfuric vừa đủ. Sau phản ứng thấy có 4 g chất rắn không tan.
a) Tính thể tích khí thoát ra ở đktc.
b) Lượng khí thu được trên khử vừa đủ một lượng sắt III oxit ở nhiệt độ cao. Tính khối lượng của sắt III oxit đó.