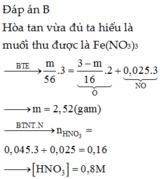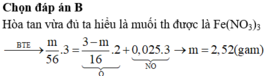Oxi hoá chậm m gam Fe ngoài không khí thu được 12g hỗn hợp A gồm FeO, Fe2O3, Fe3O4 và Fe dư. Hoà tan hỗn hợp A vừa đủ bởi dung dịch HNO3 thu được 2,24 lít NO duy nhất (đktc). Khối lượng m gam Fe ban đầu là:

Những câu hỏi liên quan
Oxi hoá chậm m gam Fe ngoài không khí thu được 12 gam hỗn hợp A gồm FeO, Fe2O3, Fe3O4 và Fe dư. Hoà tan A bằng lượng vừa đủ 200 ml dd HNO3 thu được 2,24 lít NO duy nhất đktc. Tính m và CM dd HNO3 (Fe56;O16; N14; H1) A. Kết quả khác B. 10,08 g và 2M C. 10,08 g và 3,2M D. 6,72 gam và 2M
Đọc tiếp
Oxi hoá chậm m gam Fe ngoài không khí thu được 12 gam hỗn hợp A gồm FeO, Fe2O3, Fe3O4 và Fe dư. Hoà tan A bằng lượng vừa đủ 200 ml dd HNO3 thu được 2,24 lít NO duy nhất đktc. Tính m và CM dd HNO3 (Fe=56;O=16; N=14; H=1)
A. Kết quả khác
B. 10,08 g và 2M
C. 10,08 g và 3,2M
D. 6,72 gam và 2M
Đáp án C
Qui hỗn hợp về dạng:
Fe và O => mFe + mO = 12g (1)
nNO = 2,24: 22,4 = 0,1 mol
Bảo toàn e: 3nFe = 2nO + 3nNO => 3nFe – 2nO = 0,3 mol (2)
Từ (1,2) => nFe = 0,18 ; nO = 0,12 mol
=> nHNO3 = 4nNO + 2nO = 4.0,1 + 2.0,12 = 0,64 mol
=> CM (HNO3) = 0,64: 0,2 = 3,2 M
m = mFe = 0,18.56 = 10,08g
Đúng 0
Bình luận (0)
Oxi hóa chậm m gam Fe ngoài không khí thu được 3 gam hỗn hợp A gồm FeO, Fe3O4, Fe2O3 và Fe dư. Hòa tan A vừa đủ bởi 200 ml dung dịch HNO3 thu được 0,56 lít NO duy nhất (đktc). Tính m và nồng độ mol/l của dung dịch HNO3 A. Đáp án khác B. 2,52 gam và 0,8M C. 1,94 gam và 0,5M D. 1,94 gam và 0,8M
Đọc tiếp
Oxi hóa chậm m gam Fe ngoài không khí thu được 3 gam hỗn hợp A gồm FeO, Fe3O4, Fe2O3 và Fe dư. Hòa tan A vừa đủ bởi 200 ml dung dịch HNO3 thu được 0,56 lít NO duy nhất (đktc). Tính m và nồng độ mol/l của dung dịch HNO3
A. Đáp án khác
B. 2,52 gam và 0,8M
C. 1,94 gam và 0,5M
D. 1,94 gam và 0,8M
Oxi hóa chậm m gam Fe ngoài không khí thu được 3 gam hỗn hợp A gồm FeO, Fe3O4, Fe2O3 và Fe dư. Hòa tan A vừa đủ bởi 200 ml dung dịch HNO3 thu được 0,56 lít NO duy nhất (đktc). Tính m và nồng độ mol/l của dung dịch HNO3 A.Đáp án khác B.2,52 gam và 0,8M C. 1,94 gam và 0,5M D. 1,94 gam và 0,8M
Đọc tiếp
Oxi hóa chậm m gam Fe ngoài không khí thu được 3 gam hỗn hợp A gồm FeO, Fe3O4, Fe2O3 và Fe dư. Hòa tan A vừa đủ bởi 200 ml dung dịch HNO3 thu được 0,56 lít NO duy nhất (đktc). Tính m và nồng độ mol/l của dung dịch HNO3
A.Đáp án khác
B.2,52 gam và 0,8M
C. 1,94 gam và 0,5M
D. 1,94 gam và 0,8M
Nung m gam Fe trong không khí, sau một thời gian ta thu được 11,2 gam hỗn hợp chất rắn X gồm Fe,
Fe
2
O
3
,
Fe
3
O
4
, FeO. Hoà tan hết 11,2 gam hỗn hợp chất rắn X vào dung dịch
HNO
3
dư thu được 2,24 lít khí
NO
2
(đktc) là sản phẩm khử duy nhất....
Đọc tiếp
Nung m gam Fe trong không khí, sau một thời gian ta thu được 11,2 gam hỗn hợp chất rắn X gồm Fe, Fe 2 O 3 , Fe 3 O 4 , FeO. Hoà tan hết 11,2 gam hỗn hợp chất rắn X vào dung dịch HNO 3 dư thu được 2,24 lít khí NO 2 (đktc) là sản phẩm khử duy nhất. Giá trị m là:
A. 7,28
B. 5,6
C. 8,40
D. 7,40
Nung m gam Fe trong không khí, thu được 104,8g hỗn hợp A gồm Fe, FeO, Fe2O3, Fe3O4. Hoà tan hoàn toàn A trong dung dịch HNO3 dư, thu được dung dịch B và 12,096 lít hỗn hợp khí C gồm NO và NO2 (đktc) có tỉ khối so với He là 10,167. Giá trị của m là
Nung 8,4 gam Fe trong không khí, sau phản ứng thu được m gam X gồm Fe, FeO,
Fe
2
O
3
và
Fe
3
O
4
. Hoà tan m gam hỗn hợp X bằng
HNO
3
dư, thu được 2,24 lít khí
NO
2
(đktc) là sản phẩm khử duy nhất. Giá trị m là A. 11,2 gam B. 25,2 gam...
Đọc tiếp
Nung 8,4 gam Fe trong không khí, sau phản ứng thu được m gam X gồm Fe, FeO, Fe 2 O 3 và Fe 3 O 4 . Hoà tan m gam hỗn hợp X bằng HNO 3 dư, thu được 2,24 lít khí NO 2 (đktc) là sản phẩm khử duy nhất. Giá trị m là
A. 11,2 gam
B. 25,2 gam
B. 25,2 gam
D. 6,8 gam.
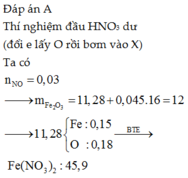
Cho 11,28 gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư thu được 0,672 lít khí NO sản phẩm khử duy nhất (ở đktc) và dung dịch Y. Dung dịch Y có thể hoà tan được tối đa 5,88 gam Fe (thu được khí NO và dung dịch Z). Khối lượng muối có trong Z là: A. 45,9 gam B. 43,8 gam C. 48,8 gam D. 40,6 gam
Đọc tiếp
Cho 11,28 gam hỗn hợp X gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư thu được 0,672 lít khí NO sản phẩm khử duy nhất (ở đktc) và dung dịch Y. Dung dịch Y có thể hoà tan được tối đa 5,88 gam Fe (thu được khí NO và dung dịch Z). Khối lượng muối có trong Z là:
A. 45,9 gam
B. 43,8 gam
C. 48,8 gam
D. 40,6 gam
Oxi hoá chậm m gam Fe ngoài KK thu được 12 gam hỗn hợp A gồm FeO , Fe2O3 , Fe3O4 và Fe dư . Hoà tan A bằng lượng vừa đủ 200 ml dd HNO3 thu được 2,24 lít NO ! ở đktc . Tính m và CM dd HNO3:
Fe→Fe 3
O→ O {-2}
N{+5}→N{+2}
nFe=m/56
nO=(12-m)/16
nNO=0,1
Ta có:3nFe = 2nO + 3nNO
<=>3(m/56) = 2(12-m)/16 + 3*0,1
<=> m = 10,08
nHNO3 = 3*m/56 + nNO = 3*10,08/56 + 0,1 = 0,64(mol)
CM = 0,64/0,2 = 3,2 (M)
O→ O {-2}
N{+5}→N{+2}
nFe=m/56
nO=(12-m)/16
nNO=0,1
Ta có:3nFe = 2nO + 3nNO
<=>3(m/56) = 2(12-m)/16 + 3*0,1
<=> m = 10,08
nHNO3 = 3*m/56 + nNO = 3*10,08/56 + 0,1 = 0,64(mol)
CM = 0,64/0,2 = 3,2 (M)
Đúng 0
Bình luận (0)
Fe→Fe 3
O→ O {-2}
N{+5}→N{+2}
nFe=m/56
nO=(12-m)/16
nNO=0,1
Ta có:3nFe = 2nO + 3nNO
<=>3(m/56) = 2(12-m)/16 + 3*0,1
<=> m = 10,08
nHNO3 = 3*m/56 + nNO = 3*10,08/56 + 0,1 = 0,64(mol)
CM = 0,64/0,2 = 3,2 (M)
O→ O {-2}
N{+5}→N{+2}
nFe=m/56
nO=(12-m)/16
nNO=0,1
Ta có:3nFe = 2nO + 3nNO
<=>3(m/56) = 2(12-m)/16 + 3*0,1
<=> m = 10,08
nHNO3 = 3*m/56 + nNO = 3*10,08/56 + 0,1 = 0,64(mol)
CM = 0,64/0,2 = 3,2 (M)
Đúng 0
Bình luận (3)
Oxi hoá chậm m gam Fe ngoài KK thu được 12 gam hỗn hợp A gồm FeO , Fe2O3 , Fe3O4 và Fe dư . Hoà tan A bằng lượng vừa đủ 200 ml dd HNO3 thu được 2,24 lít NO ! ở đktc . Tính m và CM dd HNO3:
Bài này nếu là trắc nghiệm thì làm như sau:
Áp dung công thức kinh ngiệm: mFe=0,7mhh + 5,6 ne
Thay số vào thì được: m=0,7.12 + 5,6.2,24/22,4*3= 10,08 g
Nếu là tự luận thì làm theo bảo toàn e.
Fe .... -3e ---> Fe (3+)
m/56 3m/56
O2 .................. +4e ---> 2O (2-)
(12 - m)/32 ---> (12 - m)/8
N (+5) +3e ---> N (+2)
........... 0,3 <--- 0,1
Áp dụng định luật bảo toàn e: 3m/56 = (12-m)/8 + 0,3
Giải ra đc m = 10,08 g
Còn tính C M dd HNO3 thì làm chung theo cách sau:
Áp dụng ĐLBTNT Nitơ : n HNO3 = n NO + 3n Fe(NO3)3 = n NO + 3n Fe = 0,1 + 3*0,18 = 0,64
=> Cm dd HNO3 = 0,64/0,2 = 3,2 M
Đúng 1
Bình luận (0)