Trong phòng thí nghiệm người ta điều chế Fe bằng cách cho kh í H2 đi qua ống sứ đựng Fe2O3 nung nóng và thu được 11,2g Fe
a/ Viết phương trình hóa học của các phản ứng?
b/ Tính khối lượng Fe2O3 đã tham gia p ư.
c/ Tính thể tích H2 (đktc) đã dùng?
Bài 1: Viết phương trình phản ứng cho mỗi thí nghiệm sau:
1. Dẫn khí CO (dư) đi qua ống sứ đựng Fe2O3 nung nóng
………………………………………………………………………………………………………………………………………………………………………………………………
2. Dẫn khí CO (dư) đi qua ống sứ đựng Al2O3 và Fe2O3 nung nóng
………………………………………………………………………………………………
………………………………………………………………………………………………
3. Dẫn khí CO2 vào dung dịch Ca(OH)2 (dư)
………………………………………………………………………………………………
………………………………………………………………………………………………
4. Dẫn khí CO2 (dư) vào dung dịch Ca(OH)2
………………………………………………………………………………………………
………………………………………………………………………………………………
5. Dẫn hỗn hợp khí CO và CO2 vào dung dịch Ba(OH)2 dư
………………………………………………………………………………………………
………………………………………………………………………………………………
\(1.\)\(Fe_2O_3+3CO\underrightarrow{^{^{t^0}}}3Fe+3CO_2\)
\(2.\)\(Fe_2O_3+3CO\underrightarrow{^{^{t^0}}}3Fe+3CO_2\)
\(3.Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
\(4.Ca\left(OH\right)_2+2CO_2\rightarrow Ca\left(HCO_3\right)_2\)
\(5.Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
1) \(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
2)
\(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
3) \(Ca\left(OH\right)_2+CO_2->CaCO_3\downarrow+H_2O\)
4) \(Ca\left(OH\right)_2+CO_2->CaCO_3\downarrow+H_2O\)
\(CaCO_3+CO_2+H_2O->Ca\left(HCO_3\right)_2\)
5) \(Ba\left(OH\right)_2+CO_2->BaCO_3\downarrow+H_2O\)
Hỗn hợp X gồm Fe, FeO và Fe2O3. Cho một luồng CO đi qua ống sứ đựng m gam hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm thu được 64 gam chất rắn A trong ống sứ và 11,2 lít khí B (đktc) có tỉ khối so với H2 là 20,4. Tính giá trị m
A. 35,2 gam
B. 105,6 gam
C. 70,4 gam
D. 140,8 gam
Đáp án : C
Tổng quát : CO + OOxit -> CO2
,nB = 0,5 mol ; MB = 40,8g => có CO và CO2
=> nCO = 0,1 ; nCO2 = 0,4 mol
=> mX = mA + mO pứ = 64 + 0,4.16 = 70,4g
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam
chon C nha
Hỗn hợp X gồm Fe, FeO và Fe2O3. Cho một luồng CO đi qua ống sứ đựng m gam hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm thu được 64 gam chất rắn A trong ống sứ và 11,2 lít khí B (đktc) có tỉ khối so với H2 là 20,4. Tính giá trị m.
A. 105,6 gam.
B. 35,2 gam.
C. 70,4 gam.
D. 140,8 gam.
Các phản ứng khử sắt oxit có thể có:
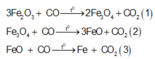
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 Fe2O3 dư hoặc ít chất hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, các bạn chỉ cần quan sát và nhận thấy luôn có: n C O 2 = n C O
n B = 11 , 2 22 , 4 = 0 , 5 m o l .
Ta có B gồm CO2 mới tạo thành và CO dư
Gọi:
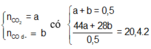

Áp dụng định luật bảo toàn khối lượng ta có:
![]()
⇒ m = 64 + 0,4.44 - 0,4.28 = 60,4 (gam)
Đáp án C.
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.
chọn C nha
Hỗn hợp X gồm Fe, FeO và Fe2O3. Cho một luồng CO đi qua ống sứ đựng m gam hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm thu được 64 gam chất rắn A trong ống sứ và 11,2 lít khí B (đktc) có tỉ khối so với H2 là 20,4. Tính giá trị m.
\(n_{CO\left(dư\right)}=a\left(mol\right)\)
\(n_{CO_2}=b\left(mol\right)\)
\(n_B=a+b=0.5\left(mol\right)\left(1\right)\)
\(m_B=2\cdot20.4\cdot0.5=20.4\left(g\right)\)
\(\Rightarrow28a+44b=20.4\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.4\)
\(n_{CO\left(pư\right)}=n_{CO_2}=0.4\left(mol\right)\)
\(BTKL:\)
\(m_X+m_{CO}=m_A+m_B\)
\(\Leftrightarrow m_X=64+0.4\cdot44-0.4\cdot28=70.4\left(g\right)\)
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.
Cho 11g hỗn hợp Al, Fe tác dụng với một lượng dư dung dịch axit Clohidric. Sau khi các phản ứng xảy ra hoàn toàn, thu được V lít H2 (đktc). Dẫn toàn bộ lượng khí H2 này đi chậm qua ống sứ đựng 32g CuO nung nóng. Sau một thời gian, thấy trong ống sứ còn lại 26,88g chất rắn và chỉ có 80% H2 đã phản ứng.
a) Viết phương trình hóa học của các phản ứng xảy ra.
b) Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)
Dẫn khí H2 đi qua lọ đựng Fe2O3 nung nóng thu được 11, 2 g Fe và nước. a. Tính VH2 đã phản ứng (đctc) b. Tính khối lượng Fe2O3 cần dùng ( 2 cách)
Câu 7: Dẫn luồng khí CO đi qua ống chứa 56gam Fe2O3 nung nóng. Sau một thời gian ta thu được 48,8gam chất rắn X. Biết khí CO khử Fe2O3 thành Fe
a) Viết phương trình phản ứng xảy ra
b) Tính khối lượng Fe có trong rắn X
Câu 9: Cho các chất : nitơ lỏng, amoniac lỏng, phốt phua kẽm, cacbonic rắn, sô đa, đá vôi, silic, silicagen
Mỗi câu hỏi dưới đây, học sinh chỉ được nêu đúng 1 hoá chất thích hợp (trong các hoá chất nêu trên)
a) Chất làm thuốc diệt chuột
b) Chất dùng làm chất hút ẩm
c) Chất dùng trong công nghiệp thuỷ tinh, đồ gốm, bột giặt
d) Chất gây lạnh trong các thiết bị, máy móc làm lạnh
Câu 7
a) Fe2O3 + 3CO --to--> 2Fe + 3CO2
b) \(n_{Fe_2O_3}=\dfrac{56}{160}=0,35\left(mol\right)\)
Fe2O3 + 3CO --to--> 2Fe + 3CO2
_a---------------------->2a
=> 160(0,35-a) + 56.2a = 48,8
=> a = 0,15
=> nFe = 2a.56 = 16,8 (g)
Câu 9
a) phốt phua kẽm
b) silicagen
c) sô đa
d) cacbonic rắn
Hỗn hợp X gồm Fe, FeO và Fe2O3. Cho một luồng CO đi qua ống sứ đựng m gam hỗn hợp X nung nóng. Sau khi kết thúc thí nghiệm thu được 64 gam chất rắn A trong ống sứ và 11,2 lít khí B (đktc) có tỉ khối so với H2 là 20,4. Tính giá trị m.
bạn hãy xác định xem khí B gồm những khí gì (99.9% các bài đều có lẫn khí CO và H2) .sau đó dùng qui tắc đường chéo để xđ tỉ lệ số mol 2 khí như vậy sẽ dễ làm hơn
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.
chon C nha
Bài 2: Khi cho khí hidro đi qua bột sắt(III) oxit ( Fe2O3 ) nung nóng người ta thu được sắt theo sơ đồ phản ứng: Fe2O3 + H2 Fe + H2O
a) Viết phương trình phản ứng
b) Nếu sau phản ứng người ta thu được 21g sắt thì khối lượng sắt(III) oxit tham gia phản ứng là bao nhiêu?
\(a,Fe_2O_3+3H_2\to2Fe+3H_2O\\ b,n_{Fe}=\dfrac{21}{56}=0,375(mol)\\ \Rightarrow n_{Fe_2O_3}=0,1875(mol)\\ \Rightarrow m_{Fe_2O_3}=0,1875.160=30(g)\)