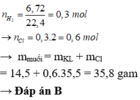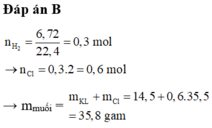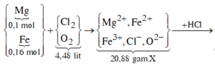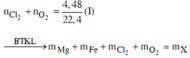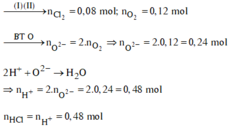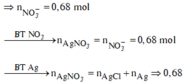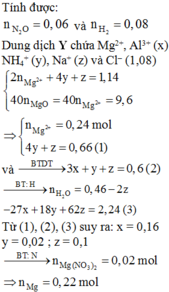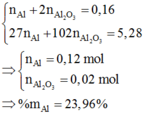cho 16g hỗn hợp X gồm 3 kim loại Mg , Al, Fe vào 2 lít dung dịch HCl 0.35M, phản ứng kết thúc thu được dung dịch A và 6.72l khí ở đktc. Cho biết axit HCl hết hay dư? Tính tổng khối lượng muối có trong dung dịch A?

Những câu hỏi liên quan
cho 8 gam hỗn hợp X gồm 3 kim loại Mg, Al, Fe vào dung dịch chứa 12,7 gam axit HCl, phản ứng kết thúc thu được dung dịch A và 3,36 lít khí (đktc)
a) Axit HCl hết hay dư ?
b)Tổng khối lượng muối có trong dung dịch A?
c) cho 8g hỗn hợp X trên vào dung dịch H2SO4 dư , phản ứng xong thu được V lít khí H2 ở ( đktc). tính khối lượng H2SO4 đem thí nghiệm, biết lượng axit lấy dư 10%
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
a) Ta có: \(\left\{{}\begin{matrix}n_{HCl}=\dfrac{12,7}{36,5}=\dfrac{127}{365}\left(mol\right)\\n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\end{matrix}\right.\)
Ta thấy: \(2n_{H_2}< n_{HCl}\) \(\Rightarrow\) Axit còn dư
b) Theo PTHH: \(n_{HCl\left(p/ứ\right)}=2n_{H_2}=0,3\left(mol\right)\) \(\Rightarrow m_{HCl}=0,3\cdot36,5=10,95\left(g\right)\)
Mặt khác: \(m_{H_2}=0,15\cdot2=0,3\left(g\right)\)
Bảo toàn khối lượng: \(m_{muối}=m_{KL}+m_{HCl\left(p/ứ\right)}-m_{H_2}=18,65\left(g\right)\)
Đúng 2
Bình luận (1)
cho 16g hỗn hợp X gồm 3 kim loại Mg,Al,Fe vào dung dịch chứa 25,55g dung dịch axit HCl,phản ứng kết thúc thu đc dung dịch A và 6,72g chất khí (đkt).
a,axit HCl hết hay dư?
b,tính tộng khối lượng muối có trong dung dịch A?
tham khảo : # Trương Hồng Hạnh
X gồm Mg, Al, Fe
Mg + 2HCl => MgCl2 + H2
2Al + 6HCl => 2AlCl3 + 3H2
Fe + 2HCl => FeCl2 + H2
nH2 = V/22.4 = 6.72/22.4 = 0.3 (mol)
Ta thấy: theo phương trình, nHCl = 2nH2
==> nHCl = 0.3x2 = 0.6 (mol)
mHCl = n.M = 0.6x36.5 = 21.9 (g)
mHCl phản ứng =21.9 < mHCl = 25.55
===> dung dịch HCl dư
Theo định luật BTKL: ta có:
m muối = 21.9 + 16 - 0.3x2 = 37.3 (g)
Đúng 1
Bình luận (1)
Hòa tan hết 11,61 gam hỗn hợp bột kim loại Mg, Al, Zn, Fe bằng 500ml dung dịch hỗn hợp axit HCl 1,5M và H2SO4 0,45M (loãng) thu được dung dịch X và 13,44 lít khí H2 (đktc). Cho rằng các axit phản ứng đồng thời với các kim loại. Tổng khối lượng muối tạo thành sau phản ứng là A. 38,935 gam B. 59,835 gam C. 38,395 gam D. 40,935 gam
Đọc tiếp
Hòa tan hết 11,61 gam hỗn hợp bột kim loại Mg, Al, Zn, Fe bằng 500ml dung dịch hỗn hợp axit HCl 1,5M và H2SO4 0,45M (loãng) thu được dung dịch X và 13,44 lít khí H2 (đktc). Cho rằng các axit phản ứng đồng thời với các kim loại. Tổng khối lượng muối tạo thành sau phản ứng là
A. 38,935 gam
B. 59,835 gam
C. 38,395 gam
D. 40,935 gam
Đáp án : B
Vì phản ứng các axit đồng thời => số mol HCl và H2SO4 phản ứng theo tỷ lệ mol giống như nồng độ mol ban đầu của chúng
=> nHCl : nH2SO4 = 1,5 : 0,45 = 10 : 3 = 10x : 3x
=> 2nH2 = nHCl + 2nH2SO4 => 1,2 mol = 10x + 2.3x
=> x = 0,075 mol
=> Trong muối có : 0,225 mol SO42- và 0,75 mol Cl- ; ion kim loại
( phản ứng hết axit)
=> mmuối = 11,61 + 0,225.96 + 0,75.35,5 = 59,835g
Đúng 0
Bình luận (0)
Hoà tan 14,5 gam hỗn hợp gồm ba kim loại Mg, Fe và Zn vừa đủ trong dung dịch HCl, kết thúc phản ứng thu được 6,72 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thu được khối lượng muối clorua khan là A. 38,5 gam B. 35,8 gam C. 25,8 gam D. 28,5 gam
Đọc tiếp
Hoà tan 14,5 gam hỗn hợp gồm ba kim loại Mg, Fe và Zn vừa đủ trong dung dịch HCl, kết thúc phản ứng thu được 6,72 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thu được khối lượng muối clorua khan là
A. 38,5 gam
B. 35,8 gam
C. 25,8 gam
D. 28,5 gam
Hoà tan 14,5 gam hỗn hợp gồm ba kim loại Mg, Fe và Zn vừa đủ trong dung dịch HCl, kết thúc phản ứng thu được 6,72 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thu được khối lượng muối clorua khan là A. 38,5 gam. B. 35,8 gam. C. 25,8 gam. D. 28,5 gam.
Đọc tiếp
Hoà tan 14,5 gam hỗn hợp gồm ba kim loại Mg, Fe và Zn vừa đủ trong dung dịch HCl, kết thúc phản ứng thu được 6,72 lít khí (đktc) và dung dịch X. Cô cạn dung dịch X thu được khối lượng muối clorua khan là
A. 38,5 gam.
B. 35,8 gam.
C. 25,8 gam.
D. 28,5 gam.
cho 16g hh X gồm 3 kim loại Mg, Al,Fe vào đ chứa 25,55g axit HCl, PƯ kết thúc thu được đ A và 6,72 lít khí(đktc). Axit HCl hết hay dư
Mg + 2HCl =====> MgCl2 + H2
2Al + 6HCl ====> 2AlCl3 +3H2
Fe + 2HCl ===> FeCl2 + H2
nH2=6,7222,4=0,3(mol)nH2=6,7222,4=0,3(mol)
ta có 10 mol HCl pư tạo thành 5 mol H2
0.6 mol HCl pư tạo thành 0.3 mol H2
nhưng thực tế 0.7mol HCl pư tạo thành 0.3mol H2
=======> HCl dư 0.1 mol
Đúng 1
Bình luận (0)
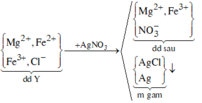
Đốt cháy hỗn hợp gồm 0,10 mol Mg và 0,16 mol Fe trong 4,48 lít (đktc) hỗn hợp khí gồm Cl2 và O2, thu được 20,88 gam hỗn hợp rắn X gồm các muối và oxit của kim loại (không thấy khí thoát ra). Hòa tan X trong dung dịch HCl loãng, thu được dung dịch Y chỉ chứa các muối. Cho dung dịch AgNO3 dư vào Y, kết thúc phản ứng thu được Y, kết thúc phản ứng thu được m gam kết tủa. Giá trị của m là: A. 98,32. B. 96,16. C. 91,84. D. 94,00.
Đọc tiếp
Đốt cháy hỗn hợp gồm 0,10 mol Mg và 0,16 mol Fe trong 4,48 lít (đktc) hỗn hợp khí gồm Cl2 và O2, thu được 20,88 gam hỗn hợp rắn X gồm các muối và oxit của kim loại (không thấy khí thoát ra). Hòa tan X trong dung dịch HCl loãng, thu được dung dịch Y chỉ chứa các muối. Cho dung dịch AgNO3 dư vào Y, kết thúc phản ứng thu được Y, kết thúc phản ứng thu được m gam kết tủa. Giá trị của m là:
A. 98,32.
B. 96,16.
C. 91,84.
D. 94,00.
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch NaNO3 và 1,08 mol HCl (đun nóng). Sau khi kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2. Tỉ khối của Z so với He bằng 5. Cho Y tác dụng với dung dịch NaOH dư, thấy có 1,14 mol NaOH phản ứng, thu được kết tủa T. Nung T trong không khí tới khối lượng không đổi, thu được 9,6 gam rắn. Phần trăm khối lượng của Al có trong hỗn hợp X là A. 23,96%. B. 27,96% C. 19,97%...
Đọc tiếp
Hòa tan hết 13,52 gam hỗn hợp X gồm Mg(NO3)2, Al2O3, Mg và Al vào dung dịch NaNO3 và 1,08 mol HCl (đun nóng). Sau khi kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối và 3,136 lít (đktc) hỗn hợp khí Z gồm N2O và H2. Tỉ khối của Z so với He bằng 5. Cho Y tác dụng với dung dịch NaOH dư, thấy có 1,14 mol NaOH phản ứng, thu được kết tủa T. Nung T trong không khí tới khối lượng không đổi, thu được 9,6 gam rắn. Phần trăm khối lượng của Al có trong hỗn hợp X là
A. 23,96%.
B. 27,96%
C. 19,97%
D. 31,95%
Hoà tan hoàn toàn 11 gam hỗn hợp X gồm Al và Fe bằng dung dịch axit sunfuric loãng dư. Sau khi phản ứng phản ứng kết thúc thu được 8,96 lít khí (đktc).
a) Tính thành phần phần trăm về khối lượng mỗi kim loại trong hỗn hợp X.
b) Tính khối lượng muối khan thu được.
c) Lượng khí hiđro ở trên khử vừa đủ 23,2 gam oxit của kim loại M. Xác định CTHH của oxit đó.
Gọi x,y lần lượt là số mol của Al, Fe
nH2 = \(\dfrac{8,96}{22,4}\)=0,4 mol
Pt: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
......x.................................0,5x...........1,5x
.....Fe + H2SO4 --> FeSO4 + H2
.......y..........................y............y
Ta có hệ pt:
{27x+56y=11
1,5x+y=0,4
⇔x=0,2, y=0,1
% mAl = \(\dfrac{0,2.27}{11}\).100%=49,1%
% mFe = \(\dfrac{0,1.56}{11}\).100%=50,9%
mAl2(SO4)3 = 0,5x . 342 = 0,5 . 0,2 . 342 = 34,2 (g)
mFeSO4 = 152y = 152 . 0,1 = 15,2 (g)
Gọi CTTQ: MxOy
Pt: MxOy + yH2 --to--> xM + yH2O
\(\dfrac{0,4}{y}\)<-------0,4
Ta có: 232,2=\(\dfrac{0,4}{y}\)(56x+16y)
⇔23,2=\(\dfrac{22,4x}{y}\)+6,4
⇔\(\dfrac{22,4x}{y}\)=16,8
⇔22,4x=16,8y
⇔x:y=3:4
Vậy CTHH của oxit: Fe3O4
Đúng 1
Bình luận (0)