Tính: 15%+ 82,3%

Những câu hỏi liên quan
Đặt tính rồi tính:
b) 82,3 – 27,96
Tính nhanh 45,8+82,3+18,7+54,2= ?
45,8+82,3+18,7+54,2
=(45,8+54,2) + (82,3+18,7)
=100 + 100
= 200
Đúng 0
Bình luận (0)
Câu 3. Điền dấu thích hợp vào chỗ chấm:
a. 82,3 …….. 82,29
31,5 ……... 31,500
b. 9,843 ………. 9,85
80,7 ……….. 79,7
a. 82,3 …>….. 82,29
31,5 …=…... 31,500
b. 9,843 ……<…. 9,85
80,7 ……>….. 79,7
Đúng 0
Bình luận (0)
Điền dấu thích hợp vào chỗ chấm:
a. 82,3 …….. 82,29
31,5 ……... 31,500
b. 9,843 ………. 9,85
80,7 ……….. 79,7
a. 82,3 > 82,29
31,5 = 31,500
b. 9,843 < 9,85
80,7 > 79,7
Đúng 0
Bình luận (0)
tính bằng cách thuận tiện:
9,8 x 3,7 + 4,9 x 2 x 5,2 - 9,8 x 6,4 + 19,6 x 0,5
20,18 x 82,3 + 20,18 x 49,6 - 20,18 x 31,9
a: =9,8(3,7+5,2-6,4+1)=9,8*3,5=34,3
b: =20,18(82,3+49,6-31,9)=2018
Đúng 0
Bình luận (0)
Tính bằng cách thuận tiện:
a, 0,43 + \(\dfrac{25}{100}\) + 0,64 + \(\dfrac{57}{100}\) + 0,75 + \(\dfrac{46}{100}\)
b, 56,3 x 2,4 + 56,3 x 8,9 - 56,3 x 1,3
c, 9,8 x 3,7 + 4,9 x 2 x 5,2 - 9,8 x 6,4 + 19,6 x 5,5
d, 20,18 x 82,3 + 20,18 x 49,6 - 20,18 x 31,9
a: =(0,43+0,57)+(0,25+0,75)+(0,64+0,46)
=1+1+1,1=3,1
b: =56,3(2,4+8,9-1,3)=56,3x10=563
Đúng 1
Bình luận (0)
`43/100+25/100+64/100+57/100+75/100+46/100`
`=>``(43/100+57/100)+(25/100+75/100)+(64/100+46/100)`
`=>` `1 + 1 + 110/100`
`=>` `1/1 +1/1+110/100`
`=>` ` 2/1 + 110/100`
`=>` `310/100`
=>` `31/25`
Đúng 1
Bình luận (0)
tổng của 1 số thập phân và 1 số tự nhiên là 82,3 . Khi thực hiện phép tính , Mai đã quên víêt dấu phẩy của số thập phân rồi công 2 số tự nhiên lại nên có tổng mới là 106 .tìm số thập phân và số tự nhiên đó
Hoà tan 12,8 g kim loại hoá trị II trong một lượng vừa đủ dung dịch
H
N
O
3
60,0% (D 1,365 g/ml), thu được 8,96 lít (đktc) một khí duy nhất màu nâu đỏ. Tên của kim loại và thể tích dung dịch
H
N
O
3
đã phản ứng làA. đồng; 61,5 ml.B. chì; 65,1 ml.C. thuỷ ngân; 125,6 ml.D. sắt; 82,3 ml.
Đọc tiếp
Hoà tan 12,8 g kim loại hoá trị II trong một lượng vừa đủ dung dịch H N O 3 60,0% (D = 1,365 g/ml), thu được 8,96 lít (đktc) một khí duy nhất màu nâu đỏ. Tên của kim loại và thể tích dung dịch H N O 3 đã phản ứng là
A. đồng; 61,5 ml.
B. chì; 65,1 ml.
C. thuỷ ngân; 125,6 ml.
D. sắt; 82,3 ml.
Đáp án: A.
Phương trình hóa học:
![]()
Số mol khí
N
O
2
: 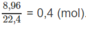
Theo phương trình hoá học :
n M = 0,2 mol và
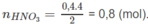
Khối lượng mol nguyên tử của kim loại M :
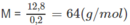
⇒ kim loại là Cu (đồng).
Gọi V (ml) là thể tích của dung dịch H N O 3 60,0%. Ta có phương trình liên hệ V với n H N O 3 :
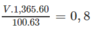
⇒ V = 61,5 ml
Đúng 0
Bình luận (0)
Hỗn hợp X gồm
K
C
l
O
3
,
C
a
C
l
O
3
2
,
C
a
C
l
2
và KCl có khối lượng 82,3 gam. Nhiệt phân hoàn toàn X thu được 13,44 lít
O
2
(đ...
Đọc tiếp
Hỗn hợp X gồm K C l O 3 , C a C l O 3 2 , C a C l 2 và KCl có khối lượng 82,3 gam. Nhiệt phân hoàn toàn X thu được 13,44 lít O 2 (đktc), chất rắn Y gồm C a C l 2 và KCl. Toàn bộ Y tác dụng vừa đủ với 0,3 lít dung dịch K 2 C O 3 1M thu được dung dịch Z. Lượng KCl trong Z nhiều gấp 5 lần lượng KCl trong X. Thành phần phần trăm khối lượng KCl trong X là
A. 25,62%
B. 12,67%
C. 18,10%
D. 29,77%
Chọn đáp án C
n O 2 = 0,6 mol; n K 2 C O 3 = 0,3 mol => n C a C l 2 = n K 2 C O 3 = 0,3 mol
Bảo toàn khối lượng: m Y = 82,3 – 0,6.32 = 63,1 (gam).
=> m K C l Y = 63,1 – 0,3.111 = 29,8 (gam) => n K C l Y = 0,4 mol
=> n K C l Z = n K C l Y + 2 n K 2 C O 3 = 0,4 + 2.0,3 = 1 (mol)
=> n K C l X = 1 5 .1= 0,2 (mol)
=> % m K C l = 0 , 2 . 74 , 5 82 , 3 .100% = 18,10%
Đúng 0
Bình luận (0)




















