Bài 6: Cho H2 khử 20 gam hỗn hợp Fe2O3 và CuO trong đó CuO chiếm 40% khối lượng.
a) Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng?
b) Tính thể tích khí Hiđro (đktc) cần dùng?
B5: Cho 16 (g) Fe2O3 bị khử bởi khí H2. Sau phản ứng thu được là Fe và H2O. Tính khối lượng Fe, khối lượng H2O. Biết H=80%.
B 6: Dùng khí CO để khử CuO ở to cao . Sau phản ứng thu được 19,2 (g) Cu . Tính khối lượng CuO. Tính V CO đã dùng ở đktc Biết H = 85%.
B7: Dùng khí CO để khử ZnO ở to cao . Sau phản ứng thu được 26 (g) Zn. Tính khối lượng ZnO. V CO ở đktc Biết H = 75%.
giúp em câu này với ạ,em đang cần gấp.em cảm ơn.
Khí hidro khử 56 gam hỗn hợp gồm CuO và fe2o3 trong hỗn hợp khối lượng fe2o3 nhiều hơn khối lượng CuO là 8 g
A/ tính khối lượng fe và cu thu được
B/tính thể tích khí hiđro sinh ra
Có một hỗn hợp gồm 60% F e 2 O 3 và 40% CuO. Người ta dùng H 2 ( dư) để khử 20g hỗn hợp đó. Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng.
Khử 24g hỗn hợp 2 oxit CuO và Fe2O3 bằng khí H2 theo sơ đồ sau: CuO + H𝟸 ---> Cu + H𝟸O; Fe𝟸O𝟹 + H𝟸 ---> Fe + H𝟸O Tính thể tích H𝟸(đktc) cần dùng, biết rằng trong hỗn hợp Fe𝟸O𝟹 chiếm 75% khối lượng
\(n_{Fe_2O_3}=24.75\%=18g\)
\(n_{Fe_2O_3}=\dfrac{18}{160}=0,1125mol\)
\(n_{CuO}=\dfrac{24-18}{80}=0,075mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,1125 0,3375 ( mol )
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,075 0,075 ( mol )
\(V_{H_2}=\left(0,3375+0,075\right).22,4=9,24l\)
giúp em câu này với ạ,em đang cần gấp.em cảm ơn.
câu 4: có một hỗn hợp gồm 75% Fe2O3 và 25% CuO. Người ta dùng hiđro dư để khử 32g hỗn hợp đó
a) tính khối lượng Fe và Cu thu được sau phản ứng
b) tính thể tích khí H2 (đktc) đã tham gia phản ứng
c) tính khối lượng nhôm và axit clohiđric cần dùng để điều chế được thể tích khí hiđro nói trên
a, mFe2O3 = 32 . 75% = 24 (g)
nFe2O3 = 24/160 = 0,15 (mol)
mCuO = 32 - 24 = 8 (g)
nCuO = 8/80 = 0,1 (mol)
PTHH:
Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
0,15 ---> 0,45 ---> 0,3
CuO + H2 -> (t°) Cu + H2O
0,1 ---> 0,1 ---> 0,1
mFe = 0,3 . 56 = 16,8 (g)
mCu = 64 . 0,1 = 6,4 (g)
b, nH2 = 0,1 + 0,45 = 0,55 (mol)
VH2 = 0,55 . 22,4 = 12,32 (l)
c, PTHH:
2Al + 6HCl -> 2AlCl3 + 3H2
11/30 <--- 1,1 <--- 11/30 <--- 0,55
mAl = 11/30 . 27 = 9,9 (g)
mHCl = 1,1 . 36,5 = 40,15 (g)
Khử hoàn toàn 80 gam hỗn hợp X(gồm CuO và Fe2O3 )bằng khí H2 a. Tính khối lượng mỗi chất trong X biết số mol CuO bằng ½ số mol Fe2O3. a. Tính thể tích H2 cần dùng (đktc) b. Tính khối lượng chất rắn tạo thành sau phản ứng?
\(n_{CuO}=2a\left(mol\right)\Rightarrow n_{Fe_2O_3}=a\left(mol\right)\)
\(m_X=80\cdot2a+160a=80\left(g\right)\)
\(\Rightarrow a=0.25\left(mol\right)\)
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(n_{H_2}=0.5+0.25\cdot3=1.25\left(mol\right)\)
\(V_{H_2}=1.25\cdot22.4=28\left(l\right)\)
\(m_{cr}=0.5\cdot64+0.5\cdot56=60\left(g\right)\)
|
|
Câu 6. Cho 32g hỗn hợp A gồm Fe2O3 và CuO (trong đó %m CuO chiếm 40%) phản ứng hoàn toàn với hiđro ở nhiệt độ cao thu được hỗn hợp 2 kim loại.
a. Viết PTHH và tính thể tích khí hiđro đã phản ứng?
b.Tính khối lượng mỗi kim loại thu được .
c. Dùng lượng kim loại trên cho phản ứng hoàn toàn với dung dịch chứa 18,25g HCl, tính thể tích khí sinh ra sau phản ứng?
*ét ô ét❤
a)
\(m_{CuO}=\dfrac{32.40}{100}=12,8\left(g\right)\) => \(n_{CuO}=\dfrac{12,8}{80}=0,16\left(mol\right)\)
\(n_{Fe_2O_3}=\dfrac{32-12,8}{160}=0,12\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,16->0,16---->0,16
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,12-->0,36----->0,24
=> \(V_{H_2}=\left(0,16+0,36\right).22,4=11,648\left(l\right)\)
b)
mCu = 0,16.64 =10,24 (g)
mFe = 0,24.56 = 13,44 (g)
c)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
Xét tỉ lệ: \(\dfrac{0,24}{1}< \dfrac{0,5}{2}\) => HCl dư, Fe hết
PTHH: Fe + 2HCl --> FeCl2 + H2
0,24------------------->0,24
=> \(V_{H_2}=0,24.22,4=5,376\left(l\right)\)
Khử hoàn toàn a gam hỗn hợp Fe2O3 và CuO phải dùng 8,96 lit khí H2 (đktc) . Biết tỉ lệ m CuO : m Fe2O3 = 1: 2
a) Tính a
b) Tính khối lượng Fe và Cu thu được
\(a)Gọi : n_{CuO} = x(mol) \Rightarrow n_{Fe_2O_3} = \dfrac{80a.2}{160}=x(mol)\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + H_2O\\ n_{H_2} = x + x = \dfrac{8,96}{22,4} = 0,4(mol)\Rightarrow x = 0,2\\ a = 0,2.80 + 0,2.160 = 48(gam)\\ b)\\ n_{Fe} = 2n_{Fe_2O_3} = 0,4(mol) \Rightarrow m_{Fe} = 0,4.56 = 22,4(gam)\\ n_{Cu} = n_{CuO} = 0,2(mol) \Rightarrow m_{Cu} = 0,2.64 = 12,8(gam)\)
Cho H 2 khử 16g hỗm hợp FeO và CuO trong đó CuO chiếm 25% khối lượng. Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng.
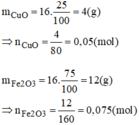
PTHH của phản ứng là:
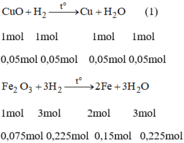
Từ pt (1), ta có: n C u = n C u O = 0,05 mol
m C u = 0,05.64 = 3,2(g)
Từ pt (2), ta có n F e = 2 . n F e 2 O 3 = 2. 0,075 = 0,15 mol
m F e = 0,15.56 = 8,4(g)