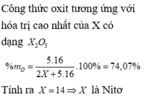X là oxit của một kim loại hóa chiếm 40% về khối lượng. Công trị II. Trong X, nguyên tố oxi thức hóa học của X là gì ?

Những câu hỏi liên quan
Phân tử X gồm nguyên tố kim loại hóa trị II liên kết với oxi. Biết trong X chứa 20% oxi về khối lượng. Công thức hóa học của X là:(Cho Mg = 24; Zn =65; Cu = 64; Fe = 56; O = 16)
A.feO
b.MgO
C.ZnO
d.CuO
\(CTTQ:AO\\ \%m_O=20\%\\ \Leftrightarrow\dfrac{16}{M_A+16}.100\%=20\%\\ \Leftrightarrow M_A=64\left(\dfrac{g}{mol}\right)\Rightarrow A:Đồng\left(Cu=64\right)\\ \Rightarrow X:CuO\\ \Rightarrow D\)
Đúng 2
Bình luận (0)
Oxit của một nguyên tố R có hóa trị II chiếm 20% oxi (về khối lượng). Tìm công thức hóa học của hợp chất oxit ?
Gọi CTHH của hợp chất là $RO$
Ta có :
$\%O = \dfrac{16}{R + 16}.100\% = 20\%$
$\Rightarrow R = 64(Cu)$
Vậy CTHH là $CuO$
Đúng 3
Bình luận (0)
Một oxit của phi kim (hóa trị VI) trong đó nguyên tố phi kim chiếm 40% theo khối lượng . a)Xác định công thức hóa học và đọc tên oxit nói trên. b)Cho 8g oxit trên tác dụng với 152g nước thu được dung dịnh chứa axit tương ứng.tính % theo khối lượng của axit trong dung dịch thu được.Các bạn giúp mh với
Đọc tiếp
Một oxit của phi kim (hóa trị VI) trong đó nguyên tố phi kim chiếm 40% theo khối lượng . a)Xác định công thức hóa học và đọc tên oxit nói trên. b)Cho 8g oxit trên tác dụng với 152g nước thu được dung dịnh chứa axit tương ứng.tính % theo khối lượng của axit trong dung dịch thu được.
Các bạn giúp mh với
a) Gọi công thức hóa học của oxit : RO3
\(\%R=\dfrac{R}{R+16.3}.100\%=40\%\Rightarrow R=32\)
\(\Rightarrow CTHH:SO_3\left(lưu.huỳnh.trioxit\right)\)
b) \(n_{SO3}=\dfrac{8}{80}=0,1\left(mol\right)\)
Pt : \(SO_3+H_2O\rightarrow H_2SO_4\)
Theo Pt : \(n_{H2SO4}=n_{SO3}=0,1\left(mol\right)\)
\(\Rightarrow m_{H2SO4}=0,1.98=9,8\left(g\right)\)
\(m_{ddspu}=8+152=160\left(g\right)\)
\(C\%_{ddH2SO4}=\dfrac{9,8.}{160}.100\%=6,125\%\)
Chúc bạn học tốt
Đúng 3
Bình luận (0)
Oxit của một nguyên tố có hóa trị II chứa 20% oxi về khối lượng. Công thức hóa học của oxit trên là
A.
CuO.
B.
CaO
C.
MgO
D.
FeO
Gọi CTHH là $R_2O_n$
Ta có : $\%O = \dfrac{16n}{2R + 16n}.100\% =2 0\%$
$\Rightarrow R = 32n$
Với n = 2 thì R = 64(Cu)
Vậy Chọn đáp án A
Đúng 1
Bình luận (0)
1.Tỷ lệ khối lượng của nitơ và oxi trong một oxit là 7 : 20. Công thức của oxit là? (Đáp án là N2O5)
2.Một loại sắt oxit có tỉ lệ khối lượng mFe : mO = 7 : 2. Công thức hóa học của oxit là
3.Cho oxit của nguyên tố R hóa trị IV, trong đó R chiếm 46,7% theo khối lượng. Công thức của oxit đó là
(Nhờ các bạn, thầy, cô hướng dẫn)
1. Gọi CTHH của oxit là NxOy.
Ta có: \(\dfrac{m_N}{m_O}=\dfrac{7}{20}\Rightarrow\dfrac{n_N}{n_O}=\dfrac{7}{20}:\dfrac{14}{16}=\dfrac{2}{5}\)
⇒ x:y = 2:5
→ N2O5
2. Gọi CTHH cần tìm là FexOy.
\(\Rightarrow\dfrac{m_{Fe}}{m_O}=\dfrac{7}{2}\Rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{7}{2}:\dfrac{56}{16}=1\)
⇒ x:y = 1
→ FeO
3. CTHH cần tìm: RO2
Mà: %R = 46,7%
\(\Rightarrow\dfrac{M_R}{M_R+16.2}.100\%=46,7\%\)
⇒ MR = 28 (g/mol)
→ SiO2
Đúng 1
Bình luận (0)
Oxit của một nguyên tố có hóa trị (II) chứa 20% oxi ( về khối lượng). Công thức hóa học của oxit đó là:
A.CuO. B. FeO. C.CaO. D.ZnO
Tìm công thức đúng.
Công thức hóa học của oxit cần tìm là MO.
Khối lượng mol của MO = M + 16
Và trong 100g MO có 20g oxi.
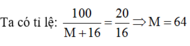
Vậy M là kim loại Cu, công thức hóa học của oxit là CuO.
Đúng 0
Bình luận (0)
Một oxit của kim loại M có hóa trị II trong đó M chiếm 60% về khối lượng. Xác định công thức hóa học của oxit trên
Tham khảo:
Gọi CTHH của hợp chất là MxOy
Ta có: %M = 100% - 20% = 80%
Ta có: x : y = %M / MM : %O / 16 = 80% / MM : 20% / 16 = 80 / MM : 20 / 16
=> MM = ( 16 x 80 ) : 20 = 64 g
Ta có:
x : y = %Cu / 64 : %O / 16 = 80% / 64 : 20% / 16 = 80 / 64 : 20 / 16 = 1,25 : 1,25 = 1 : 1
=> x = 1, y = 1
=> CTHH: CuO
Đúng 1
Bình luận (0)
\(Đặt:MO\\ \%m_{\dfrac{M}{MO}}=60\%\\ \Leftrightarrow\dfrac{M_M}{M_M+16}.100\%=60\%\\ \Leftrightarrow M_M=24\left(\dfrac{g}{mol}\right)\\ \Rightarrow M:Magie\left(Mg=24\right)\\ CTHH.oxit:MgO\)
Đúng 3
Bình luận (0)
một hợp chất của nguyên tố X hóa trị III với nguyên tố oxi trong đó X chiếm 52,94% về khối lượng . Xác định công thức hóa học và tính phân tử khối của hợp chất
Hợp chất với hiđro của nguyên tố X có công thức hóa học X H 3 . Biết thành phần phần trăm về khối lượng của oxi trong oxit ứng với hóa trị cao nhất của X là 74,07%. Tên gọi của X là
A. nitơ
B. asen
C. lưu huỳnh
D. photpho