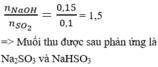Cho 5,6 lit khí SO2 (ở đktc) vào 300 ml dung dịch NaOH 1M sau phản ứng thu được m (g) muối. Tìm m= ?

Những câu hỏi liên quan
Cho 5,6 lit khí SO2 (ở đktc) vào 300 ml dung dịch KOH 1M sau phản ứng thu được m (g) muối. Tìm m= ?
\(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
nKOH = 0,3.1 = 0,3 (mol)
PTHH: 2KOH + SO2 --> K2SO3 + H2O
0,3-->0,15--->0,15
K2SO3 + SO2 + H2O --> 2KHSO3
0,1<--0,1----------------->0,2
=> hh muối gồm \(\left\{{}\begin{matrix}K_2SO_3:0,05\left(mol\right)\\KHSO_3:0,2\left(mol\right)\end{matrix}\right.\)
=> m = 0,05.158 + 0,2.120 = 31,9 (g)
Đúng 2
Bình luận (0)
Cho 5,6 lit khí SO2 (ở đktc) vào 300 ml dung dịch NaOH 1M sau phản ứng thu được dung
dịch A. Tổng khối lượng muối thu được trong dung dịch A là?
Cho 5,6 lit khí SO2 (ở đktc) vào 300 ml dung dịch NaOH 1M sau phản ứng thu được dung dịch A. Tổng khối lượng muối thu được trong dung dịch A là
A. 27,1 gam.
B. 46,4 gam.
C. 21,7 gam.
D. 44,6 gam.
Ta có:
\(n_{SO2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
\(n_{NaOH}=1.0,3=0,3\left(mol\right)\)
\(\frac{n_{NaOH}}{n_{SO2}}=\frac{0,3}{0,25}=1,2\)
Phản ứng tạo 2 muối
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
a_______2a _______ a_______
\(SO_2+NaOH\rightarrow NaHSO_3\)
b_______b__________b
Giải hệ PT:
\(\left\{{}\begin{matrix}a+b=0,25\\2a+b=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Na2SO3}=0,05.126=6,3\left(g\right)\)
\(\Rightarrow m_{NaHSO3}=0,2.104=20,8\left(g\right)\)
\(\Rightarrow\Sigma m=20,8+6,3=27,1\left(g\right)\)
Đáp án đúng : A
Đúng 0
Bình luận (0)
1. Cho 2240 ml khí H2S (ở đktc) hấp thụ hết vào 200 ml dung dịch NaOH 1M. Sau phản ứng thu được ?
2. Cho 2240 ml khí SO2 (ở đktc) hấp thụ hết vào 200 ml dung dịch NaOH 1M. Sau phản ứng thu được ?
1) \(n_{H_2S}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
Xét \(\dfrac{n_{NaOH}}{n_{H_2S}}=\dfrac{0,2}{0,1}=2\) => Tạo muối Na2S
PTHH: 2NaOH + H2S --> Na2S + 2H2O
0,2------------>0,1
=> mNa2S = 0,1.78 = 7,8 (g)
2)
\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{NaOH}=0,2.1=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{n_{NaOH}}{n_{SO_2}}=\dfrac{0,2}{0,1}=2\) => Tạo muối Na2SO3
PTHH: 2NaOH + SO2 --> Na2SO3 + H2O
0,2-------------->0,1
=> mNa2SO3 = 0,1.126 = 12,6 (g)
Đúng 1
Bình luận (0)
2. \(\left\{{}\begin{matrix}n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\n_{NaOH}=0,2.1=0,2\left(mol\right)\end{matrix}\right.\)
Ta có: \(T=\dfrac{0,2}{0,1}=2\) ⇒ tạo ra muối Na2SO3
SO2 + 2NaOH -----> Na2SO3 + H2O
Đúng 0
Bình luận (0)
Cho hỗn hợp X gồm 2 chất hữu cơ đơn chức phản ứng vừa đủ với 300 ml dung dịch NaOH 1M. Sau phản ứng thu được 1 muối của axit hữu cơ và 1 rượu . Cho toàn bộ lượng rượu thu được ở trên tác dụng với Na dư, sinh ra 5,6 lit khí H2 (dktc). Hỗn hợp X là : A. 1 axit và 1 este B. Đáp án khác C. 1 axit và 1 rượu D. 1 este và 1 rượu
Đọc tiếp
Cho hỗn hợp X gồm 2 chất hữu cơ đơn chức phản ứng vừa đủ với 300 ml dung dịch NaOH 1M. Sau phản ứng thu được 1 muối của axit hữu cơ và 1 rượu . Cho toàn bộ lượng rượu thu được ở trên tác dụng với Na dư, sinh ra 5,6 lit khí H2 (dktc). Hỗn hợp X là :
A. 1 axit và 1 este
B. Đáp án khác
C. 1 axit và 1 rượu
D. 1 este và 1 rượu
Đáp án : B
nancol = 2nH2 = 0,5 mol > nNaOH = 0,3 mol => X phải có 1 ancol và chất còn lại có thể là este hoặc axit
Đúng 0
Bình luận (0)
Cho m gam K tan hết vào 100 ml dung dịch gồm (
H
2
S
O
4
1M và HCl 2M) thu được 5,6 lít khí
H
2
(ở đktc). Cô cạn dung dịch sau phản ứng khối lượng chất rắn thu được là A. 32,3 B. 37,9 gam C. 24,95 gam D. 30,1gam
Đọc tiếp
Cho m gam K tan hết vào 100 ml dung dịch gồm ( H 2 S O 4 1M và HCl 2M) thu được 5,6 lít khí H 2 (ở đktc). Cô cạn dung dịch sau phản ứng khối lượng chất rắn thu được là
A. 32,3
B. 37,9 gam
C. 24,95 gam
D. 30,1gam
Sục 2,24 lít khí
S
O
2
(đktc) vào 500 ml dung dịch NaOH 0,3M. Muối thu được sau phản ứng là A.
N
a
2
S
O
3
B.
N
a
H
S
O
3
C.
N
a
2
S
O
3
v
à
N...
Đọc tiếp
Sục 2,24 lít khí S O 2 (đktc) vào 500 ml dung dịch NaOH 0,3M. Muối thu được sau phản ứng là
A. N a 2 S O 3
B. N a H S O 3
C. N a 2 S O 3 v à N a H S O 3
D. N a H S O 3 v à N a O H
Hấp thụ hoàn toàn V lit khí CO2 (ở đktc) vào 500 ml dung dịch NaOH 1M, sau phản ứng thu được dung dịch X có chứa 25,2 gam chất tan. Giá trị V là
A. 4,48
B. 6,72
C. 8,96
D. 3,36
Đáp án : A
+) TH1 : NaOH hết
Giả sử sau phản ứng có x mol Na2CO3 ; y mol NaHCO3
=> 106x + 84y = 25,2g ; 2x + y = nNaOH = 0,5 mol
=> Loại
+) TH2 : NaOH dư => x mol Na2CO3 ; NaOH : y mol
=> 106x + 40y = 25,2g ; 2x + y = 0,5 mol
=> x = 0,2 ; y = 0,1 mol
=> nCO2 = nNa2CO3 = 0,2 mol
=>V = 4,48 lit
Đúng 0
Bình luận (0)
Câu 4: Cho m gam Fe vào 500 ml dung dịch HCl, phản ứng xảy ra vừa đủ thu được 3,36 lit khí H2 (Đktc). Tính m g Fe? Và CM của HCl
Câu 5: cho 8,3 gam hỗn hợp kim loại Fe, Al tác dụng với 500ml dung dịch HCl vừa đủ thu được 5,6 lit khí Hidro (Đktc). Xác định thành phần % mỗi kim loại trong hỗn hợp ban đầu
\(4.\)
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.15.....0.3....................0.15\)
\(m_{Fe}=0.15\cdot56=8.4\left(g\right)\)
\(C_{M_{HCl}}=\dfrac{0.3}{0.5}=0.6\left(M\right)\)
\(5.\)
\(Đặt:n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m_{hh}=56a+27b=8.3\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow a+1.5b=0.25\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%Fe=\dfrac{5.6}{8.3}\cdot100\%=67.47\%\)
\(\%Al=32.53\%\)
Đúng 2
Bình luận (1)