Tính thể tích không khí cần thiết để đốt cháy hoàn toàn 5,6 lít khí metan, biết rằng các thể tích khí đều đo ở đktc và khí oxi chiếm \(\dfrac{1}{5}\) thể tích không khí.

Những câu hỏi liên quan
Đốt cháy hoàn toàn 5,6 lít etilen.Hãy tính thể tích oxi và thể tích không khí cần đung cho phản ứng,biết rằng oxi chiếm 20% thể tích không khí.Tính thể tích khí đó ở đktc
\(n_{C_2H_4}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PT: \(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
Theo PT: \(n_{O_2}=3n_{C_2H_4}=0,75\left(mol\right)\Rightarrow V_{O_2}=0,75.22,4=16,8\left(l\right)\)
\(\Rightarrow V_{kk}=\dfrac{V_{O_2}}{20\%}=84\left(l\right)\)
Đúng 2
Bình luận (0)
: Khí metan(CH4) được dung làm nhiên liệu, khi đốt cháy trong không khí tỏa nhiều nhiệt. Tính thể tích O2 và thể tích không khí cần để đốt cháy hoàn toàn 4,48 lít khí CH4. Biết rằng thể tích các khí đo ở đktc
CH4 + 2O2 ---to--> CO2 + 2H2O
nCH4 = 4,48 : 22,4 = 0,2 (mol)
--> VO2 = 0,2 x 2 x 22,4 = 8,96 (l)
--> Vkk = 8,96 x 5 = 44,8 (l)
nhá
Tính thể tích khí Oxi cần thiết để đốt cháy hoàn toàn khí metan CH4 có trong 1m3 khí chứa 2% tạp chất không cháy. Các thể tích đo ở đktc
1 m3 = 1000 lít
$V_{CH_4} = 1000.(100\% - 2\%) = 980(lít)$
$CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O$
Theo PTHH :
$V_{O_2} =2 V_{CH_4} = 1960(lít)$
Đúng 2
Bình luận (1)
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là: A. 70,0 lít B. 78,4 lít C. 84,0 lít D. 56,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là:
A. 70,0 lít
B. 78,4 lít
C. 84,0 lít
D. 56,0 lít
Đáp án A
Hỗn hợp khí gồm CH4, C2H6 và C3H8 là các hidrocacbon.
Mà khi đốt cháy 1 hidrocacbon bất kì ta luôn có:
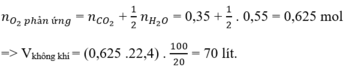
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là : A. 78,4 lít B. 56,0 lít C. 70,0 lít D. 84,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiên gồm metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là :
A. 78,4 lít
B. 56,0 lít
C. 70,0 lít
D. 84,0 lít
Đốt cháy hoàn toàn một thể tích khí thiên nhiêm gồm: metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là A. 84,0 lít B. 70,0 lít C. 78,4 lít D. 56,0 lít
Đọc tiếp
Đốt cháy hoàn toàn một thể tích khí thiên nhiêm gồm: metan, etan, propan bằng oxi không khí (trong không khí, oxi chiếm 20% thể tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thể tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn toàn lượng khí thiên nhiên trên là
A. 84,0 lít
B. 70,0 lít
C. 78,4 lít
D. 56,0 lít
Tính thể tích khí oxi cần thiết để đốt cháy hoàn toàn khí metan CH4 có trong 1 m3 khí chứa 2% tạp chất không cháy. Các thể tích đó được đo ở đktc.
VCH4(nguyênchất)=1000.98%=980(l)
⇒nCH4=\(\dfrac{980}{22,4}\)=43,75(mol)
CH4+2O2-to→CO2+2H2O
⇒nO2=87,5(mol)
⇒VO2=87,5.22,4=1960(l)=1,96(m3)
Đúng 3
Bình luận (0)
tính thể tích khí oxi cần thiết để đốt cháy hoàn toàn khí metan CH4 có 1m3 khí chứa
2% tạp chất không cháy .Các thể tích đó được đo ở đktc
\(V_{CH_4(nguyên chất)}=1000.98\%=980(l)\\ \Rightarrow n_{CH_4}=\dfrac{980}{22,4}=43,75(mol)\\ CH_4+2O_2\xrightarrow{t^o}CO_2+2H_2O\\ \Rightarrow n_{O_2}=87,5(mol)\\ \Rightarrow V_{O_2}=87,5.22,4=1960(l)=1,96(m^3)\)
Đúng 2
Bình luận (0)
Đốt cháy hoàn toàn một thể tích khí metan cần dùng 336 ml không khí (a) Tính thể tích khí metan đã cháy (b) Tính thể tích khí CO2 tạo thành. Biết oxi chiếm 1/5 thể tích không khí. Các khí đo ở cùng điều kiện nhiệt độ và áp suất
\(V_{O_2}=\dfrac{336}{5}=67,2\left(ml\right)=0,0672\left(l\right)\\ n_{O_2}=\dfrac{0,0672}{22,4}=0,003\left(mol\right)\\ CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\\ n_{CO_2}=n_{CH_4}=\dfrac{0,003}{2}=0,0015\left(mol\right)\\ a,V_{CH_4\left(đktc\right)}=0,0015.22,4=0,0336\left(l\right)\\ b,V_{CO_2\left(đktc\right)}=V_{CH_4\left(đktc\right)}=0,0336\left(l\right)\)
Đúng 1
Bình luận (0)



















