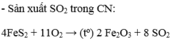Viết phương trình điều chế: a. H2S b. SO2

Những câu hỏi liên quan
II-Tự luận
Viết phương trình hóa học điều chế H 2 S trong phòng thí nghiệm và sản xuất S O 2 trong công nghiệp?
Viết 5 phương trình hóa học trực tiếp điều chế ra các chất O2. H2S. SO2 .H2 .SO4.
\(2KClO_3\underrightarrow{^{to}}2KCl+3O_2\)
\(S+H_2⇌H_2S\)
\(S+O_2\underrightarrow{^{to}}SO_2\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
Một phương pháp được đề xuất để loại bỏ SO2 khỏi khí thải của nhà máy điện bằng cách dẫn khí thải qua dung dịch H2S.(a) Viết phương trình phản ứng giữa SO2 và H2S.(b) Cần bao nhiêu lít H2S (ở đkc) để loại bỏ SO2 sinh ra khi đốt cháy 2,0 tấn than chứa sulfur chiếm 3,5% theo khối lượng? Biết các phản ứng xảy ra hoàn toàn. các bạn giúp tớ giải bài này với, mình đang cần ạ!
Đọc tiếp
Một phương pháp được đề xuất để loại bỏ SO2 khỏi khí thải của nhà máy điện bằng cách dẫn khí thải qua dung dịch H2S.
(a) Viết phương trình phản ứng giữa SO2 và H2S.
(b) Cần bao nhiêu lít H2S (ở đkc) để loại bỏ SO2 sinh ra khi đốt cháy 2,0 tấn than chứa sulfur chiếm 3,5% theo khối lượng? Biết các phản ứng xảy ra hoàn toàn.
các bạn giúp tớ giải bài này với, mình đang cần ạ!
a) Phương trình phản ứng giữa SO2 và H2S là:
SO2 + H2S -> 2H2O + 3S b) Để tính số lít H2S cần thiết, ta cần biết số mol SO2 sinh ra từ việc đốt cháy 2,0 tấn than chứa sulfur. - Khối lượng sulfur trong 2,0 tấn than = 2,0 tấn x 3,5% = 70 kg.- Số mol sulfur = khối lượng sulfur / khối lượng mol sulfur = 70 kg / 32,06 g/mol = 2180,5 mol.- Vì phản ứng xảy ra hoàn toàn, số mol H2S cần thiết cũng là 2180,5 mol.- Theo phương trình phản ứng, ta thấy tỉ lệ mol giữa SO2 và H2S là 1:1.- Vậy, số lít H2S cần thiết là 2180,5 lít.
Đúng 1
Bình luận (0)
Câu 2: a.Từ quặng pirit, NaCl và nước, viết các phương trình phản ứng điều chế: SO2 Fe(OH)3, Na2SO3, Fe, Fe(OH)2.
b.Từ những chất sau: Cu, C, S, Na2SO3, FeS2, O2, H2SO4, viết tất cả các phương trình phản ứng có thể dùng để điều chế SO2. Ghi rõ điều kiện phản ứng nếu có
Viết các phương trình phản ứng chỉ ra: 2 cách điều chế HCl, H2S, H3PO4, HNO3, H2SO4
| HCl | H2S | H3PO4 | HNO3 | H2SO4 | |
| AgNO3 | kt trắng | kt đen | kt vàng | - | kt trắng |
| BaCl2 | - | - | kt trắng | ||
HCl + AgNO3 -> HNO3 + AgCl
H2S + AgNO3 -> HNO3 + Ag2S
H3PO4 + AgNO3 -> HNO3 + Ag3PO4
H2SO4 + AgNO3 -> HNO3 + Ag2SO4
BaCl2 + H2SO4 -> BaSO4 + HCl
Đúng 2
Bình luận (0)
Viết phương trình hóa học của các phản ứng biểu diễn các chuyển đổi sau: a. KClO3 -> O2-> SO2-> Na2SO3 b. S-> H2S -> SO2 -> SO3 ->H2SO4
\(a,\left(1\right)2KClO_3\rightarrow\left(^{t^o}_{MnO_2}\right)2KCl+3O_2\\ \left(2\right)S+O_2\rightarrow^{t^o}SO_2\\ \left(3\right)SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\\ b,\left(1\right)S+H_2\rightarrow^{t^o}H_2S\\ \left(2\right)2H_2S+3O_2\rightarrow^{t^o}2H_2O+2SO_2\\ \left(3\right)2SO_2+O_2\rightarrow^{\left(t^o,V_2O_5\right)}2SO_3\\ \left(4\right)SO_3+H_2O\rightarrow H_2SO_4\)
Đúng 1
Bình luận (0)
Có thể điều chế lưu huỳnh từ khí SO 2 và H 2 S . Viết PTHH của phản ứng.
Viết phương trình hoá học khi cho kim loại A hoá trị n tác dụng với các chất sau đây: Khí oxi; Nước; Axit clohidric (điều chế H2); Axit sunfuric (điều chế H2); Axit sunfuric (điều chế SO2).
A + O2 \(\underrightarrow{t^o}\) A2On (Trường hợp này ko dành cho Fe3O4 nhé)
A + nH2O \(\rightarrow\) A(OH)n + \(\dfrac{1}{2}n\)H2 (Cái này có khi và chỉ khi A là kim loại kiềm hoặc kiềm thổ)
2A + 2nHCl \(\rightarrow\) 2ACln + nH2 (Trường hợp này ko dành cho Fe3O4 nhé)
2A + nH2SO4 \(\rightarrow\) A2(SO4)n + nH2 (Trường hợp này ko dành cho Fe3O4 nhé)
2A + 2nH2SO4 (đ) \(\underrightarrow{t^o}\) A2(SO4)n + nSO2 + 2nH2O
Đúng 1
Bình luận (1)
bạn có cần giải thích rõ hơn vì sao các pt này ko dành cho Fe3O4 không?
Đúng 1
Bình luận (1)
9. Trong công nghiệp điều chế H2SO4 từ FeS2 theo sơ đồ sau: FeS2 SO2 SO3 H2SO4 a) Viết phương trình phản ứng và ghi rõ điều kiện. b) Tính lượng axit H2SO4 điều chế được từ 1 tấn quặng chứa 60% FeS2. Biết H% của quá trình là 80%.
a)
$4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
$2SO_2 + O_2 \xrightarrow{t^o,xt} 2SO_3$
$SO_3 + H_2O \to H_2SO_4$
b)
$m_{FeS_2} = 1000.60\% = 600(kg)$
$n_{FeS_2} = \dfrac{600}{120} = 5(kmol)$
$n_{FeS_2\ pư} = 5.80\% = 4(kmol)$
$n_{H_2SO_4} = 2n_{FeS_2} = 8(kmol)$
$m_{H_2SO_4} = 8.98 = 784(kg)$
Đúng 1
Bình luận (0)
4FeS2+11O2to→2Fe2O3+8SO2
4FeS2+11O2→to2Fe2O3+8SO2
2SO2+O2to,xt−−→2SO3
2SO2+O2→to,xt2SO3
SO3+H2O→H2SO4
SO3+H2O→H2SO4
b)
mFeS2=1000.60%=600(kg)
mFeS2=1000.60%=600(kg)
nFeS2=600120=5(kmol)
nFeS2 pư=5.80%=4(kmol)
nFeS2 pư=5.80%=4(kmol)
nH2SO4=2nFeS2=8(kmol)
nH2SO4=2nFeS2=8(kmol)
mH2SO4=8.98=784(kg)
Đúng 0
Bình luận (0)