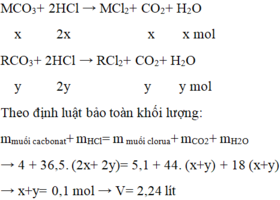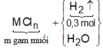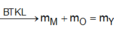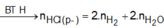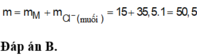Hòa tan hoàn toàn m(g) hỗn hợp Al, Fe vào trong dung dịch HCl loãng dư thấy có 1,456 lít khí thoát ra (ở đktc) và dung dịch X. Cô cạn dung dịch X thu được 6,545 gam muối khan. Tính giá trị của m?

Những câu hỏi liên quan
Hòa tan hoàn toàn 33,1 gam hỗn hợp X gồm Mg, Fe, Zn vào dung dịch H2SO4 loãng dư thấy có 13,44 lít khí thoát ra (đktc) và dung dịch Y. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là A. 78,7. B. 75,5. C. 74,6. D. 90,7
Đọc tiếp
Hòa tan hoàn toàn 33,1 gam hỗn hợp X gồm Mg, Fe, Zn vào dung dịch H2SO4 loãng dư thấy có 13,44 lít khí thoát ra (đktc) và dung dịch Y. Cô cạn dung dịch Y thu được m gam muối khan. Giá trị của m là
A. 78,7.
B. 75,5.
C. 74,6.
D. 90,7
Đáp án D
Khí thu được là H2 : n H 2 = 13 , 44 22 , 4 = 0 , 6 mol
Gọi M là kim loại chung cho Mg, Fe và Zn với hóa trị n
Sơ đồ phản ứng :
![]()
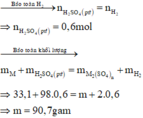
Đúng 0
Bình luận (0)
hoàn tan hoàn toàn 25,7 g hỗn hợp Mg,Fe,Zn vào trong dung dịch H2SO4 loãng dư thấy có 13,44 lít khí thoát ra (ở đktc) và dung dịch X . cô cận dung dịch X thu đc m gam muối khan . giá trị của m
Gọi công thức chung của Mg, Fe, Zn là A
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: A + H2SO4 --> ASO4 + H2
=> nH2SO4 = nH2 = 0,6 (mol)
Theo ĐLBTKL: mA + mH2SO4 = mASO4 + mH2
=> mASO4 = 25,7 + 0,6.98 - 0,6.2 = 83,3 (g)
Đúng 3
Bình luận (0)
Hoà tan hoàn toàn 8,48 gam hỗn hợp Mg và Fe trong dung dịch HCl dư thấy có 4,928 lít khí thoát ra (ở đktc) và dung dịch X. Cô cạn dung dịch X được bao nhiêu gam muối khan?A. 12,05 gam
A. 12,05 gam
B. 26,35 gam
C. 24,1 gam
D. 30,3 gam
Hòa tan hoàn toàn 4 gam hỗn hợp MCO3 và RCO3 bằng dung dịch HCl dư thấy thoát ra V lít khí (đktc). Dung dịch thu được đem cô cạn được 5,1 gam muối khan. Giá trị của V là:
A. 1,12 lít
B. 1,68 lít
C. 2,24 lít
D. 3,36 lít
Hỗn hợp X gồm Al, Fe và Mg. Cho 15 gam X tác dụng với oxi, sau một thời gian thu được 18,2 gam chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 ở đktc và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan. Giá trị của m là: A.38,5. B. 50,5. C. 53,7. D. 46,6.
Đọc tiếp
Hỗn hợp X gồm Al, Fe và Mg. Cho 15 gam X tác dụng với oxi, sau một thời gian thu được 18,2 gam chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 ở đktc và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan. Giá trị của m là:
A.38,5.
B. 50,5.
C. 53,7.
D. 46,6.
Hòa tan hoàn toàn 5,65 gam hỗn hợp Mg và Zn trong dung dịch HCl dư, thu được 3,36 lít (đktc) khí H2 và dung dịch X. Cô cạn dung dịch X, được m gam muối khan. Giá trị m là:
A. 16,3
B. 21,95
C. 11,8
D. 18,10
Chọn đáp án A
Mg + 2HCl → MgCl2 + H2↑ || Zn + 2HCl → ZnCl2 +H2↑.
nH2↑ = 0,15 mol ⇒ nCl− trong muối = 2nH2 = 0,3 mol.
||→ m = mmuối = mkim loại + mCl− = 5,65 + 0,3 × 35,5 = 16,3 gam. Chọn A.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 5,65 gam hỗn hợp Mg và Zn trong dung dịch HCl dư, thu được 3,36 lít (đktc) khí H2 và dung dịch X. Cô cạn dung dịch X, được m gam muối khan. Giá trị m là:
A. 16,3
B. 21,95
C. 11,8
D. 18,10
Chọn đáp án A
Mg + 2HCl → MgCl2 + H2↑ || Zn + 2HCl → ZnCl2 +H2↑.
nH2↑ = 0,15 mol ⇒ nCl- trong muối = 2nH2 = 0,3 mol.
||→ m = mmuối = mkim loại + mCl- = 5,65 + 0,3 × 35,5 = 16,3 gam. Chọn A
Đúng 0
Bình luận (0)
1,hòa tan hoàn toàn 4g hơn hợp mco3 và m'co3 vào dung dịch hcl thấy thoát ra v lít khí ở đktc. Dung dịch thu được đem khô cạn thấy có 5,1g muối khan . v có giá trị là ?
2,hòa tan 4g hơn hợp 2 muối mco3 và m'co3 bằng dung dịch hcl dư thu được dung dịch a và v lít khí b ở đktc ,cô cạn dung dịch a thu được 4,55g muối khan . giá trị của v là ?
Câu 48. Hoà tan hoàn toàn 11 gam hỗn hợp Al và Fe trong dung dịch HCl dư thấy thoát ra 8,96 lit khí H2 đktc. Cô cạn dung dịch thu được m gam muối khan. m có giá trị là :A. 2,52 B. 39,4 C. 3,94 D. 25,2Câu 49. Cho 4,15 g hỗn hợp gồm Al và Fe tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng thu được 2,8 lít khí H2 (đktc). Thành phần % theo khối lượng mỗi kim loại trong hỗn hợp lần lượt làA. 45% và 55%. B...
Đọc tiếp
Câu 48. Hoà tan hoàn toàn 11 gam hỗn hợp Al và Fe trong dung dịch HCl dư thấy thoát ra 8,96 lit khí H2 đktc. Cô cạn dung dịch thu được m gam muối khan. m có giá trị là :
A. 2,52 B. 39,4 C. 3,94 D. 25,2
Câu 49. Cho 4,15 g hỗn hợp gồm Al và Fe tác dụng với dung dịch H2SO4 loãng dư. Sau phản ứng thu được 2,8 lít khí H2 (đktc). Thành phần % theo khối lượng mỗi kim loại trong hỗn hợp lần lượt là
A. 45% và 55%. B. 67,5% và 32,5%. C. 55% và 45%. D. 32,5% và 67,5%.
Câu 50. Hòa tan hỗn hợp X gồm 11,2 gam Fe và 2,4 gam Mg bằng dung dịch H2SO4 loãng (dư), thu được dung dịch Y. Cho dung dịch NaOH dư vào Y thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được m gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
A. 36. B. 20. C. 18. D. 24.
Câu 48:
\(n_{Al}=x(mol);n_{Fe}=y(mol)\\ \Rightarrow 27x+56y=11(1)\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow 1,5x+y=\dfrac{8,96}{22,4}=0,4(2)\\ (1)(2)\Rightarrow x=0,2(mol);y=0,1(mol)\\ \Rightarrow n_{AlCl_3}=0,2(mol);n_{FeCl_2}=0,1(mol)\\ \Rightarrow m_{muối}=0,2.133,5+0,1.127=39,4(g)(B)\)
Câu 49:
\(n_{Al}=x(mol);n_{Fe}=y(mol)\\ \Rightarrow 27x+56y=4,15(1)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ Fe+H_2SO_4\to FeSO_4+H_2\\ \Rightarrow 1,5x+y=\dfrac{2,8}{22,4}=0,125(2)\\ (1)(2)\Rightarrow x=y=0,05(mol)\\ \Rightarrow \%_{Fe}=\dfrac{0,05.56}{4,15}.100\%=67,5\%\\ \Rightarrow \%_{Al}=100\%-67,5\%=32,5\%\\ \Rightarrow B\)
Đúng 1
Bình luận (0)
Câu 50:
\(Fe+H_2SO_4\to FeSO_4+H_2\\ Mg+H_2SO_4\to MgSO_4+H_2\\ FeSO_4+2NaOH\to Fe(OH)_2\downarrow+Na_2SO_4\\ MgSO_4+2NaOH\to Mg(OH)_2\downarrow+Na_2SO_4\\ 4Fe(OH)_2+O_2\xrightarrow{t^o}2Fe_2O_3+4H_2O\\ Mg(OH)_2\xrightarrow{t^o}MgO+H_2O\\ \Rightarrow n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=\dfrac{11,2}{56}=0,1(mol)\\ n_{MgO}=n_{Mg}=\dfrac{2,4}{24}=0,1(mol)\\ \Rightarrow \Sigma m_{\text{chất rắn}}=0,1.160+0,1.40=20(g)\)
Chọn B
Đúng 1
Bình luận (0)