Tính số mol và số gam potassium chlorate cần thiết để điều chế được:
a) 48gam khí Oxygen
b) 49,58 lít khí Oxygen
Để điều chế Iron(II, III) oxide, người ta đốt cháy Iron trong khí oxygen
a. Tính khối lượng Iron và thể tích khí Oxygen(điều kiện chuẩn) cần dùng để điều chế được 4,64 gam Iron(II, III) oxide
b. Cần bao nhiêu gam Potassium chlorate(KClO3) để điều chế ra lượng Oxygen cần dùng ở phản ứng trên?
3Fe+2O2-to>Fe3O4
0,06---0,04------0,02 mol
n Fe3O4=\(\dfrac{4,64}{232}\)=0,02 mol
=>m Fe=0,06.56=3,36g
=>VO2=0,04.22,4=0,896l
b)2KClO3-to>2KCl+3O2
\(\dfrac{2}{75}\)------------------0,04 mol
=>m KClO3=\(\dfrac{2}{75}\).122,5=32,67g
Tính số mol và số gam kali clorat cần thiết để điều chế được:
a) 48g khí oxi.
b) 44,8 lít khí oxi (ở đktc).
Chú ý các bạn ko chép mạng nha tại mình xem rồi mà chx hiểu nên mình mới hỏi
a) \(n_{O_2}=\dfrac{48}{32}=1,5\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
1<--------------------1,5
=> \(n_{KClO_3}=1\left(mol\right)\)
=> \(m_{KClO_3}=1.122,5=122,5\left(g\right)\)
b) \(n_{O_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\)
PTHH: 2KClO3 --to--> 2KCl + 3O2
\(\dfrac{4}{3}\)<-------------------2
=> \(n_{KClO_3}=\dfrac{4}{3}\left(mol\right)\)
=> \(m_{KClO_3}=\dfrac{4}{3}.122,5=\dfrac{490}{3}\left(g\right)\)
tính số mol và số gam kali clorat cần thiết để điều chế được :
a, 48g khí oxi b, 44,8 lít khí oxi (đktc)
$2KClO_3 \xrightarrow{t^o} 2KCl +3 O_2$
a) n O2 = 48/32 = 1,5(mol)
n KClO3 = 2/3 n O2 = 1(mol)
m KClO3 = 1.122,5 = 122,5(gam)
b) n O2 = 44,8/22,4 = 2(mol)
n KClO3 = 2/3 n O2 = 4/3 (mol)
m KClO3 = 122,5.4/3 = 163,33(gam)
\(a.\)
\(n_{O_2}=\dfrac{48}{32}=1.5\left(mol\right)\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\)
\(1...............................1.5\)
\(m_{KClO_3}=1\cdot122.5=122.5\left(g\right)\)
\(b.\)
\(n_{O_2}=\dfrac{44.8}{22.4}=2\left(mol\right)\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\)
\(\dfrac{4}{3}.................2\)
\(m_{KClO_3}=\dfrac{4}{3}\cdot122.5=163.3\left(g\right)\)
Tính số mol và số gam kali clorat cần thiết để điều chế đc
a) 48 g khí oxi
b) 44,8 lít khí oxi ở đktc
\(2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\)
a)
\(n_{O_2} = \dfrac{48}{32} = 1,5(mol)\)
Theo PTHH :
\(n_{KClO_3} = \dfrac{2}{3}n_{O_2} = 1(mol)\\ \Rightarrow m_{KClO_3} = 1.122,5 = 122,5(gam)\)
b)
\(n_{O_2} = \dfrac{44,8}{22,4} = 2(mol) \)
Theo PTHH :
\(n_{KClO_3} = \dfrac{2}{3}n_{O_2} = \dfrac{4}{3}mol\\ \Rightarrow m_{KClO_3} = \dfrac{4}{3}.122.5 = 163,33(gam)\)
a) PTHH: 2KClO3-->2KCl + 3O2 1mol <---1mol<---1,5mol nO2=48/32=1,5mol=> nKClO3=1 =>mKClO3=1.122,5=122,5 gamvậy cần 122,5 gam KClO3 để điều chế 48 gam khí oxi
b)PTHH: 2KClO3-->2KCl + 3O2 4/3mol <---4/3mol<---2mol nO2=44,8/22,4=2mol=> nKClO3=4/3mol =>mKClO3=4/3.122,5=163,33333gamVậy cần 163,33333gam KClO3 để điều chế 44,8 lít khí oxi ở đktc
Tính số mol và số gam kali clorat cần thiết để điều chế được:
a) 48g khí oxi.
b) 44,8 lít khí oxi (ở đktc).
a) Phương trình phản ứng:
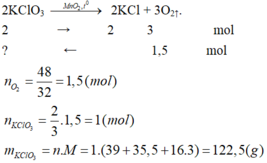
b) Phương trình phản ứng:
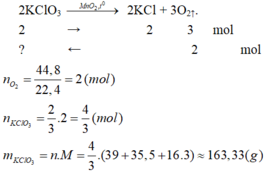
`Tính số mol và số gam Kali Clorat cần thiết để điều chế được :a) 48g khí oxib) 44,8 lít khí oxi ( đo ở đktc )
a) PTHH: 2KClO3-->2KCl + 3O2 1mol <---1mol<---1,5mol nO2=48/32=1,5mol=> nKClO3=1 =>mKClO3=1.122,5=122,5 gamvậy cần 122,5 gam KClO3 để điều chế 48 gam khí oxi
b)PTHH: 2KClO3-->2KCl + 3O2 4/3mol <---4/3mol<---2mol nO2=44,8/22,4=2mol=> nKClO3=4/3mol =>mKClO3=4/3.122,5=163,33333gamVậy cần 163,33333gam KClO3 để điều chế 44,8 lít khí oxi ở đktc
Bài 4: Tính số mol và số gam kali clorat cần thiết để điều chế được:
a) 48g khí oxi.
b) 44,8 lít khí oxi (ở đktc). Bài 6: Trong phòng thí nghiệm người ta điều chế oxit sắt từ Fe3O4 bằng cách dùng oxi hóa sắt ở nhiệt độ cao.
a) Tính số gam sắt và oxi cần dùng để điều chế được 2,32g oxi sắt từ?
b) Tính số gam kali pemanganat KMnO4 cần dùng để có được lượng oxi dùng cho phản ứng trên, biết rằng khi nung nóng 2 mol KMnO4 thì thu được 1 mol O2.
Nung hoàn toàn 1 lượng potassium chlorate (KClO3) thu được 7,437 (lít) khí oxygen ở đkc
a. Viết PTHH xảy ra.
b. Tính khối lượng KClO3 cần cho phản ứng.
Câu 3: Tính số mol và số gam thuốc tím cần để điều chế được:
1. 48 gam khí oxi.
2,24 lít khí oxi ở đktc
1) nO2= 48/32=1,5(mol)
PTHH: 2 KMnO4 -to-> K2MnO4 + MnO2 + O2
nKMnO4=2.1,5=3(mol)
=>mKMnO4=158.3= 474(g)
2) nO2=2,24/22,4=0,1(mol)
nKMnO4=2.0,1=0,2(mol)
-> mKMnO4=158.0,2= 31,6(g)