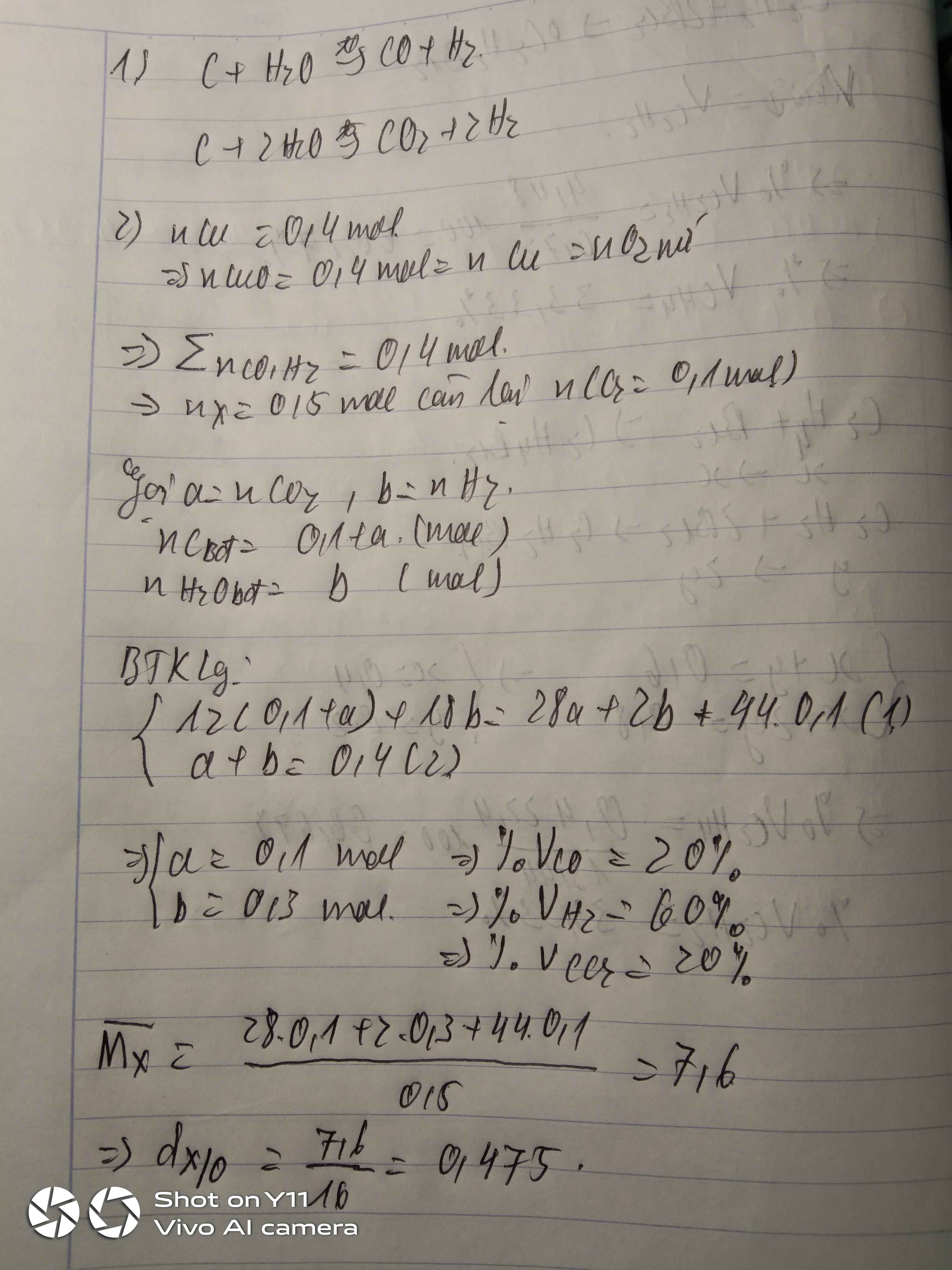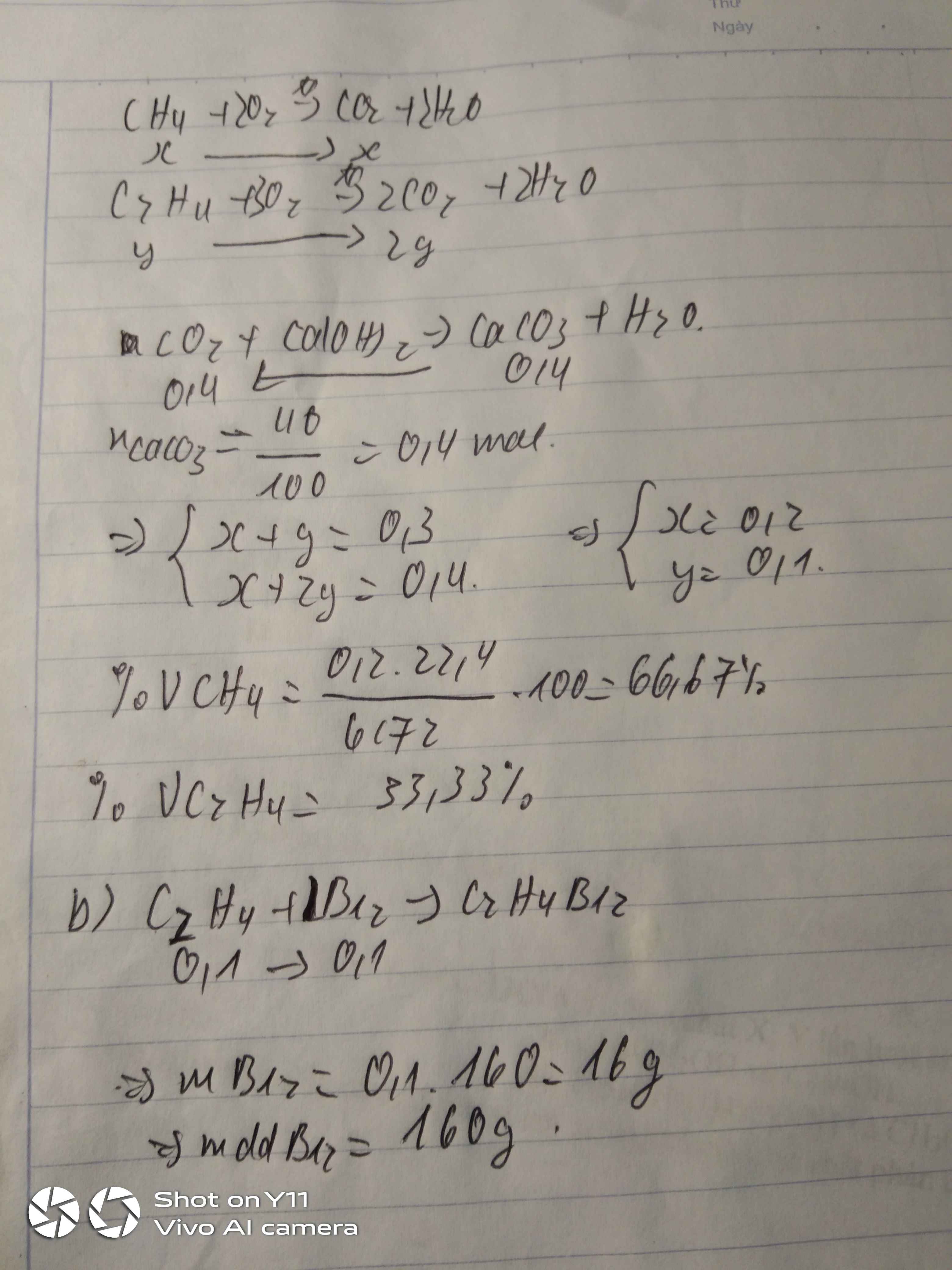Đốt cháy hoàn toàn 6,72 lit hỗn hợp CH4 và C2H4 với 17,92 lit O2 (đkc). a/ Tính % (V) mỗi khí trong hỗn hợp. b/ Dẫn toàn bộ sản phẩm vào dung dịch Ca(OH)2 dư. Tính khối lượng kết tủa.

Những câu hỏi liên quan
4. Đốt cháy hoàn toàn 6,72 lit khí CH4 và C2H4 dẫn sản phẩm qua dd Ca(CH)2 dư sau phản ứng thu được 40g kết tủa
a. Tính %V mỗi khí
b. Dẫn 6,72 lit hỗn hợp khí trên qua Br2. Tính Kl dung dịch Br2 10% đã phản ứng?
a.\(n_{hh}=\dfrac{6,72}{22,4}=0,3mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_4}=y\end{matrix}\right.\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
x x ( mol )
\(C_2H_4+3O_2\rightarrow\left(t^o\right)2CO_2+2H_2O\)
y 2y ( mol )
\(n_{CaCO_3}=\dfrac{40}{100}=0,4mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,4 0,4 ( mol )
Ta có:
\(\left\{{}\begin{matrix}x+y=0,3\\x+2y=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\%V_{CH_4}=\dfrac{0,2}{0,3}.100=66,67\%\)
\(\%V_{C_2H_4}=100\%-66,67\%=33,33\%\)
b.\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
0,1 0,1 ( mol )
\(m_{Br_2}=0,1.160:10\%=160g\)
Đúng 1
Bình luận (0)
Hỗn hợp x gốc CH4 và C2H4 . dẫn 0.1 mol hỗn hợp x vào dung dịch Br2 dư có 0.08 mol khí thoát ra . đốt cháy hoàn toàn 0.1 mol hỗn hợp x bằng O2 rồi dẫn toàn bộ sản phẩm cháy vào dung dịch Ca(OH)2 dư thu dược m g kết tủa . tính m
Xem chi tiết
Đốt cháy hoàn toàn hỗn hợp khí CH4 và C2H4. Dẫn toàn bộ khí thoát ra qua dung dịch nước vôi trong dư thu được 10g kết tủa. Cũng cho hỗn hợp trên tác dụng với 200ml dung dịch Brom 0,2M
a. Tính % thể tích mỗi khí ban đầu
b. Tính khối lượng C2H2Br2
a)
nBr2 = 0,2.0,2 = 0,04 (mol)
nCaCO3 = \(\dfrac{10}{100}=0,1\left(mol\right)\)
PTHH: C2H4 + Br2 --> C2H4Br2
0,04<--0,04---->0,04
C2H4 + 3O2 --to--> 2CO2 + 2H2O
0,04--------------->0,08
CH4 + 2O2 --to--> CO2 + 2H2O
0,02<-------------0,02
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,1<------0,1
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,02}{0,02+0,04}.100\%=33,33\%\\\%V_{C_2H_4}=\dfrac{0,04}{0,02+0,04}.100\%=66,67\%\end{matrix}\right.\)
b) mC2H4Br2 = 0,04.188 = 7,52 (g)
Đúng 4
Bình luận (0)
đốt cháy hết 5,6 lít hỗn hợp gồm CH4 và C2H4 cần dùng 13,44 lít khí oxi
a) viết pthh
b) tính % thể tích trong mỗi khí trong hỗn hợp
c) dẫn toàn bộ sản phẩm tạo thành vào dung dịch Ca(OH)2 dư. tính khối lượng muối tạo thành (các thể tích đo ở đktc)
Theo gt ta có: $n_{O_2}=0,6(mol);n_{hh}=0,25(mol)$
a, $CH_4+2O_2\rightarrow CO_2+2H_2O$
$C_2H_4+3O_2\rightarrow 2CO_2+2H_2O$
Gọi số mol CH4 và C2H4 lần lượt là a;b(mol)
Ta có: $a+b=0,25;2a+3b=0,6\Rightarrow a=0,15;b=0,1$
b, Suy ra $\%V_{CH_4}=60\%;\%V_{C_2H_4}=40\%$
c, Ta có: $n_{CaCO_3}=n_{CO_2}=0,15+0,1.2=0,35(mol)\Rightarrow m_{CaCO_3}=35(g)$
Đúng 2
Bình luận (0)
\(a)\\ CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_4 + 3O_2 \xrightarrow{t^o} 2CO_2 + 2H_2O\\ b)\ V_{CH_4} = a(lít) ; V_{C_2H_4} = b(lít)\\ \Rightarrow a + b = 5,6(1)\\ V_{O_2} = 2a + 3b = 13,44(2)\\ (1)(2)\Rightarrow a = 3,36 ; b = 2,24\\ \%V_{CH_4} = \dfrac{3,36}{5,6}.100\% = 60\%\\ \%V_{C_2H_4} = 40\%\\ c) V_{CO_2} = a + 2b = 7,84(lít)\\\)
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CaCO_3} = n_{CO_2} = \dfrac{7,84}{22,4} = 0,35(mol)\\ \Rightarrow m_{CaCO_3} = 0,35.100 = 35(gam)\)
Đúng 3
Bình luận (0)
a, PT: \(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
b, Giả sử: \(\left\{{}\begin{matrix}n_{CH_4}=x\left(mol\right)\\n_{C_2H_4}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{5,6}{22,4}=0,25\left(1\right)\)
Ta có: \(n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Theo PT: \(n_{O_2}=2n_{CH_4}+3n_{C_2H_4}=2x+3y\)
⇒ 2x + 3y = 0,6 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,15\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,15}{0,25}.100\%=60\%\\\%V_{C_2H_4}=40\%\end{matrix}\right.\)
b, Theo PT: \(n_{CO_2}=n_{CH_4}+2n_{C_2H_4}=0,35\left(mol\right)\)
PT: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_{3\downarrow}+H_2O\)
Theo PT: \(n_{CaCO_3}=n_{CO_2}=0,35\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,35.100=35\left(g\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Hỗn hợp A gồm CH4 và C2H4. Đốt cháy hoàn toàn 5,6 lít hỗn hợp A (đktc) rồi cho toàn bộ sản phẩm cháy vào bình nước vôi trong dư thu được 40 gam kết tủa. Tính % khối lượng mỗi chất trong A ?
chia hỗn hợp A gồm CH4 và C2H4 có khối lượng 3,2 gam thành hai phần không bằng nhau . Phần 1 : hấp thụ hết vào bình chứa dung dịch brom dư, sau phản ứng đã có 3,2 gam brom tham gia phản ứng. Phần 2: đốt cháy hoàn toàn trong khí oxi, rồi dẫn toàn bộ sản phẩm cháy vào dung dịch Ba(OH)2 dư thu được 32,505 gam kết tủa. a) viết các phản ứng xảy ra b) tính khối lượng CH4 trong A
Đốt cháy 2,8 lít hỗn hợp khí CH4 và C2H2 ở đktc cần phải dùng 6,72 lít khí oxi a. Viết PTHH b. Tíng thành phần phần trăm theo thể tích mỗi khí trong hỗn hợp c. Dẫn toàn bộ lượng khí sản phẩm hấp thụ hết vào dung dịch Ca(OH)2 dư, thấy xuất hiện kết tủa. Tính khối lượng kết tủa
\(n_{hhkhí}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\\ n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ Gọi\left\{{}\begin{matrix}n_{CH_4}=a\left(mol\right)\\n_{C_2H_2}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
CH4 + 2O2 \(\underrightarrow{t^o}\) CO2 + 2H2O
a 2a a
2C2H2 + 5O2 \(\underrightarrow{t^o}\) 4CO2 + 2H2O
b 2,5b 2b
Hệ phương trình: \(\left\{{}\begin{matrix}a+b=0,125\\2a+2,5b=0,3\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,025\left(mol\right)\\b=0,1\left(mol\right)\end{matrix}\right.\)
\(\%V_{C_2H_2}=\dfrac{0,1}{0,125}=80\%\\ \%_{CH_4}=100\%-80\%=20\%\)
nCO2 = 2.0,025 + 2.0,1 = 0,25 (mol)
PTHH: Ca(OH)2 + CO2 -> CaCO3 + H2O
0,25 0,25
=> mCaCO3 = 0,25.100 = 25 (g)
Đúng 3
Bình luận (0)
đốt cháy hoàn toàn 1.68l hỗn hợp khí A gồm metan và etilen (đktc) nếu cho toàn bộ sản phẩm vào dd ca(oh) dư thu đc 10g kết tủa. tính thành phần % và khối lượng mỗi khí trong hỗn hợp
\(n_{hh}=\dfrac{V_{hh}}{22,4}=\dfrac{1,68}{22,4}=0,075mol\)
Gọi \(\left\{{}\begin{matrix}n_{CH_4}=x\\n_{C_2H_4}=y\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{CO_2\left(CH_4\right)}=x\\n_{CO_2\left(C_2H_4\right)}=2y\end{matrix}\right.\)
\(n_{CaCO_3}=\dfrac{m_{CaCO_3}}{M_{CaCO_3}}=\dfrac{10}{100}=0,1mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
x+2y x+2y ( mol )
Ta có:
\(\left\{{}\begin{matrix}22,4x+22,4y=1,68\\x+2y=0,1\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,025\end{matrix}\right.\)
\(\%CH_4=\dfrac{0,05}{0,075}.100=66,66\%\)
\(\%C_2H_4=100\%-66,66\%=33,34\%\)
\(m_{CH_4}=0,05.16=0,8g\)
\(m_{C_2H_4}=0,025.28=0,7g\)
Đúng 2
Bình luận (2)
Hỗn hợp X gồm CH4 và c2h6 có tỉ khối so với hiđrô bằng 12,2 đốt cháy hoàn toàn 11,2l khí X hấp thụ hết toàn bộ sản phẩm vào dung dịch Ca(OH)2 dư thu được m gam kết tủa .viết các phương trình phản ứng xảy ra. tính khối lượng kết tủa thu được
Gọi số mol CH4, C2H6 là a, b (mol)
Có: \(\left\{{}\begin{matrix}a+b=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\M_X=\dfrac{16a+30b}{a+b}=12,2.2=24,4\left(g/mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,2---------------->0,2
2C2H6 + 7O2 --to--> 4CO2 + 6H2O
0,3----------------->0,6
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,8---------------->0,8
=> mCaCO3 = 0,8.100 = 80 (g)
Đúng 3
Bình luận (0)