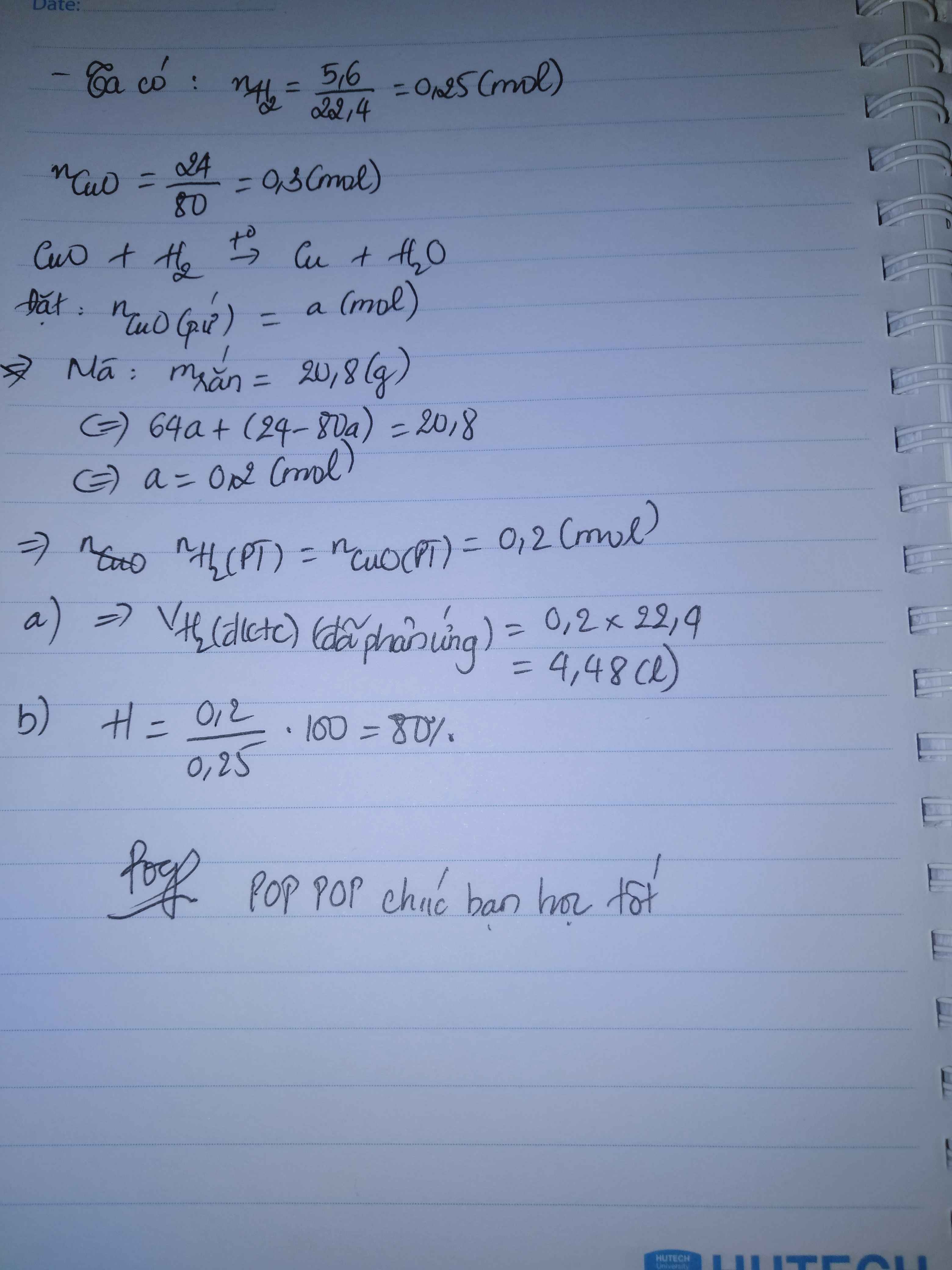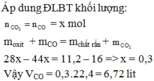dùng 11,2 lít H2(đktc) để khử 48 gam CuO ở nhiệt độ cao. Sau phản ứng được 41,6 gam chất rắn tính hiejeu suất phản ứng tính % thể tích h2 đã phản ứng % khối lượng CuO đã phản ứng

Những câu hỏi liên quan
Dẫn 5,6 lít H2 (đktc) qua ống sứ đựng 24 gam bột CuO ở nhiệt độ cao, sau một thời gian thu được 20,8 gam chất rắn.
a/ Tính thể tích H2 (đkc) đã phản ứng.
b/ Tính hiệu suất phản ứng.
a)
\(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
Xét tỉ lệ \(\dfrac{0,3}{1}>\dfrac{0,25}{1}\)=> Hiệu suất tính theo H2
Gọi số mol CuO phản ứng là a
=> nCu = a (mol)
Có: (0,3-a).80 + 64a = 20,8
=> a = 0,2 (mol)
\(n_{H_2}=n_{CuO}=0,2\left(mol\right)\)
=> \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b) \(H\%=\dfrac{0,2}{0,25}.100\%=80\%\)
Đúng 4
Bình luận (0)
Số mol CuO bài ra là:
\(n_{CuObr}=\dfrac{24}{80}=0,3\left(mol\right)\)
Số mol hidro bài ra là:
\(n_{H_2br}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH
\(CuO+H_2\rightarrow Cu+H_2O\)
\(\dfrac{n_{CuObr}}{n_{CuOpt}}>\dfrac{n_{H_2br}}{n_{H_2pt}}\)
=> CuO dư sau phản ứng, bài toán tính theo hidro
Vậy thể tích hidro đã p/ứ là 5,6(lít)
b, Theo pt: \(n_{H_2}=n_{Cu}=0,25\left(mol\right)\)
Khối lượng Cu sản phẩm là:
\(m_{Cu}=0,25.64=16\left(g\right)\)
Hiệu suất của phản ứng là:
\(H=\dfrac{m_{Cu}}{m_{chat.ran}}.100\%=\dfrac{16}{20,8}.100\%\approx76,92\%\)
Đúng 0
Bình luận (0)
Khử 16 gam hỗn hợp các oxit kim loại : FeO, Fe2O3, Fe3O4, CuO và PbO bằng khí CO ở nhiệt độ cao, khối lượng chất rắn thu được là 11,2 gam. Tính thể tích khí CO đã tham gia phản ứng (đktc)? A. 5,6 lit B. 6,72 lit C. 13,44 lit D. 2,24 lit
Đọc tiếp
Khử 16 gam hỗn hợp các oxit kim loại : FeO, Fe2O3, Fe3O4, CuO và PbO bằng khí CO ở nhiệt độ cao, khối lượng chất rắn thu được là 11,2 gam. Tính thể tích khí CO đã tham gia phản ứng (đktc)?
A. 5,6 lit
B. 6,72 lit
C. 13,44 lit
D. 2,24 lit
hòa tan hoàn toàn 2,7g al vào dung dịch hcl
.a>tính khối lượng hcl đã dùng .b>tính thể tích h2 (đktc) thu được sau phản ứng?P.c>nếu dùng toàn bộ lượng khí h2 bay ra ở trên đem khử 20g bột cuo ở nhiệt độ cao thì chất nào còn dư?dư bao nhiêu gam?a. Để tính khối lượng HCl đã dùng, ta cần biết số mol của Al đã phản ứng với HCl. Ta sử dụng phương trình phản ứng:
2Al + 6HCl → 2AlCl3 + 3H2
Theo đó, 2 mol Al tương ứng với 6 mol HCl. Vậy số mol HCl cần để phản ứng với 2,7 g Al là:
n(HCl) = n(Al) x (6/2) = 2,7/(27x2) x 6 = 0,05 mol
Khối lượng HCl tương ứng là:
m(HCl) = n(HCl) x M(HCl) = 0,05 x 36,5 = 1,825 g
Vậy khối lượng HCl đã dùng là 1,825 g.
b. Theo phương trình phản ứng, 2 mol Al tạo ra 3 mol H2. Vậy số mol H2 tạo ra từ 2,7 g Al là:
n(H2) = n(Al) x (3/2) = 2,7/(27x2) x 3 = 0,025 mol
Theo định luật Avogadro, 1 mol khí ở ĐKTC chiếm thể tích 22,4 L. Vậy thể tích H2 thu được là:
V(H2) = n(H2) x 22,4 = 0,025 x 22,4 = 0,56 L
P.c. CuO + H2 → Cu + H2O
Khối lượng CuO cần để khử hết 0,025 mol H2 là:
n(CuO) = n(H2)/2 = 0,0125 mol
m(CuO) = n(CuO) x M(CuO) = 0,0125 x 79,5 = 0,994 g
Vậy để khử hết H2, ta cần dùng 0,994 g CuO. Nếu dùng toàn bộ lượng H2 bay ra, chất CuO sẽ bị khử hoàn toàn thành Cu và không còn chất nào còn dư.
Đúng 0
Bình luận (0)
Người ta dùng hiđro để khử sắt từ oxit Fe3O4 ở nhiệt độ cao thu được 11,2 gam kim loại sắt.a. Viết phương trình phản ứng xảy ra.b. Tính khối lượng sắt từ oxit đã phản ứng.c. Tính thể tích khí H2 ở đktc cần dùng cho phản ứng.d. Tính khối lượng Zn, khối lượng axit HCl cần dùng để điều chế lượng khí H2 ở trên.cíu em mn ơiiiii, ngày 14/3 em thi ruiiiii
Đọc tiếp
Người ta dùng hiđro để khử sắt từ oxit Fe3O4 ở nhiệt độ cao thu được 11,2 gam kim loại sắt.
a. Viết phương trình phản ứng xảy ra.
b. Tính khối lượng sắt từ oxit đã phản ứng.
c. Tính thể tích khí H2 ở đktc cần dùng cho phản ứng.
d. Tính khối lượng Zn, khối lượng axit HCl cần dùng để điều chế lượng khí H2 ở trên.
cíu em mn ơiiiii, ngày 14/3 em thi ruiiiii
a, \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
b, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PT: \(n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=\dfrac{1}{15}\left(mol\right)\Rightarrow m_{Fe_3O_4}=\dfrac{1}{15}.232=\dfrac{232}{15}\left(g\right)\)
c, \(n_{H_2}=\dfrac{4}{3}n_{Fe}=\dfrac{4}{15}\left(mol\right)\Rightarrow V_{H_2}=\dfrac{4}{15}.22,4=\dfrac{448}{75}\left(l\right)\)
d, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Zn}=n_{H_2}=\dfrac{4}{15}\left(mol\right)\Rightarrow m_{Zn}=\dfrac{4}{15}.65=\dfrac{52}{3}\left(g\right)\)
\(n_{HCl}=2n_{H_2}=\dfrac{8}{15}\left(mol\right)\Rightarrow m_{HCl}=\dfrac{8}{15}.36,5=\dfrac{292}{15}\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 11,2 gam sắt vào một lượng dư axit hcl a Tính thể tích khí hiđro ở đktc b Tính khối lượng axit hcl đã phản ứng c Dùng lượng khí hiđro trên khử CuO ở nhiệt độ cao. Tính khối lượng Cu thu đc
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{H_2}=n_{Fe}=0.2\left(mol\right)\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(n_{HCl}=2n_{Fe}=0.2\cdot2=0.4\left(mol\right)\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
\(CuO+H_2\underrightarrow{t^0}Cu+H_2O\)
\(n_{Cu}=n_{H_2}=0.2\left(mol\right)\)
\(m_{Cu}=0.2\cdot64=12.8\left(g\right)\)
Đúng 1
Bình luận (0)
Bài 4. Khử 40 gam bột CuO nung nóng bằng 3,36 lít khí H2(đktc) a. Sau phản ứng chất nào hết, chất nào dư? Tính khối lượng chất dư? b. Tính khối lượng Cu thu được sau phản ứng? c. Tính khối lượng hỗn hợp rắn thu được sau phản ứng?
\(a.n_{CuO}=\dfrac{40}{80}=0,5\left(mol\right)\\ n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ Vì:\dfrac{0,15}{1}< \dfrac{0,5}{1}\\ \rightarrow CuOdư\\ n_{CuO\left(p.ứ\right)}=n_{Cu}=n_{H_2}=0,15\left(mol\right)\\ \rightarrow n_{CuO\left(dư\right)}=0,5-0,15=0,35\left(mol\right)\\ m_{CuO\left(DƯ\right)}=0,35.80=28\left(g\right)\\ b.m_{Cu}=0,35.64=22,4\left(g\right)\\ c.m_{hh_{rắn}}=m_{Cu}+m_{CuO\left(dư\right)}=22,4+28=50,4\left(g\right)\)
Đúng 1
Bình luận (1)
Bài của câu này đây nha em! Bị lỗi CT anh gõ, thôi anh cap lại từ trang cá nhân của anh!

Đúng 3
Bình luận (1)
Khử 11,2 gam hỗn hợp gồm FeO và CuO bằng khí H2 ở nhiệt độ cao thì thu được 9,28 gam hỗn hợp chất rắn. Biết rằng trong điều kiện thí nghiệm các phản ứng chỉ đạt hiệu suất 80%a) Tính khối lượng mỗi oxit trong hỗn hợp ban đầu.b) Cho hỗn hợp chất rắn thu được sau thí nghiệm trên vào dung dịch H2SO4 loãng dư. Sau khi các phản ứng kết thúc, hãy tính số gam chất rắn không tan và thể tích khí thoát ra? ( đo ở đktc)Giúp mình với:))
Đọc tiếp
Khử 11,2 gam hỗn hợp gồm FeO và CuO bằng khí H2 ở nhiệt độ cao thì thu được 9,28 gam hỗn hợp chất rắn. Biết rằng trong điều kiện thí nghiệm các phản ứng chỉ đạt hiệu suất 80%
a) Tính khối lượng mỗi oxit trong hỗn hợp ban đầu.
b) Cho hỗn hợp chất rắn thu được sau thí nghiệm trên vào dung dịch H2SO4 loãng dư. Sau khi các phản ứng kết thúc, hãy tính số gam chất rắn không tan và thể tích khí thoát ra? ( đo ở đktc)
Giúp mình với:))
a) PTHH : \(FeO+H_2-t^o->Fe+H_2O\)
\(CuO+H_2-t^o->Cu+H_2O\)
Đặt \(\hept{\begin{cases}n_{FeO}=x\left(mol\right)\\n_{CuO}=y\left(mol\right)\end{cases}}\) => \(72x+80y=11,2\left(I\right)\)
Có : \(m_{O\left(lấy.đi\right)}=m_{giảm}=1,92\left(g\right)\)
=> \(n_{O\left(lấy.đi\right)}=\frac{1,92}{16}=0,12\left(mol\right)\) Vì H% = 80% => Thực tế : \(n_{O\left(hh\right)}=\frac{0,12}{80}\cdot100=0,15\left(mol\right)\)
BT Oxi : \(x+y=0,15\left(II\right)\)
Từ (I) và (II) suy ra : \(\hept{\begin{cases}x=0,1\\y=0,05\end{cases}}\)
=> \(\hept{\begin{cases}m_{FeO}=7,2\left(g\right)\\m_{CuO}=4\left(g\right)\end{cases}}\)
b) PTHH : \(Fe+H_2SO_4-->FeSO_4+H_2\)
BT Fe : \(n_{Fe}=n_{FeO}=0,1\left(mol\right)\)
Theo pthh : \(n_{H_2}=n_{Fe}=0,1\left(mol\right)\)
=> \(V_{H_2}=2,24\left(l\right)\)
BT Cu : \(n_{Cu}=n_{CuO}=0,05\left(mol\right)\)
=> \(m_{CR\left(ko.tan\right)}=0,05\cdot64=3,2\left(g\right)\)
Bài 5: Dẫn khí H2 đi qua ống thủy tinh chưa 16 gam bột CuO màu đen nung đến 4000C .
a) Tính khối lượng nước tạo thành nếu lượng CuO phản ứng chiếm 80% lượng ban đầu.
b) Tính khối lượng chất rắn sau phản ứng nếu đã dung 3,36 lit H2 ở đktc và phản ứng xảy ra hoàn toàn.
c) Tính hiệu suất phản ứng theo CuO nếu khối lượng chất rắn thu được sau phản ứng nặng 13,28 gam
a) \(CuO+H_2-^{t^o}\rightarrow Cu+H_2O\)
\(n_{CuO\left(bđ\right)}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(\Rightarrow n_{CuO\left(pứ\right)}=0,2.80\%=0,16\left(mol\right)\)
\(n_{H_2O}=n_{CuO}=0,16\left(mol\right)\)
=> \(m_{H_2O}=0,16.18=2,88\left(g\right)\)
b) \(n_{H_2}=0,15\left(mol\right)\)
Lập tỉ lệ : \(\dfrac{0,2}{1}>\dfrac{0,15}{1}\Rightarrow\)Sau phản ứng CuO dư
Chất rắn sau phản ứng là Cu, CuO dư
\(m_{cr}=0,15.64+\left(0,2-0,15\right).80=13,6\left(g\right)\)
c) Gọi x là số mol CuO phản ứng
\(m_{cr}=\left(0,2-x\right).80+64x=13,28\)
=> x=0,17 (mol)
\(H=\dfrac{0,17}{0,2}.100=85\%\)
Đúng 3
Bình luận (2)
Bài 5: Dẫn khí H2 đi qua ống thủy tinh chưa 16 gam bột CuO màu đen nung đến 4000C .
a) Tính khối lượng nước tạo thành nếu lượng CuO phản ứng chiếm 80% lượng ban đầu.
b) Tính khối lượng chất rắn sau phản ứng nếu đã dung 3,36 lit H2 ở đktc và phản ứng xảy ra hoàn toàn.
c) Tính hiệu suất phản ứng theo CuO nếu khối lượng chất rắn thu được sau phản ứng nặng 13,28 gam